脊髓損傷,往往發生得突然,卻帶來長期甚至終身的影響。在經歷了急救、手術、康復訓練之后,許多患者會逐漸進入一個相對穩定的階段——生命體征平穩,病情不再惡化,但肢體功能、感覺恢復卻十分有限。
正是在這樣的背景下,“干細胞移植治療脊髓損傷的手術”逐漸進入公眾視野。它被寄予改善功能的希望,同時也伴隨著疑問與爭議。
那么,這種手術到底是怎么做的?是否真的適合脊髓損傷患者?本文將圍繞手術本身,進行系統梳理。
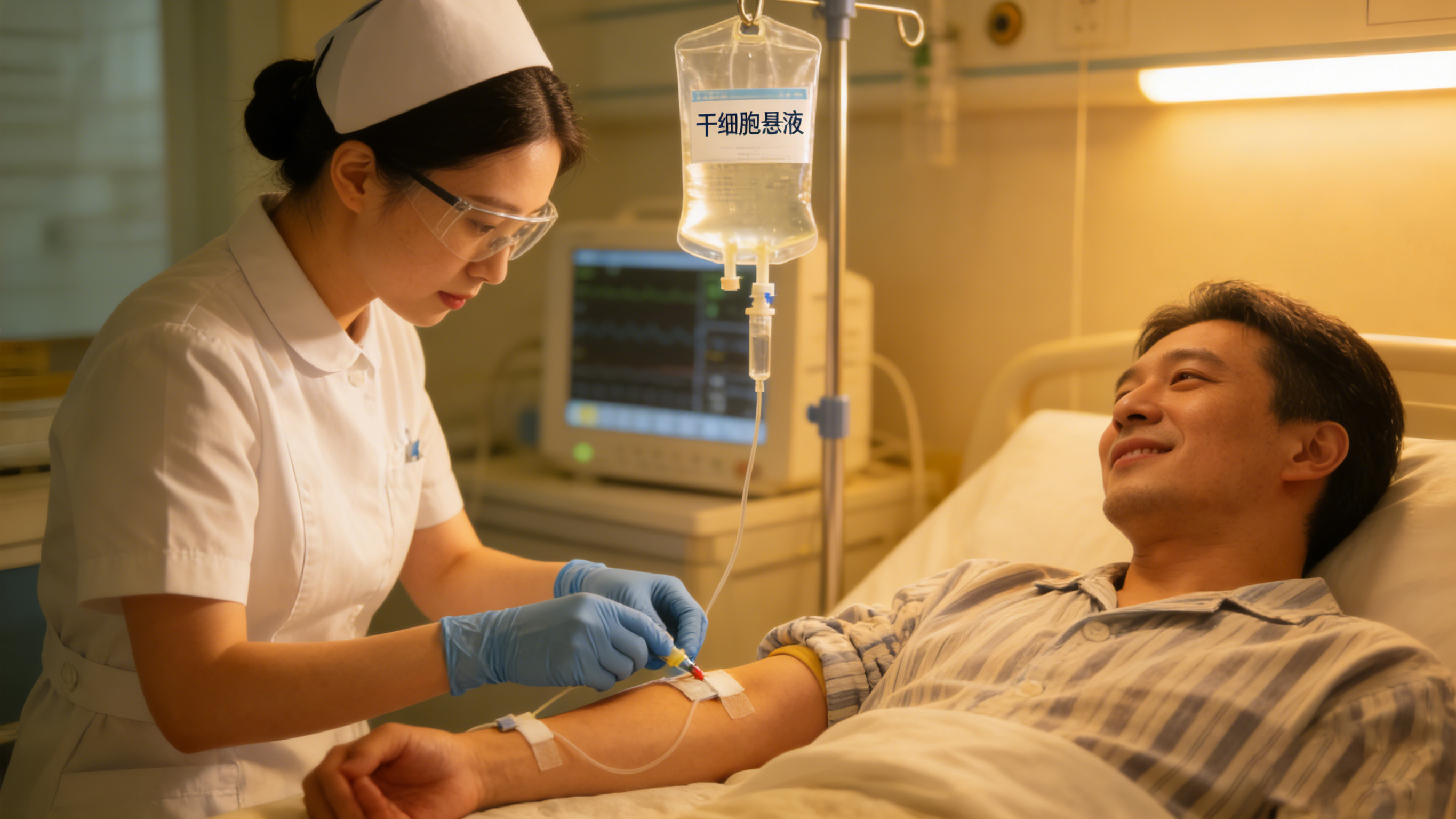
干細胞移植保護危險:5種常見手術方式介紹
一、什么是干細胞移植治療脊髓損傷的手術?
首先需要明確,干細胞手術并非傳統意義上的開刀切除或縫合,而更準確地應稱為 “干細胞移植術”或“細胞輸注術” 。
其核心是將體外制備、具有再生和修復潛能的干細胞,通過特定的方式(如注射)植入患者體內,目標是促進受損脊髓的修復。
它是一種生物療法,而非結構外科手術,旨在從細胞層面干預疾病進程。
二、干細胞移植手術與傳統手術有什么不同?
干細胞移植手術與傳統手術在目標、機制和方式上存在根本差異:
| 比較維度? | 傳統手術? | 干細胞手術? |
|---|---|---|
| 治療目標? | 穩定脊柱結構、解除壓迫 | 促進神經再生,重建功能 |
| 作用機制? | 機械性固定與減壓 | 細胞替代、營養分泌、免疫調節 |
| 技術特點? | 依賴物理植入物(如鋼釘) | 依賴活性細胞與生物材料 |
| 療效范圍? | 有限的功能恢復,無法解決神經壞死 | 潛在改善運動、感覺及自主神經功能 |
| 干預時機? | 主要針對急性期損傷 | 可覆蓋急性期、亞急性期與部分慢性期患者 |
| 技術復雜性? | 操作標準化程度高 | 需個體化細胞制備與精準移植 |
| 長期影響? | 僅能維持現狀,無法逆轉損傷 | 可能實現神經功能的漸進性恢復 |
三、干細胞移植手術的核心原理與細胞選擇
干細胞修復脊髓損傷的機制主要體現在三方面:
- 細胞替代與分化:干細胞可分化為神經元、少突膠質細胞等神經細胞,替代受損組織;
- 旁分泌效應:分泌神經營養因子(如BDNF、GDNF),抑制炎癥反應,促進內源性修復;
- 結構橋接:結合生物支架填充損傷空洞,引導軸突再生與神經回路重建。
目前臨床常用的干細胞類型包括:
- 間充質干細胞(MSCs):來源廣泛(骨髓、脂肪、臍帶),免疫排斥風險低,主要通過營養支持與免疫調節發揮作用;
- 神經干細胞(NSCs):可分化為多種神經細胞,具有向神經元、星形膠質細胞和少突膠質細胞分化的能力,更貼近脊髓組織本身的生物學特性,被認為在神經結構修復和功能重建方面具有獨特潛力;
- 誘導多能干細胞(iPS細胞):可定向分化為神經細胞,避免倫理爭議,但需嚴格控制癌變風險。
四、常見的干細胞移植治療脊髓損傷的手術有哪些?
根據細胞類型、遞送方式和技術組合的不同,目前干細胞主要有以下5種手術或治療策略。[1][2]
1.局部(髓內 / 病灶周圍)移植
操作方式:在手術顯微鏡或術中影像導航的精確引導下,將干細胞懸液直接注射到脊髓損傷的病灶內部或緊鄰區域。
核心優點:定位精準,能使高濃度的細胞直接作用于損傷靶點;便于與生物材料原位復合。
主要考量:屬于有創手術操作,對醫療團隊的技術與設備要求高;理論上伴隨的手術相關風險(如出血、感染、額外損傷)相對高于微創方式。
2.鞘內(腦脊液途徑)注射
操作方式:通過腰椎穿刺,將細胞注入包裹脊髓的蛛網膜下腔腦脊液中,使其隨腦脊液循環分布。
核心優點:操作微創、簡便,易于重復治療,患者耐受性好。
主要考量:細胞在循環過程中會擴散,實際抵達特定損傷部位的細胞數量有限且不精確,療效個體差異較大。
3.靜脈或動脈輸注(系統性給藥)
操作方式:通過外周靜脈或針對脊髓供血動脈的選擇性插管,輸注干細胞或其衍生物(如外泌體)。
核心優點:創傷最小,操作便捷,系統性給藥可能調節全身免疫狀態。
主要考量:絕大多數細胞無法有效穿越“血-脊髓屏障”進入損傷核心,靶向效率很低;主要依賴細胞的遠程旁分泌效應發揮作用。
4.細胞+生物材料/支架聯合移植
操作方式:將干細胞預先負載于特制的生物支架或水凝膠中,再手術植入已清創的損傷空腔。
核心優點:材料為細胞提供三維支撐,能顯著提高細胞滯留率、引導神經有序再生,并可協同緩釋活性因子。
主要考量:技術體系復雜,是前沿研究熱點;生物材料的長期安全性、降解速率及與宿主的整合效果需要嚴格評估。
5.聯合干預策略
操作方式:在細胞移植前后或同時,輔助應用神經營養因子、免疫調節藥物、物理刺激(如電刺激)等手段,旨在優化損傷局部的微環境。
核心優點:通過“組合拳”方式,針對修復的多重障礙進行協同干預,理論上能顯著提升細胞存活與功能整合效率。
主要考量:治療方案高度復雜,變量多,需在嚴謹的臨床研究框架下探索最佳組合與時序。
五、干細胞移植手術的一般流程是怎樣的?
盡管不同機構方案存在差異,但通常包括以下幾個步驟:
1.術前評估:包括影像學檢查、神經功能分級、整體健康評估等。
2.干細胞來源與制備:可能涉及自體或異體細胞,需在合規條件下制備。
3.手術或給藥過程:根據所選路徑實施注射或移植。
4.術后隨訪與康復配合:觀察安全性變化,并結合系統康復訓練。
詳情請瀏覽:癱瘓有望恢復?詳解干細胞治療脊髓損傷的原理、適用人群及治療流程
六、干細胞手術適合所有脊髓損傷患者嗎?
干細胞治療并非對所有脊髓損傷患者都適用。一般臨床和研究經驗提示:
按損傷時期分:
- 亞急性期(損傷后2周–6個月):通常被認為是“窗口期”,局部炎癥逐步受控,內源性修復尚有余地,部分研究顯示該期受益可能較大。
- 慢性期(>6個月):瘢痕形成和組織結構重塑較明顯,理論上更難實現顯著結構性修復,但仍有研究報道功能改善。
按損傷程度分:
- 不完全性損傷(如ASIA B–D):殘存神經傳導通路較多,通常更可能從干細胞或再生療法中獲益。
- 完全性損傷(ASIA A):長期完全截癱患者實現大幅功能恢復的可能性較低,但仍可評估是否有改善自主神經或感覺的機會。
需評估的關鍵指標:年齡、合并疾病(心肺肝腎功能)、是否有活動性感染或惡性腫瘤、凝血功能、呼吸機依賴程度等。
禁忌或需慎重者:活動性感染、嚴重心肺肝腎功能不全、不能配合隨訪或有未控的惡性腫瘤史者通常不適合。
七、干細胞移植手術有風險嗎?安全性怎么樣?
任何醫療干預都不可避免地存在風險,干細胞手術也不例外。其風險主要來自兩方面:
1.移植操作本身的風險:包括麻醉風險、穿刺部位出血、感染、一過性神經根刺激癥狀(疼痛、麻木)等。在經驗豐富的中心,此類風險可控。
2.干細胞相關風險:
- 短期風險:發熱、頭痛、過敏反應等輕微反應。
- 長期與未知風險:這是監管和學術界最關注的核心。包括細胞異常增殖或形成腫瘤、異位組織形成、加重疼痛或痙攣、引發自身免疫反應等。
從目前公開的臨床研究和真實治療數據來看,規范開展干細胞治療在損傷患者中整體安全性是嚴重的,嚴重不良反應發生率極低。
詳情請瀏覽:干細胞治療脊髓損傷有副作用嗎?9年隨訪數據揭示其真實風險與安全性
結語
總體來看,干細胞移植治療手術為脊髓損傷的修復提供了一種全新的醫學思路。隨著再生醫學和細胞技術的不斷發展,相關手術方式、細胞類型及治療流程正在持續完善,并在臨床探索中展現出改善神經功能的潛力。
在規范評估和科學實施的前提下,干細胞移植手術有望為部分脊髓損傷患者帶來新的治療選擇,并與手術、康復訓練等手段協同作用,推動功能恢復向更高水平邁進。未來,隨著研究的深入和經驗的積累,其臨床價值也將更加清晰。
參考資料:
[1]Jin Y, Rong X, Liu H. [Advances in stem cell transplantation for traumatic spinal cord injury at different stages]. Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi. 2023 Jun 15;37(6):721-726. Chinese. doi: 10.7507/1002-1892.202302028. PMID: 37331950; PMCID: PMC10277250.
[2]Platt A, David BT, Fessler ARG. Stem Cell Clinical Trials in Spinal Cord Injury: A Brief Review of Studies in the United States. Medicines (Basel). 2020 May 12;7(5):27. doi: 10.3390/medicines7050027. PMID: 32408562; PMCID: PMC7281746.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信