Meta描述:2026年系統評價納入7項研究123例多系統萎縮(MSA)患者,評估間充質干細胞治療的安全性與有效性。Singer等研究顯示高劑量MSC組UMSARS月進展率顯著低于歷史對照(0.40vs1.44分/月,p=0.004);短期安全性可接受,但動脈注射存在微栓塞風險。證據尚不支持常規臨床應用,需大型III期試驗驗證。
多系統萎縮這種病,最讓人難受的,不只是手抖、走路不穩。很多患者和家屬真正感到絕望的,是眼看著身體一點一點“失守”——從站立時血壓驟降暈厥,到說話含糊不清,再到吞咽困難、臥床不起,而且這個過程往往只有六到十年。現有藥物能緩解一點點癥狀,比如用左旋多巴試試帕金森樣的僵硬,但效果差、時間短。到現在,沒有一個藥能真正把疾病的進展“踩住剎車”。
也正因為這樣,間充質干細胞治療這些年一直被寄予厚望:它能不能靠免疫調節、抗炎這些多靶點作用,讓病情慢下來,哪怕只是慢一點點?
2026最新研究:梳理間充質干細胞治療多系統萎縮(MSA)的安全性與有效性
2026年3月31日,一篇發表在《Biologics: Targets and Therapy》上的系統評價,把過去十年間有關間充質干細胞治療多系統萎縮(MSA)的臨床研究從頭到尾梳理了一遍,給了我們一個目前最完整的答案輪廓[1]。
這篇評價納入了7項研究,共123例MSA患者。其中有5項是早期的單臂試驗,另外2項是隨機對照試驗。干細胞來源五花八門:自體骨髓、脂肪組織,還有異體的。給藥方式絕大多數是鞘內注射,少數用的是靜脈或動脈(表1)。
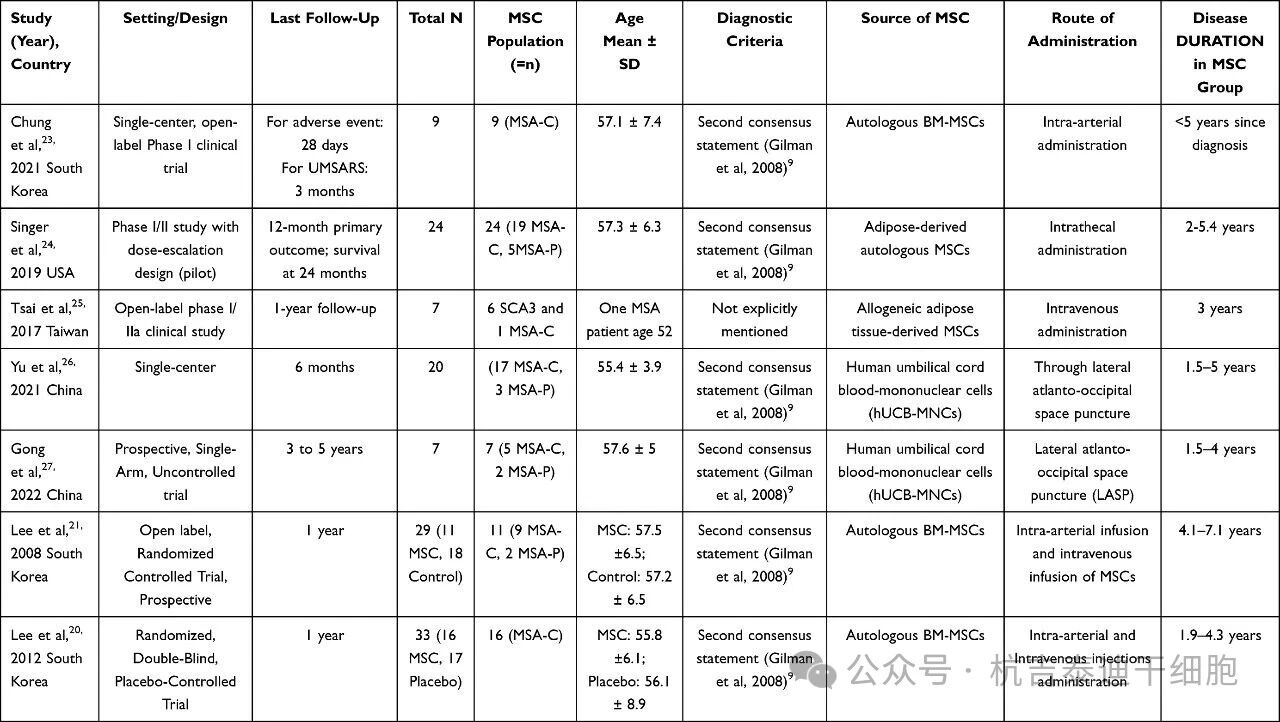
先說大家最關心的結果:多項研究表明,MSC治療確實有可能延緩疾病進展。舉個例子,Singer等人2019年的研究發現,接受高劑量MSC治療的患者,和配對的病史對照組相比,UMSARS總評分的月進展速度明顯更慢(0.40±0.59vs1.44±1.42分/月,p=0.004),提示可能存在劑量依賴性效應。不過,不同研究之間的治療效果差別不小,跟劑量、給藥途徑、疾病處于哪一期都有關系。
總體來看,間充質干細胞療法顯示出通過延緩神經功能惡化來改善MSA病情的潛力。而且耐受性還算不錯。當然,要想真正確認它的臨床療效,還需要更大規模、方案更統一、隨訪時間更長的試驗。
安全性:能接受,但不是“絕對安全”
在現有證據(最長隨訪2年)的前提下,MSC治療MSA的短期安全性可以評為“可接受的”,但絕不是“絕對安全”,見表2。

- 如果你考慮的是鞘內或靜脈輸注:安全性較好,主要風險是輕度的、一過性的操作相關反應,比如頭痛、發熱、背痛,沒有發現嚴重的神經或全身毒性。
- 如果你考慮的是動脈內注射:那就要警惕微栓塞的風險了。雖然目前沒有造成永久性損傷的報道,但應該把它看作一種需要優化方案的高風險途徑。
不管哪種途徑,目前都沒有發現感染、腫瘤或死亡跟MSC直接相關。但遠期安全性仍然是個未知數,需要長期隨訪盯著看。
一句話總結:這項研究告訴我們,MSC治療MSA在短期內“不會捅出大簍子”,但要證明它“長期絕對安全”,還得靠更大樣本、更長時間的研究。
有效性:有積極信號,但還談不上“確鑿證據”
根據現有研究,間充質干細胞治療多系統萎縮的有效性尚未獲得確切的證據,但多個研究顯示出一致且積極的信號。
支持有效性的具體數據信號:在納入的7項研究(共123例患者)中,多個研究報告了積極的療效信號。
Singer等(2019,24例)的隨機、安慰劑對照劑量遞增研究顯示,鞘內注射脂肪來源MSC的高劑量組UMSARS總評分月進展率為0.40±0.59分,顯著低于匹配歷史對照組的1.44±1.42分(p=0.004),且存在劑量依賴性。Lee等(2012,隨機對照)中,MSC組UMSARS總評分和第二部分(運動功能)的增幅均顯著小于安慰劑組(p=0.047和p=0.008)。
在單臂研究中,Yu等(2021,4例)使用臍帶血單核細胞,UMSARS總分從基線23.50±4.72降至隨訪時19.40±4.11,第二部分從30.15±5.63降至24.25±5.05;Gong等(2022,2例)報告治療后3-6個月UMSARS總分從基線42.57±7.96顯著改善至25.71±11.87(p=0.001);Chung等(2021,劑量比較)中,中、高劑量組UMSARS第二部分進展速度慢于低劑量組(組別×時間交互作用p=0.131),雖未達統計學意義但趨勢一致。
總體而言,現有證據支持MSC治療MSA具有延緩疾病進展的潛力,尤其在鞘內或動脈內高劑量給藥時,但由于研究設計偏倚風險高、結果異質性大且缺乏長期隨訪數據,尚不能得出“確切有效”的結論。
背后的機制:它到底怎么起作用的?
第一,旁分泌神經營養支持:MSC通過釋放多種神經營養因子,包括腦源性神經營養因子(BDNF)、膠質細胞源性神經營養因子(GDNF)以及血管內皮生長因子(VEGF),直接給受損的神經元提供生存支持,抑制細胞凋亡,并促進局部微血管的修復與再生。這種旁分泌作用不靠MSC和宿主細胞直接融合,而是通過分泌可溶性因子實現遠距離調控。
第二,免疫調節與內源性干細胞活化:MSC能減少膠質細胞的過度活化和神經炎癥。MSA的病變中,少突膠質細胞內的α-突觸核蛋白聚集會誘發慢性神經炎癥,MSC通過抑制小膠質細胞和星形膠質細胞的促炎表型,減輕對神經元的間接損傷。另外,MSC還能激活宿主腦內的內源性神經干細胞或祖細胞,促進自我修復——這個效應在治療早期最明顯,和臨床上觀察到的短期改善時間窗是吻合的。
第三,MSC歸巢與療效的時間模式:在疾病早期,血腦屏障通透性相對保持得還好,有利于MSC向受損腦區歸巢,進一步增強上述效應。這些機制合在一起,正好解釋了臨床研究中看到的典型時間模式:療效在治療后3-8個月達到峰值,然后逐漸減弱。這說明MSC的旁分泌和免疫調節作用是相對短效的,不是持久的細胞替代,換句話說,可能需要重復給藥才能維持長期療效。
未來研究該往哪兒走?
以后做MSC治療MSA的研究,優先要干的事是搞足夠樣本量的II期和III期隨機對照試驗,看看療效到底能不能超過安慰劑效應和疾病的自然波動。
MSC生產的標準化也迫在眉睫——細胞來源、培養條件、給藥方案和給藥途徑,都得統一,才能做出可靠的比較,找出最佳治療策略。試驗應該重點瞄準MSA的早期階段,因為這時候神經保護干預最可能有效;隨訪時間要拉長(至少24個月),評估重復給藥(可能在首次給藥后6-8個月)的效果。最好再整合一些客觀的生物標志物,比如腦脊液中的炎癥因子、神經絲輕鏈,還有先進的神經影像技術,這樣才能真正驗證機制。
另外,有必要直接對比一下鞘內給藥和動脈內給藥,看看哪個途徑能更好地把藥物送到中樞神經系統,同時把操作風險降到最低。
結論與展望
基于現有證據,可以得出以下結論:
間充質干細胞治療MSA的短期安全性可接受。
- 有效性方面,存在延緩疾病進展的信號,尤其在高劑量、鞘內注射方案中,但尚不能確證。
- 證據等級為低至極低級,不足以支持常規臨床應用。
未來需要大型、多中心、雙盲、安慰劑對照的III期試驗,隨訪至少3–5年,并以硬終點(如生存質量、透析或死亡時間)為主要結局指標。目前Mayo Clinic等機構的II期研究正在進行中,其結果值得期待。
常見問題解答(FAQ)
參考資料:
[1]:Elimam N, Albarari SS, Shaalan Y, Elsheikh SM, Alzamari AA, Elmekkawi N, Mogahed R, Alghuweiri RH. Safety and Efficacy of Mesenchymal Stem Cell Therapy in Multiple System Atrophy: Systematic Review. Biologics. 2026 Mar 31;20:593367. doi: 10.2147/BTT.S593367. PMID: 41938822; PMCID: PMC13050157.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信