核心速覽:間充質干細胞(MSC)通過免疫調節、抗纖維化、促再生及鐵死亡調控四重機制,在肝病治療中展現獨特價值。臨床研究證實,MSC可改善酒精性肝硬化患者Child-Pugh評分(下降2-3分)及白蛋白水平(提升15%-20%);在肝衰竭中,異體MSC輸注將24周生存率從55.6%提升至73.2%;病理研究亦提供了纖維化逆轉的直接組織學證據(Laennec評分顯著降低)。安全性良好,未見致瘤性報告。當前瓶頸在于歸巢效率低與細胞異質性,工程化細胞外囊泡、基因編輯及AI標準化策略正推動臨床轉化。
南方醫科大學最新綜述:間充質干細胞修復肝臟的核心機制與臨床進展
01 引言:肝病治療的未滿足需求與MSC的潛力
肝病(包括肝硬化、病毒性肝炎、酒精性肝病、肝衰竭等)是全球范圍內導致死亡和殘疾的主要原因之一。終末期肝病的唯一根治手段是肝移植,但供體短缺、免疫排斥及高昂費用限制了其廣泛應用。
間充質干細胞憑借其獨特的免疫調節特性、多向分化潛能與旁分泌功能,在肝組織修復與疾病治療領域展現出重要潛力。MSC并非作為“細胞替代物”直接分化為肝細胞,而是以“藥用信號細胞”的身份,通過協同網絡重塑病理微環境。
近期,由廣州南方醫科大學第一臨床醫學院牽頭,聯合深圳市龍華區人民醫院、西安國際大學醫學院共同完成的研究綜述發表于《Frontiers in Medicine》(洛桑版),題為《利用間充質干細胞治療肝病:從機制發現到臨床突破》[1]。本文基于該綜述及其他關鍵臨床證據,系統梳理MSC治療肝病的機制、臨床試驗數據及未來轉化策略。

間充質干細胞(MSCs)在肝病治療中的作用并非依賴單一通路,而是通過協同網絡重塑病理微環境。MSCs并非僅作為細胞替代物,而是以“藥用信號細胞”的身份,通過四個層級協調組織修復:免疫調節、直接抗纖維化干預、促進再生與新興代謝調控。
02 間充質干細胞介導肝臟修復的四大機制
一、免疫調節:重塑肝臟免疫微環境(圖1A)
MSCs通過固有免疫調節能力重塑肝臟微環境,其核心機制在于將巨噬細胞由促炎M1表型極化為抗炎修復型M2表型,這一過程依賴TSG-6、IL-10等可溶性因子。在IFN-γ與TNF誘導的炎癥環境下,MSCs上調PD-L1與IL-10,促進調節性T細胞生成,并通過IDO降解色氨酸抑制CD4+T細胞活化與增殖,同時下調CXCL9等趨化因子,阻斷T細胞遷移。
此外,MSC來源的細胞外囊泡(MSC-EVs)通過抑制MAPK/NF-κB通路中斷B細胞活化級聯反應,而MSCs本身則通過Fas/FasL通路誘導T細胞凋亡,并以IL-6/HGF依賴方式抑制單核細胞分化為樹突狀細胞。上述機制形成正反饋回路,放大IL-10的生成,最終恢復免疫穩態(圖1A)。
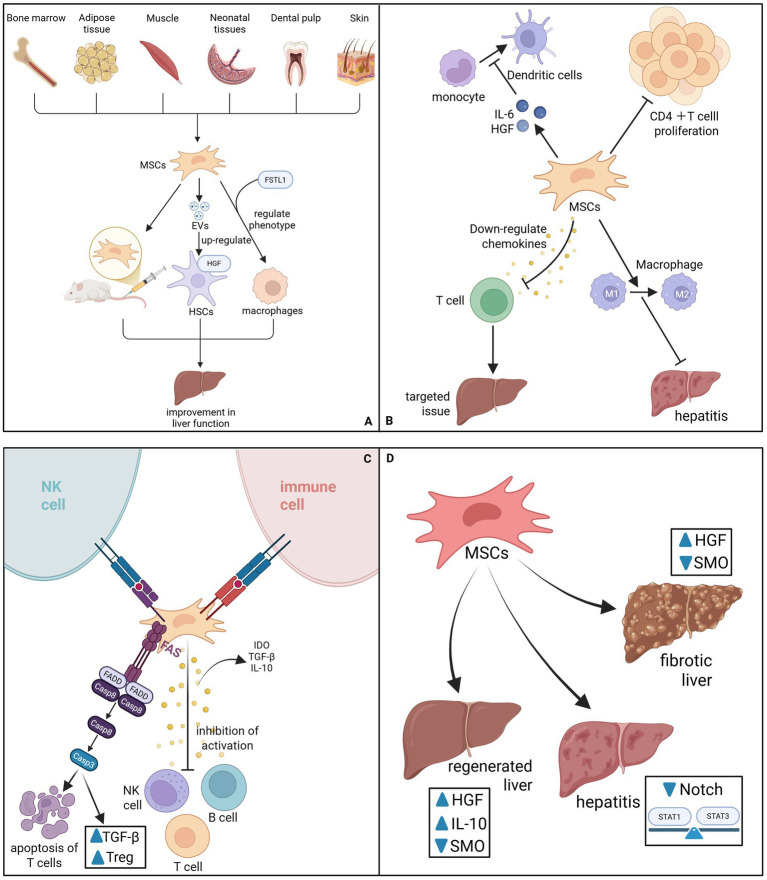
二、抗纖維化活性:直接靶向肝星狀細胞(圖1B)
作為纖維化發生的核心驅動因素,活化的肝星狀細胞(HSC)是間充質干細胞(MSC)的主要治療靶點。
MSCs通過直接干預纖維化級聯反應,實現對活化肝星狀細胞(HSCs)的抑制作用。MSCs及其細胞外囊泡可下調α-SMA、Col1α1及波形蛋白的表達,促使活化的HSCs恢復靜止狀態,這一作用通過旁分泌FSTL1、HGF等因子進一步增強。
與此同時,MSCs通過阻斷Notch信號通路、恢復STAT1/STAT3穩態平衡,并下調Smo表達以抑制Hedgehog/SMO通路,從信號層面拮抗纖維化進程。在基質重塑方面,MSCs分泌MMP-1、MMP-9并下調TIMP,促進已形成的膠原沉積降解(圖1B)。
三、促進血管生成與肝細胞再生(圖1C)
為了促進功能恢復,間充質干細胞(MSCs)提供關鍵的營養支持,刺激內源性修復過程。它們釋放大量生物活性介質,包括肝細胞生長因子(HGF)、血管內皮生長因子(VEGF)和細胞外囊泡(EVs),這些介質協同作用,刺激肝細胞增殖并促進新生血管形成。
在急性肝衰竭中,該旁分泌功能可迅速抑制炎癥并阻止肝損傷進展;經基因工程過表達VEGF的MSCs可進一步增強上述療效。此外,MSC-EVs通過富集lncEEF1G作為競爭性內源RNA,調控miR-181a-5p/HGF軸,增強HSCs中HGF的表達,從而間接促進肝細胞再生(圖1C)。
四、新興機制:鐵死亡調控與線粒體轉移(圖1D)
近期研究進展揭示了間充質干細胞(MSCs)與肝細胞之間復雜的代謝和細胞器水平相互作用,為治療提供了精準的新靶點。
一方面,MSCs經隧道納米管將功能性線粒體轉移至受損肝細胞,恢復GPX4活性與線粒體穩態,抑制脂質過氧化;另一方面,MSCs在鐵死亡調控中呈現雙重作用——臍帶間充質干細胞來源的細胞外囊泡(UC-MSC-EVs)通過外泌體BECN1通路選擇性誘導活化的HSCs發生鐵死亡,降低xc?/GPX4系統活性,而健康肝細胞不受影響。這種“鐵死亡-線粒體軸”既阻斷HSCs活化,又避免全身性鐵代謝紊亂,實現了肝細胞保護與纖維化靶向清除之間的平衡(圖1D)。
03、間充質干細胞治療肝病的臨床試驗
基于間充質干細胞(MSCs)的臨床試驗已覆蓋多種主要肝臟疾病,包括肝硬化、病毒性肝炎、酒精性肝病、肝衰竭及肝移植并發癥(表1)。

細胞來源與給藥方案
目前進入臨床試驗的MSCs主要來源于骨髓、臍帶與脂肪組織。其中臍帶MSCs應用最為廣泛,原因在于其取材無創、倫理爭議小、細胞活性強、增殖能力高,且免疫原性低,異體使用時基本無需配型,便于實現標準化批量制備,成本與質量控制均優于骨髓來源。
給藥方式以靜脈輸注為主,操作簡便,但肝臟歸巢效率有限。部分研究選擇肝動脈或門靜脈直接輸注,實現細胞向肝臟的“定向投放”,理論療效更優,但操作風險相應增加,需介入科配合。劑量范圍跨度較大,從5×10?至5×10?個細胞/公斤不等,目前尚無統一標準,各中心仍處于經驗積累階段。
不同肝病的療效數據
酒精性肝硬化:NCT03838250II期試驗采用自體骨髓MSCs,結果顯示Child-Pugh評分平均下降2至3分,血清白蛋白提升15%至20%。長期隨訪至75個月,生存率明顯優于對照組,為終末期肝病提供了較為堅實的數據支持。
病毒性肝炎:該類試驗中MSCs通常聯合抗病毒藥物使用,主要效果體現在炎癥控制方面,IL-6、TNF-α等炎癥因子水平顯著下降,但病毒載量未受明顯影響,提示MSCs發揮免疫調節而非抗病毒作用。
肝衰竭:NCT01322906試驗采用異體骨髓MSCs,24周生存率為73.2%,顯著高于標準治療組的55.6%,差異近18個百分點。值得注意的是,該療效在聯合血漿置換基礎上實現,提示MSCs在肝衰竭等急重癥中更適合作為綜合治療策略的一部分。
終末期肝病:NCT01224327試驗采用異體臍帶MSCs經肝動脈輸注,結果顯示MELD評分明顯下降,凝血功能改善,且療效與自體MSCs相當。該發現表明,異體細胞在終末期患者中同樣有效,并可規避自體細胞功能受損的問題。
纖維化逆轉:NCT01741090試驗從病理層面進行評估,肝硬化患者接受自體骨髓MSCs后,Laennec纖維化評分顯著降低,提供了組織學上纖維化逆轉的直接證據,終點指標較為堅實。
安全性數據
安全性是MSCs臨床研究中較為一致的領域。超過90%的試驗報告的不良反應主要為短暫性發熱(發生率約5%至10%)及注射部位不適。嚴重不良事件少見,目前所有公開發表的臨床試驗中均未觀察到致瘤性,這對細胞治療領域而言是一項關鍵優勢。
療效差異的影響因素
不同試驗間的療效差異較為明顯,主要原因包括:一是細胞來源不同,骨髓、臍帶與脂肪來源的MSCs生物學特性存在差異,難以直接比較;二是患者狀態不同,代償期與失代償期肝硬化對治療的反應存在顯著差異;三是劑量與給藥方式缺乏標準化,靜脈與肝動脈輸注、單次與多次給藥、劑量從數百萬至數千萬不等,均導致療效難以橫向對比。
自體與異體移植的選擇
從現有臨床實踐看,選擇傾向大致如下:代償期肝硬化患者自體骨髓或脂肪來源MSCs功能通常正常,自體移植可規避免疫排斥風險,無需配型與供體問題,為首選方案。
失代償期肝硬化或肝衰竭患者自身處于嚴重炎癥狀態,自體MSCs功能常受損,異體MSCs更具優勢。從病種來看,肝炎與肝硬化以自體移植為主,肝衰竭則以異體移植為主。
目前MSCs治療肝病面臨兩大瓶頸:歸巢效率低——靜脈輸注后多數細胞滯留于肺部,抵達肝臟者甚少;細胞異質性——同一批次中不同亞群療效差異顯著,質量控制難度較大。
04 當前瓶頸與臨床轉化新興策略
促進臨床轉化的新興策略包括:
第一,以工程化細胞外囊泡為核心的無細胞療法精準化策略:間充質干細胞來源的細胞外囊泡(MSC-EVs)是間充質干細胞旁分泌效應的關鍵介質。它們通過攜帶包括miRNA和細胞因子在內的生物活性分子來調節肝臟免疫穩態。這一過程抑制IL-6和IL-1β等促炎因子,同時平衡Th17/Treg細胞比例,最終緩解慢性肝臟炎癥和纖維化。
研究表明,靜脈注射的MSC-EVs主要積聚在肝臟中,其小尺寸(<200nm)有利于穿透組織屏障。這一特性表明其在肝硬化和脂肪性肝炎模型中具有治療潛力(圖2A)。早期臨床試驗(ChiCTR2300075676)已初步證實其安全性。然而,仍需進行大規模療效驗證。

與天然分泌的間充質干細胞來源的細胞外囊泡(MSC-EVs)相比,后者本身就具有良好的生物分布和低免疫原性,而工程化細胞外囊泡則經過人為修飾,以提高其治療的精準性和療效。這些修飾包括用靶向配體(例如RGD或GE11肽)進行表面功能化,以改善組織特異性遞送;或負載核酸(例如siRNA或lncRNA)以調控受體細胞的基因表達。這些策略性的改進凸顯了工程化細胞外囊泡作為下一代無細胞療法的巨大潛力,使其具有更強的靶向性和再生能力。
第二,結合基因編輯與生物材料工程的細胞功能強化與遞送系統優化策略:利用CRISPR/Cas9等工具對MSCs進行預編輯(如敲除Smad7或導入IL-12),可從源頭增強其免疫調節或抗腫瘤功能;誘導多能干細胞來源的MSCs則為標準化、規模化生產提供了可復制的細胞平臺。與此同時,生物材料工程(如脫細胞ECM水凝膠、MSCs球體培養)通過模擬肝臟微環境,顯著提升工程化MSCs及其分泌的SpEVs在體內的存活率、滯留時間與生物學功能。
這種“細胞內源工程化+外源微環境模擬”的組合有望通過協同效應放大治療效果,但其長期安全性(如插入突變風險)及材料免疫原性的精細調控仍是臨床轉化前必須攻克的關鍵問題。
第三,依托跨學科技術整合與標準化體系的全鏈條創新策略:人工智能通過解析多組學數據與動態分子網絡,正在解決MSCs異質性這一核心生產痛點,實現從培養參數優化(如缺氧預處理時間)到高效批次篩選的智能化質控。納米技術與機械灌注等前沿手段進一步拓展治療場景:前者通過表面修飾提升EVs靶向性,后者聯合EV脫細胞療法直接應用于移植器官修復。
然而,上述技術的臨床落地高度依賴建立從EV分離鑒定到CRISPR遞送的全流程GMP標準化體系,并通過多學科驗證機制確保跨技術整合(如AI+納米材料、機械灌注+細胞療法)的療效穩定性與安全性,最終為實現基于患者疾病分型的個性化聯合治療奠定基礎。
05 結論與研究展望
核心結論
本研究明確,間充質干細胞治療肝病最核心且證據最為充分的機制與療效在于:其作用主要依賴旁分泌因子介導的免疫調節與基質重塑,而非直接分化。
具體而言:
- 抑制肝星狀細胞活化并誘導其凋亡
- 將巨噬細胞由促炎M1型極化為抗炎M2型
- 調控膠原降解相關酶系
上述機制在多種動物模型及I/II期臨床試驗中持續降低纖維化指標并改善肝功能合成指標,是MSC發揮肝臟修復作用最可重復且臨床證據最堅實的核心機制。
未來三大轉化方向
| 方向 | 具體策略 | 目標 |
|---|---|---|
| 優化細胞來源 | 推進iPSC-MSCs;探索肝臟駐留MSCs | 解決供體短缺,提高肝臟相容性 |
| 提高靶向特異性 | CRISPR介導歸巢受體過表達;EV表面修飾;生物材料支架 | 實現精準遞送與局部滯留 |
| 評估長期安全性 | 大規模、多中心、長期隨訪(≥5年)臨床試驗 | 系統評估致瘤性與慢性免疫風險 |
研究強調,只有系統性地填補上述知識空白并推進相關方向,基于MSC的療法才能最終成為安全、可及的終末期肝病常規治療手段。
06 常見問題解答(FAQ)
參考資料:
[1]:Huang Y, Cheng R, Wang G, Xu Z, Liu S, Wan Y, Hou X, Wang J. Harnessing mesenchymal stromal cells for liver disease therapy: from mechanistic discoveries to clinical breakthroughs. Front Med (Lausanne). 2026 Feb 4;12:1677021. doi: 10.3389/fmed.2025.1677021. PMID: 41717346; PMCID: PMC12913439.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信