Meta描述:2026年4月6日,上海愛薩爾獲全國首張干細胞《藥品生產許可證》(滬20260315),其膝骨關節炎干細胞注射液已進入臨床III期,預計2027-2028年獲批上市。本文解讀首證意義、818號令影響及產業格局。
核心速覽
| 獲證企業 | 上海愛薩爾生物醫藥股份有限公司 |
| 許可證編號 | 滬20260315 |
| 核發日期 | 2026年4月6日 |
| 生產范圍 | IxCell hUC-MSC-O注射液(僅限注冊申報使用) |
| 核心產品適應癥 | 膝骨關節炎(國內首個進入臨床III期的干細胞藥品) |
| 預計上市時間 | 2027-2028年 |
| 政策背景 | 國務院818號令將于2026年5月1日正式實施 |
2026年首張干細胞生產許可證落滬,治膝蓋的干細胞新藥離上市只差最后一步
2026年4月6日,上海市藥監局正式核發今年全國首張干細胞《藥品生產許可證》,上海愛薩爾生物醫藥股份有限公司成為新年首位獲證企業,許可證編號為滬20260315。許可信息顯示,其生產范圍包括治療用生物制品:IxCell hUC-MSC-O注射液(僅限注冊申報使用)。
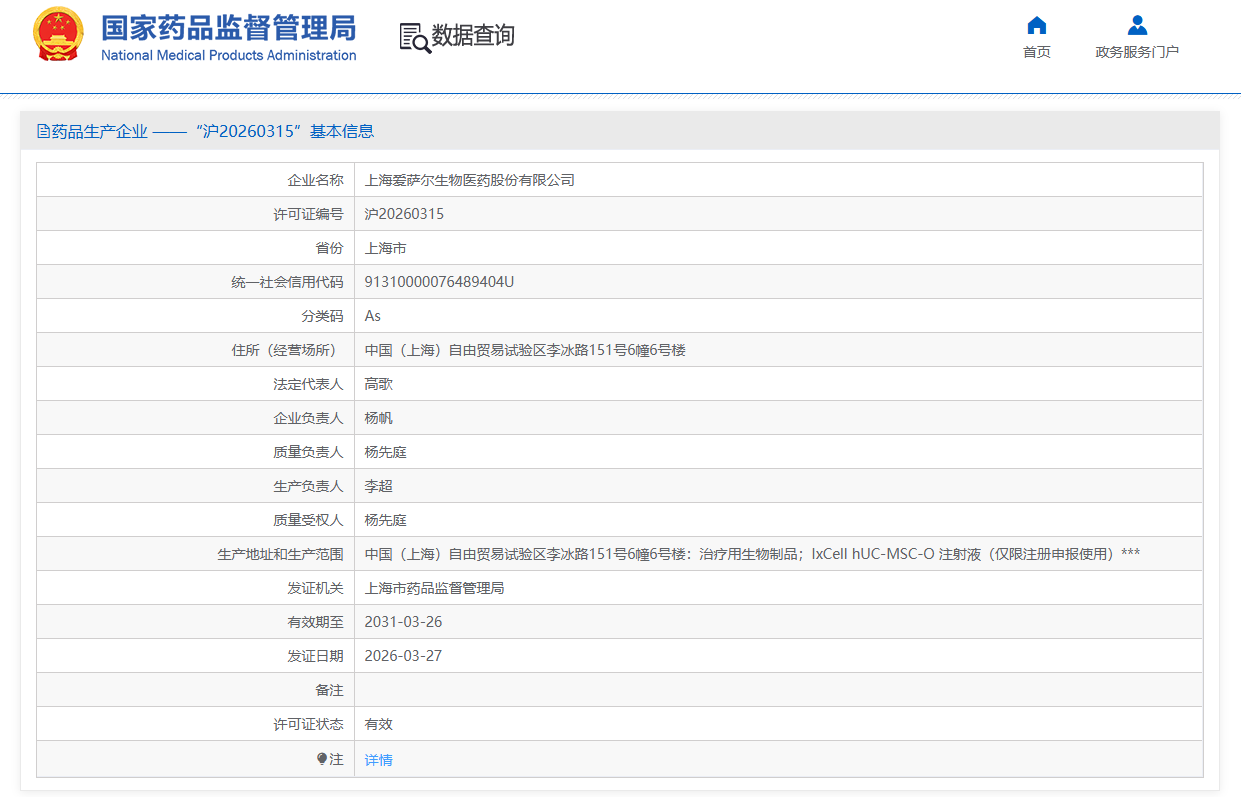
這張許可證的核發,距離國務院818號令(《生物醫學新技術臨床研究和臨床轉化應用管理條例》)2026年5月1日正式實施尚不足一個月,是中國干細胞產業從“科研備案時代”跨入“藥品生產時代”的標志性事件。
一、首證之“首”:一張許可證意味著什么?
干細胞領域的監管,長期處于一種尷尬的灰色地帶。過去十幾年,干細胞治療更像一個“江湖傳說”——你在網上搜索“干細胞”,跳出來的大多是“返老還童”“包治百病”之類的營銷話術。真正能拿到國家藥監局認可、可以按藥品來生產的,幾乎沒有。
為什么?因為監管體系一直未能完成從“科研管理”到“藥品監管”的過渡。以前你可以在實驗室里做干細胞,可以在醫院里用干細胞做研究,但你不能像生產藥片一樣,在符合GMP標準的車間里批量生產干細胞注射液,然后面向患者銷售。因為沒證。
生產許可證,是藥品上市的最后一道“準生證”門檻。它意味著企業已經通過了藥品監管部門對生產條件的全面核查,具備了符合《藥品生產質量管理規范》(GMP)的商業化生產能力。對于干細胞這種“活的藥物”而言,生產環節的質量控制遠比化學藥復雜——從供者材料的采集、運輸,到細胞在實驗室中的分離、培養、擴增,再到成品凍存、復蘇、放行,任何一個環節出現偏差,都可能影響最終產品的安全性和有效性。
正因如此,國家藥監局核查中心于2026年1月發布的《細胞治療產品生產檢查指南》明確要求,細胞治療產品的生產全過程必須實現數據可追溯、質量可管控。

愛薩爾能夠成為“2026年全國首張”或“上海市首張”干細胞《藥品生產許可證》獲證的企業,意味著其生產體系已經通過了這一極其嚴苛的審查。這不僅是企業自身的里程碑,也是整個行業的一個信號:干細胞終于被當作“藥品”來管了。
二、愛薩爾是誰?為什么是它?
說實話,如果不是這張證,很多人沒聽過愛薩爾。
它2013年在張江成立,創始團隊從哈佛、耶魯回來。頭三年基本在“燒錢積累”——做iPSC分化技術、建干細胞擴增平臺。那時候國內干細胞賽道還很冷,資本不看好,政策也不明朗。
轉機出現在2016年底。國家藥監局明確:細胞治療產品可以按藥品申報。愛薩爾是第一批反應過來的人。公司核心團隊甚至參與了國內首個細胞藥品指導原則的制定——這意味著他們從一開始就知道“游戲規則”怎么寫。
目前愛薩爾手里最有價值的產品,是治療膝骨關節炎的間充質干細胞注射液。
核心產品管線方面,愛薩爾覆蓋了間充質干細胞(MSC)、誘導多能干細胞(iPSC)和免疫細胞三大領域,在研管線涵蓋膝骨關節炎、腦卒中、肺纖維化、風濕免疫及實體瘤等多個重大疾病領域。具體而言:
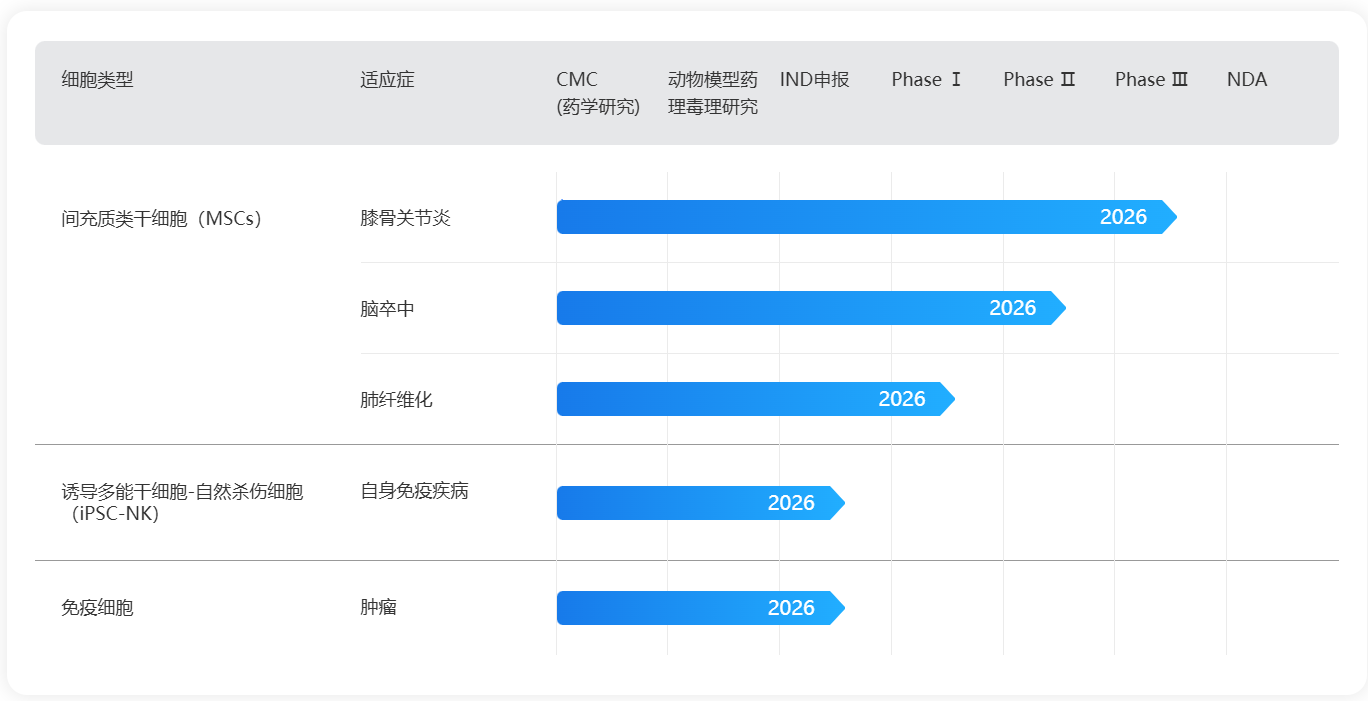
- 膝骨關節炎:間充質干細胞藥品是國內首批獲得臨床試驗默示許可的在研干細胞產品,也是目前國內首個進入臨床III期的在研干細胞藥品。目前該產品的III期臨床試驗以上海交通大學附屬第九人民醫院為組長單位,聯合首都醫科大學附屬北京潞河醫院、南方醫科大學南方醫院、深圳市人民醫院、廣州市第一人民醫院、西安市紅會醫院、北京醫院等多家三甲醫院共同推進。
- 腦卒中:間充質干細胞治療缺血性腦卒中已進入I期臨床試驗,由首都醫科大學宣武醫院牽頭。
- 肺纖維化:間充質干細胞治療結締組織病相關間質性肺病處于臨床前研發階段,已完成IND申報準備。
- iPSC-NK治療自身免疫疾病:利用誘導多能干細胞來源的自然殺傷細胞,通過清除致病性T細胞實現免疫調節,處于臨床前階段。
- 免疫細胞治療腫瘤:來源于肝癌患者的混合免疫細胞(包括γδT細胞、NK細胞和iNKT細胞)產品,具備肝歸巢和肝駐留能力,處于臨床前階段。
截至目前,公司已獲得細胞治療相關發明專利40余項,在張江建立了集研發和生產為一體的4000平方米細胞藥品產業化基地,獲得了國家高新技術企業、上海市專精特新中小企業等榮譽資質。
資本方面:2025年8月,上市公司吉貝爾聯合華甌創投、瓴真基金等機構共同參與了愛薩爾的新一輪融資,通過押注不同適應癥與技術路徑的干細胞療法,搶占行業即將到來的商業化紅利。
產業化布局方面:2026年3月,愛薩爾與南昌高新區正式簽約,落地“細胞技術全景化研發與產業化基地”項目。項目分兩期實施:一期重點建設干細胞治療、免疫細胞治療研發管線,同步搭建臨床級別培養基開發平臺及干細胞藥品生產銷售中心;二期規劃建設細胞治療產品專業化生產基地,進一步擴大產能。
臨床轉化應用方面:2025年4月,愛薩爾與海南帝灣醫院、瑞金醫院海南醫院合作,在海南博鰲樂城國際醫療旅游先行區成功獲批并完成了國內首例合規收費的人臍帶間充質干細胞治療膝骨關節炎臨床轉化應用。該項目以3%的通過率獲批,采用膝關節腔內注射的貨架藥品(復蘇即用),標志著中國細胞藥物產業在合規收費臨床應用方面邁出了關鍵一步。
三、818號令是什么?為什么大家都在提?
國務院第818號令,全稱《生物醫學新技術臨床研究和臨床轉化應用管理條例》,2025年9月通過,2026年5月1日正式實施。
簡單說,這部法規解決了干細胞行業最大的問題:誰來管?怎么管?
過去,干細胞監管是“九龍治水”——衛健委管臨床研究,藥監局管藥品審批,科技部管科研項目,但誰都沒有真正管住那些市場化的亂象。818號令明確了幾件事:
第一,以后做干細胞臨床研究,必須在三甲醫院,而且要通過倫理委員會和學術委員會的雙重評審。
第二,所有臨床研究要向國家衛健委備案,衛健委有權隨時叫停。
第三,如果想按藥品上市,就走藥監局的藥品注冊路徑;如果是個性化治療,走衛健委的醫療技術路徑。
這就是業內常說的“雙軌制”。
愛薩爾這張生產許可證,是藥品路徑上的一個重要節點。它恰好趕在818號令正式實施前不到一個月發出來,時間點很微妙——既像是給新規“獻禮”,又像是在搶跑。因為一旦新規全面落地,審批流程可能會更復雜。現在拿證,等于提前鎖定了合規身份。
四、行業格局:誰在領跑?誰能突圍?
愛薩爾不是一個人在戰斗。在干細胞藥物研發的賽道上,中國的“第一梯隊”已經初步成型。
從整體數據來看,截至2025年底,全國已有超過200款干細胞藥物臨床試驗申請獲得受理,其中超過150款已獲準開展臨床試驗。地域格局上,上海、北京與廣東構成了第一梯隊,三地合計受理數量占據全國半數以上。2026年以來,干細胞新藥研發呈現持續活躍態勢——普華賽爾生物、生創科技等企業的多個干細胞產品相繼獲得臨床試驗批件。
在進入臨床III期的干細胞產品方面,中國目前至少有6個產品已經進入這一沖刺階段,愛薩爾是其中走得最靠前的之一。按照研發進度,這批產品有望在2026-2027年間陸續獲批,形成國內干細胞治療的首個上市高潮。
在國際競爭格局方面,美國的FDA通過“再生醫學先進療法(RMAT)”通道和“國家優先券”試點機制,部分藥品審評周期已壓縮至55天。日本則通過獨特的“雙軌制”監管框架,于2025-2026年推動全球首批iPSC療法逼近商業化落地。與美日相比,中國的“雙軌制”監管體系雖已成型,但在審評效率、實施細則以及供應鏈自主可控等方面仍需進一步完善。
據共研產業研究院預測,2026年中國干細胞藥物研發市場規模將達114.91億元,同比增長17.8%,商業化進程正全面提速。全球細胞療法市場預計在2032年將達到1135.3億美元,年復合增長率高達23.17%。
五、患者什么時候能用上?
從拿到生產許可證到藥品正式上市,中間還需要通過NDA(新藥上市申請)審批——這是一個藥品從“可以生產”到“可以銷售”的最終關口。以愛薩爾目前膝骨關節炎III期臨床試驗的推進速度來看,樂觀估計在2027年到2028年,這款產品有望獲批上市。
價格方面,短期內不要指望便宜。細胞藥物的生產成本極高——每一批次的干細胞注射液都需要從供者材料采集開始,經過嚴格的質量控制、低溫運輸、細胞擴增、成品檢測等一系列流程,且每一批次的產品都具有高度的個體化屬性或復雜的質控要求。類比已經上市的CAR-T細胞療法(價格普遍在百萬元級別),干細胞藥物雖然生產成本略低,但在上市初期,每針的價格大概率在數萬元到十幾萬元之間。醫保短期內不會覆蓋,這符合新藥上市的一般規律——先讓有剛性需求且支付能力較強的患者用上,再隨著工藝優化、規模化生產和競爭加劇,逐步降低價格、擴大可及性。
值得關注的是,愛薩爾的產品已經在海南博鰲樂城完成了首例合規收費的臨床轉化應用,說明在某些特殊政策區域,符合條件的患者已經可以提前使用。隨著更多產品獲批和更多地區的政策放開,干細胞藥物的可及性將逐步提高。

六、一點判斷
中國干細胞產業喊了十幾年“春天來了”,但春天一直沒有真正到來。以往每一次所謂的“政策利好”,帶來的往往是概念股的一時躁動和行業內的魚龍混雜——各種打著“干細胞治療”旗號的民營機構遍地開花,患者花了數十萬,打的卻可能是沒有經過嚴格質量控制的“不明液體”。
但2026年這個4月,情況可能真的不同了。2026年首張生產許可證的核發,加上即將正式實施的818號令,意味著干細胞終于有了一個清晰的“游戲規則”——不再是灰色地帶的野蠻生長,而是有法可依、有證可查、有責可追。 當然,從拿證到產品真正進醫院、進醫保,還有很長的路要走。但方向已經明確,路也鋪好了第一段。
接下來,我們關注兩件事:一是愛薩爾膝骨關節炎藥物的NDA審批結果何時落地;二是2026年的第二張、第三張干細胞生產許可證會發給誰,又有哪些適應癥的產品能夠走到終點。
這個賽道,終于開始變得有趣了。
七、常見問題解答(FAQ)
參考資料:(以上信息綜合自上海市藥監局公開信息、愛薩爾生物官網、證券時報、中國高新網、國家藥監局核查中心指南、共研產業研究院報告等。全國首張干細胞生產許可證于2024年由北京鉑生卓越獲得。)
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信