核心速覽:2025-2026年,干細胞治療神經系統疾病迎來關鍵進展。缺血性中風后遺癥:II期隨機對照試驗(NCT05292625,32例)顯示,臍帶間充質干細胞輸注后6個月,神經功能缺損評分(NIHSS)顯著改善(p=0.046),功能獨立性評分(FIM)及生活質量評分(SF-36)亦顯著提升(p=0.028,p<0.001)。帕金森病:兩項I/II期試驗同期發表于《Nature》——日本京都團隊(iPSC來源多巴胺能前體細胞,7例)24個月隨訪顯示移植細胞持續產生多巴胺,運動癥狀改善;美國紀念斯隆-凱特琳團隊(hESC來源,12例)18個月隨訪顯示耐受性良好,運動功能改善趨勢明確。脊髓損傷:中山大學附屬第三醫院完成全球首例iPSC來源脊髓神經前體細胞移植(54歲,頸髓損傷),移植后12天右下肢從肌力0級恢復至可屈伸活動。上述研究均未報告與治療相關的嚴重不良事件,安全性初步建立。
干細胞真的能讓受損的腦神經再生嗎?2025年臨床數據告訴了我們什么?
當身邊親近的人遭遇意外,導致大腦和神經嚴重受損時,康復之路往往充滿未知。與身體其他細胞不同,神經細胞的再生能力較弱。無論是中風、脊髓損傷,任何損傷都可能導致更持久、更嚴重的機能改變。
傳統療法通常只能緩解癥狀,但并不能幫助修復或自然愈合受損組織,而只是減輕炎癥、延緩病情發展。因此,患者會尋求更先進的輔助治療,例如干細胞療法。干細胞療法是一種再生醫學,目前正在研究其保護神經細胞、支持修復機制并最終實現再生的潛力。
其中,干細胞療法是研究最為深入的方法之一,其目標不僅在于控制癥狀,更在于修復或再生受損的神經組織。那么,這種療法的可行性究竟如何呢?請繼續閱讀。
為什么腦部和神經損傷難以修復
由大腦和脊髓組成的中樞神經系統(CNS)自我修復能力并不強。康復過程受諸多因素影響而變得復雜:
- 神經元或神經細胞幾乎無法再生。
- 傷口愈合后可能會形成疤痕組織,阻礙新組織的生長。
- 神經網絡非常專業化且相互關聯。
- 受傷后的炎癥可能會造成更大的傷害。
某些常與神經損傷相關的疾病包括:中風、脊髓損傷、帕金森病、阿爾茨海默病、周圍神經病變。
由于這些困難,科學家們正在研究干細胞,將其作為一種可能的手段來幫助或增強人體固有的有限修復機制。
干細胞如何幫助大腦修復?四種作用機制
患者常常誤以為干細胞療法是為了重建因疾病或紊亂而受損的整個大腦和神經系統,但事實并非如此。實際上,這項療法的主要突破在于其能夠支持和保護人體自然愈合機制。這幾年的臨床試驗,也讓我們看到了這背后的真實數據。
保護現有神經細胞
間充質干細胞(MSCs)實現這一目標的方式之一是分泌腦源性神經營養因子(BDNF)和其他神經營養因子。這些神經營養因子能夠維持現有神經元的存活,并保護神經元免受進一步損傷。
說個真實的研究吧。2025年11月發表于“Stem Cells Translational Medicine”的一項II期隨機對照試驗(NCT05292625)中,越南Vinmec醫院的研究團隊對32例缺血性中風后遺癥患者進行了臍帶間充質干細胞輸注治療[1]。

結果顯示,治療組在6個月隨訪時神經功能缺損評分(NIHSS)顯著改善(p=0.046),功能獨立性評分(FIM)和生活質量評分(SF-36)亦顯著提升(p=0.028,p<0.001),且未觀察到與治療相關的嚴重不良事件。
減輕炎癥的損害作用
中風、腦外傷和神經退行性疾病后,炎癥反應會顯著增強。干細胞療法被認為能夠調節炎癥信號,從而為組織修復和再生創造適宜的環境。
臨床數據支持:在脊髓損傷的臨床研究中,鞘內注射間充質干細胞后,患者腦脊液中的促炎因子(如TNF-α、IL-6)水平下降,抗炎因子(如IL-10)升高,這一免疫調節作用在多項I/II期臨床試驗中被觀察到。
增強細胞通信
已知大多數類型的干細胞主要通過旁分泌機制發揮作用。這意味著它們分泌有益物質,影響微環境中其他細胞的行為,從而激活修復通路并恢復組織完整性。
可能的神經分化
體外研究已證實,某些類型的干細胞能夠分化成神經元以及神經膠質細胞。然而,在人體內實現功能性整合仍然非常復雜,因此研究人員仍在探索這種可能性。
2025年4月,這個領域有兩個重磅消息。《自然》(Nature)雜志同期發表了兩項干細胞治療帕金森病的I/II期臨床試驗。
日本京都大學團隊(jRCT2090220384)將人誘導多能干細胞(iPSC)來源的多巴胺能前體細胞移植入7例帕金森病患者雙側大腦,24個月隨訪顯示,6例完成評估的患者中4例在未服藥狀態下運動癥狀減少,PET證實移植細胞持續產生多巴胺,未觀察到腫瘤形成或嚴重副作用[2]。

美國紀念斯隆-凱特琳癌癥中心團隊將人胚胎干細胞來源的多巴胺能前體細胞(bemdaneprocel)移植入12例患者雙側大腦殼核,18個月隨訪顯示細胞耐受性良好,未出現與治療相關的嚴重副作用,兩組患者均觀察到運動功能改善趨勢[3]。

這兩項研究告訴我們什么?細胞移植后能在人腦里存活,能干活,而且安全性比預想的要好。
目前正在研究哪些類型的干細胞對比?
以下是幾種正在研究的干細胞類型:
間充質干細胞(MSCs):具有強大的免疫調節和神經保護作用的細胞。
2025年7月,中國也啟動了一項針對急性缺血性卒中的IIa期臨床試驗(CTR20252683),用的是臍帶間充質干細胞,計劃招募60人,隨機雙盲安慰劑對照——這是目前證據等級最高的研究設計之一[4]。
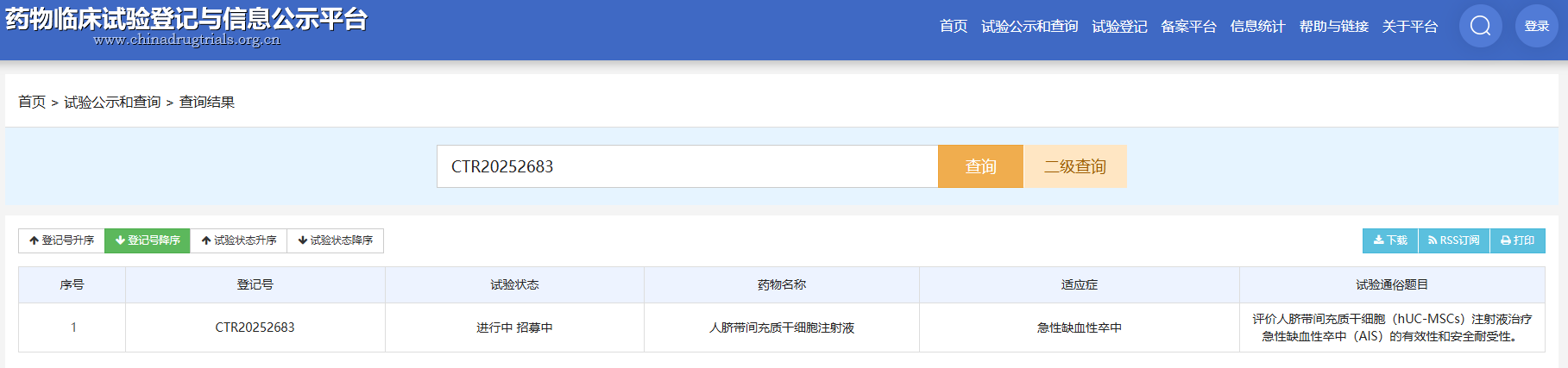
神經干細胞:具有分化成神經元潛能的細胞。
誘導多能干細胞(iPSCs):由成體細胞重新編程為多功能干細胞而形成的細胞。
2025年7月17日,中山大學附屬第三醫院完成了一件“全球首例”——他們給一位54歲的脊髓損傷患者移植了iPSC來源的脊髓神經前體細胞(XS228注射液)。這位患者是交通事故導致的頸髓損傷,治療前雙上肢肘以下完全沒勁(肌力0級)。移植后第12天,右下肢從完全不能動恢復到能屈伸活動,右手指能微微彎曲了,左下肢也恢復到了4-5級(正常人5級)。沒有不良反應,各項指標正常[5]。(來源:中山大學附屬第三醫院官網,2025年8月2日)
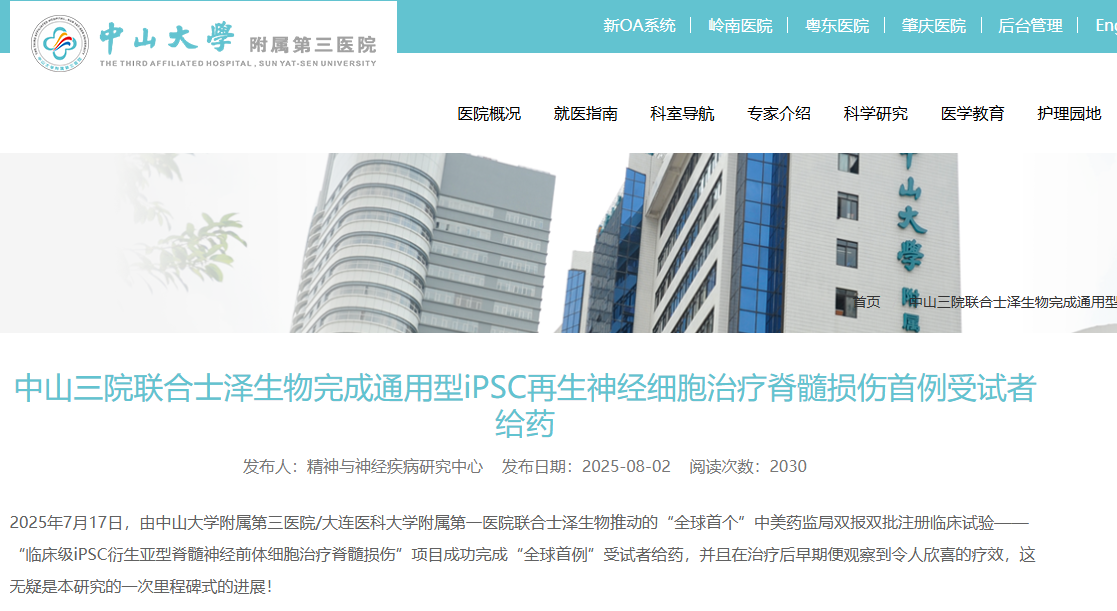
這是在中國的注冊臨床試驗(NMPA批件號:2025LP01101),中美雙報的那種。雖然目前只是一例個案,但對于脊髓損傷這個領域來說,意義不小。
不同品種各有其優點和科學難題。
| 細胞類型 | 來源 | 優勢 | 挑戰 | 代表研究 |
|---|---|---|---|---|
| 間充質干細胞(MSC) | 骨髓、臍帶、脂肪 | 免疫調節強、神經保護作用、倫理爭議小、可異體使用 | 分化能力有限 | 缺血性中風II期試驗(NCT05292625) |
| 神經干細胞 | 胎兒腦組織、iPSC分化 | 具有分化為神經元的潛能 | 來源受限、倫理爭議 | 臨床前及早期臨床階段 |
| 誘導多能干細胞(iPSC) | 成體細胞重編程 | 自體來源無免疫排斥;可無限擴增 | 致瘤風險、重編程效率 | 帕金森病(京都大學);脊髓損傷(中山三院) |
| 胚胎干細胞(hESC) | 胚胎內細胞團 | 全能性高、標準化生產 | 倫理爭議、免疫排斥 | 帕金森病(MSKCC) |
安全性與倫理考量
無論治療方法多么先進,安全性始終是決定所有治療方案成敗的關鍵因素。盡管初步結果令人鼓舞,但再生大腦和神經的療法仍處于起步階段,長期療效數據仍在積累中。
潛在風險可能包括:
- 免疫反應
- 感染
- 不受控制或異常的細胞生長
- 長期神經系統影響尚不明確
不過從目前已經公布的臨床數據來看,情況還算樂觀。 上面提到的幾項研究——越南的缺血性中風II期試驗(12個月隨訪)、日本的帕金森病移植(24個月隨訪)、美國的帕金森病移植(18個月隨訪)、中國的脊髓損傷首例移植(已平穩度過觀察期)——都沒有報告與治療相關的嚴重不良反應。
當然,長期的安全性,比如五年、十年后怎么樣,還需要繼續隨訪。
因此,除非在嚴格控制的醫療環境中進行,否則不應真正將治療視為一種選擇。這些醫療機構必須通過GMP認證進行加工,通過ISO認證的實驗室系統,確保無菌,以符合倫理的方式進行操作,有適當的文件記錄,并有適當的臨床監督。
綜合起來
干細胞療法是一種令人振奮的腦和神經組織再生新方法。2025年,我們確實看到了這個領域的進展——缺血性中風后遺癥有了II期RCT的證據支撐,帕金森病的細胞移植登上了《自然》,脊髓損傷完成了全球首例iPSC移植并觀察到了早期功能改善。大腦是有可能修復的,但我們對這一領域的理解仍在不斷發展之中。
任何計劃接受治療的患者都應通過專業醫療機構進行全面評估,并根據最新的科學發展情況獲得正確的指導。
常見問題解答(FAQ)
參考資料:
[1]:Liem Thanh Nguyen, Thuy Thi Ngoc Nguyen, Kien Trung Nguyen, Lam Nam Phung, Van Thanh Hoang, Trang Thi Kieu Phan, Minh Van Pham, Anh Thi Phuong Nguyen, Doan Van Ngo, Anh Van Nguyen, Chi Van Nguyen, Intrathecal versus intravenous umbilical cord mesenchymal stem cells for ischemic stroke sequelae, Stem Cells Translational Medicine, Volume 14, Issue 12, December 2025, szaf063, https://doi.org/10.1093/stcltm/szaf063
[2]:Sawamoto, N., Doi, D., Nakanishi, E. et al. Phase I/II trial of iPS-cell-derived dopaminergic cells for Parkinson’s disease. Nature 641, 971–977 (2025). https://doi.org/10.1038/s41586-025-08700-0
[3]:Tabar, V., Sarva, H., Lozano, A.M. et al. Phase I trial of hES cell-derived dopaminergic neurons for Parkinson’s disease. Nature 641, 978–983 (2025). https://doi.org/10.1038/s41586-025-08845-y
[4]:https://www.chinadrugtrials.org.cn/clinicaltrials.searchlist.dhtml?keywords=CTR20252683
[5]:https://zssy.com.cn/article/28760
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。部分內容由AI輔助潤色生成,并經人工審核整理。



 掃碼添加官方微信
掃碼添加官方微信