肝移植仍受供體器官短缺和手術(shù)本身風(fēng)險(xiǎn)的限制,這凸顯了開發(fā)新型肝硬化療法的迫切需求。本研究開發(fā)了一種將人原代肝細(xì)胞轉(zhuǎn)化為可擴(kuò)增的肝細(xì)胞衍生肝祖細(xì)胞樣細(xì)胞(HepLPCs)的方案,這些細(xì)胞能夠分泌高水平的基質(zhì)金屬蛋白酶和肝細(xì)胞生長因子。
上海仁濟(jì)醫(yī)院牽頭研究:肝祖細(xì)胞治療肝硬化6個(gè)月后,8例患者肝功能、凝血及纖維化指標(biāo)顯著改善
近日,上海交通大學(xué)醫(yī)學(xué)院附屬仁濟(jì)醫(yī)院的多個(gè)科室聯(lián)合中國上海海軍軍醫(yī)大學(xué)東方肝膽外科醫(yī)院臨床檢驗(yàn)科、德國漢諾威醫(yī)學(xué)院等研究機(jī)構(gòu)在《Cell Discovery》上發(fā)表了一項(xiàng)肝祖細(xì)胞治療針對(duì)9名肝硬化患者的首次人體臨床試驗(yàn)結(jié)果[1]。

研究結(jié)果表明,經(jīng)肝動(dòng)脈輸注HepLPCs安全可行,且在6個(gè)月隨訪期內(nèi),8名完成隨訪的患者在肝臟生化、凝血功能及門靜脈高壓等多個(gè)關(guān)鍵指標(biāo)上表現(xiàn)出顯著改善,為肝硬化治療提供了一種極具前景的新策略。
一、引言:肝硬化的治療挑戰(zhàn)與細(xì)胞治療新方向
肝硬化是一種嚴(yán)重的慢性肝臟疾病,其特征是肝臟進(jìn)行性瘢痕形成和功能損害,最終導(dǎo)致代謝、解毒及合成等關(guān)鍵功能的喪失。常見病因包括病毒性肝炎、酒精中毒及非酒精性脂肪肝等。肝移植雖是根治手段,卻面臨供體短缺、手術(shù)風(fēng)險(xiǎn)高和免疫排斥等挑戰(zhàn),使得開發(fā)替代療法成為當(dāng)務(wù)之急。
細(xì)胞移植是近年來備受關(guān)注的新策略。其中,胎肝細(xì)胞移植雖顯示出潛力,但受限于倫理與實(shí)際操作問題。近期研究表明,通過化學(xué)重編程可將成熟肝細(xì)胞轉(zhuǎn)化為增殖性肝祖細(xì)胞樣細(xì)胞(HepLPCs),這些細(xì)胞與胎肝細(xì)胞具有相似的基因表達(dá)譜,在促進(jìn)肝臟再生方面展現(xiàn)前景,但其對(duì)肝硬化的具體治療效果仍需深入驗(yàn)證。
為此,本研究成功通過化學(xué)重編程將人原代肝細(xì)胞轉(zhuǎn)化為可擴(kuò)增的肝祖細(xì)胞(HepLPCs)。在培養(yǎng)過程中,這些細(xì)胞能夠分泌促進(jìn)肝臟再生并抑制纖維化的因子;在肝硬化大鼠模型中,HepLPCs展現(xiàn)出明顯的抗纖維化作用與再生潛力。
毒理學(xué)風(fēng)險(xiǎn)評(píng)估完成后,一項(xiàng)納入9名肝硬化患者的臨床研究進(jìn)一步驗(yàn)證了HepLPCs在治療肝硬化方面的安全性及潛在療效。臨床前及臨床研究的綜合數(shù)據(jù)共同表明,HepLPCs具備良好的安全性及治療前景,因此有望為解決肝硬化患者尚未滿足的臨床需求提供潛在突破。
二、如何生產(chǎn)出符合良好生產(chǎn)規(guī)范(GMP)和質(zhì)量保證的HepLPC?
為確保臨床應(yīng)用的安全性與一致性,本研究在良好生產(chǎn)規(guī)范(GMP)條件下生產(chǎn)HepLPCs(圖1)。

標(biāo)準(zhǔn)化的培養(yǎng)體系:使用人原代肝細(xì)胞作為起始材料,在成分明確的無動(dòng)物源性培養(yǎng)基中進(jìn)行化學(xué)重編程,確保了生產(chǎn)過程的標(biāo)準(zhǔn)化。
全過程質(zhì)量控制:建立了雙層細(xì)胞庫系統(tǒng),并制定了嚴(yán)格的放行標(biāo)準(zhǔn),對(duì)細(xì)胞進(jìn)行特性、無菌性和安全性評(píng)估,保證最終產(chǎn)品符合預(yù)定義規(guī)格。
細(xì)胞特性與安全性驗(yàn)證:核型分析和全基因組測(cè)序證實(shí)了細(xì)胞的基因組穩(wěn)定性。流式細(xì)胞術(shù)分析顯示,HepLPCs同時(shí)表達(dá)肝臟特異性基因與干細(xì)胞/祖細(xì)胞基因,且不表達(dá)MHC II類抗原,具備低免疫原性。
功能效力確認(rèn):轉(zhuǎn)錄組學(xué)與功能實(shí)驗(yàn)證實(shí),HepLPCs能高效分泌肝細(xì)胞生長因子(HGF)和基質(zhì)金屬蛋白酶(MMPs),在功能層面具備促進(jìn)肝臟再生與抑制纖維化的雙重潛力。
三、臨床前研究:HepLPCs在大鼠模型中證實(shí)其療效與安全性
治療效果方面,在由硫代乙酰胺誘導(dǎo)的晚期肝硬化大鼠模型中,經(jīng)門靜脈移植人源HepLPCs顯示出顯著的治療益處。與陰性對(duì)照組相比,HepLPCs治療組大鼠的肝臟纖維化程度得到明顯改善,具體表現(xiàn)為細(xì)胞外基質(zhì)的主要成分(如膠原蛋白Col1a1和纖連蛋白)的積累顯著減少。這些免疫組化結(jié)果直接證實(shí)了HepLPCs具備減輕乃至逆轉(zhuǎn)肝纖維化的強(qiáng)大潛力(圖2)。

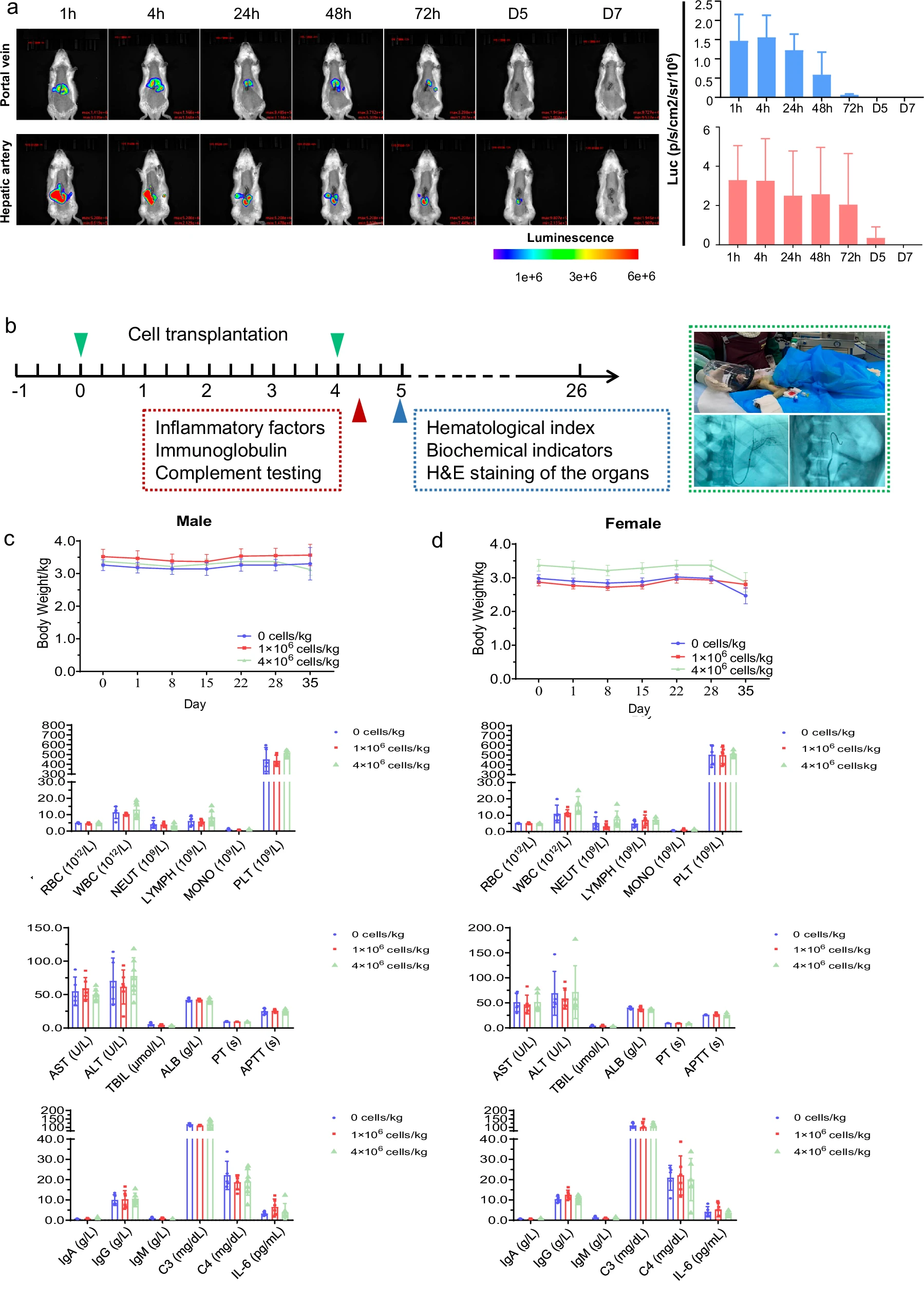
安全性與作用機(jī)制方面,整個(gè)實(shí)驗(yàn)過程中所有大鼠體重穩(wěn)定且無死亡,證明了治療的安全性。值得注意的是,得益于HepLPCs本身低免疫原性的特性,移植過程無需使用免疫抑制劑。盡管血清ALT和AST水平的變化未達(dá)統(tǒng)計(jì)學(xué)意義,但其下降趨勢(shì)仍提示肝損傷有所改善。這些綜合結(jié)果有力地支持了HepLPCs移植作為一種安全且有效的策略,也為后續(xù)臨床研究提供了有力的可行性依據(jù)(圖3)。
四、臨床研究:HepLPC治療肝硬化患者的可行性和安全性
首先,在成功建立符合GMP規(guī)范的生產(chǎn)流程并證實(shí)其臨床前療效的基礎(chǔ)上,研究人員啟動(dòng)了一項(xiàng)針對(duì)肝硬化患者的單臂、開放標(biāo)簽臨床試驗(yàn),旨在評(píng)估HepLPCs療法在人體內(nèi)的可行性與安全性。
該研究在2021年12月27日至2022年12月14日期間,共招募并篩選了14例病因各異的肝硬化患者。其中9例患者接受了經(jīng)肝動(dòng)脈輸注HepLPCs的治療,劑量遞增:低劑量組(0.3–0.4×10?/kg)、中劑量組(1.5–2.0×10?/kg)和高劑量組(3.0–4.0×10?/kg)(圖4、5a)。
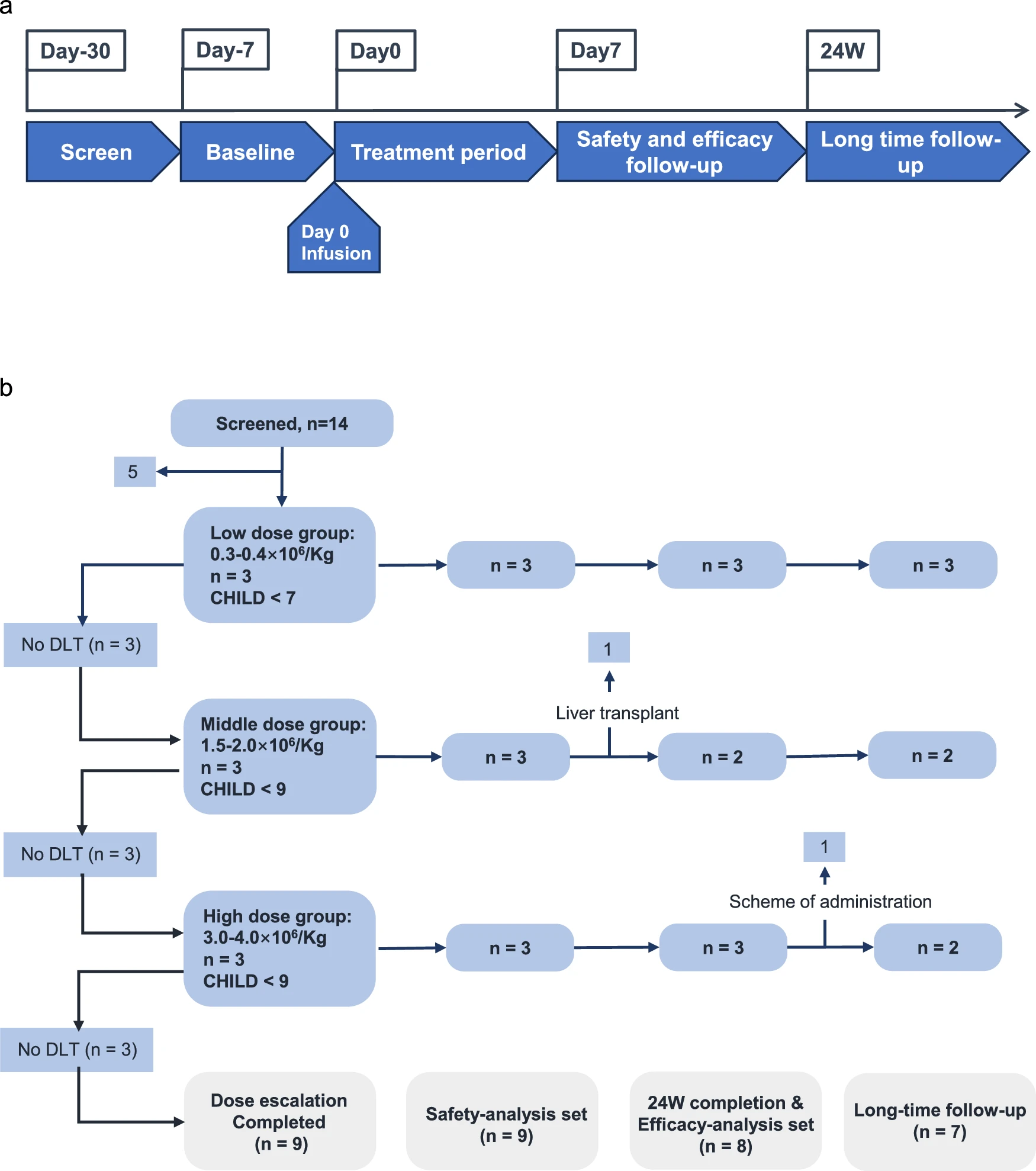
a.根據(jù)修改后的方案繪制的研究設(shè)計(jì)示意圖。b.患者處置和分配到隊(duì)列及分析集的示意圖。
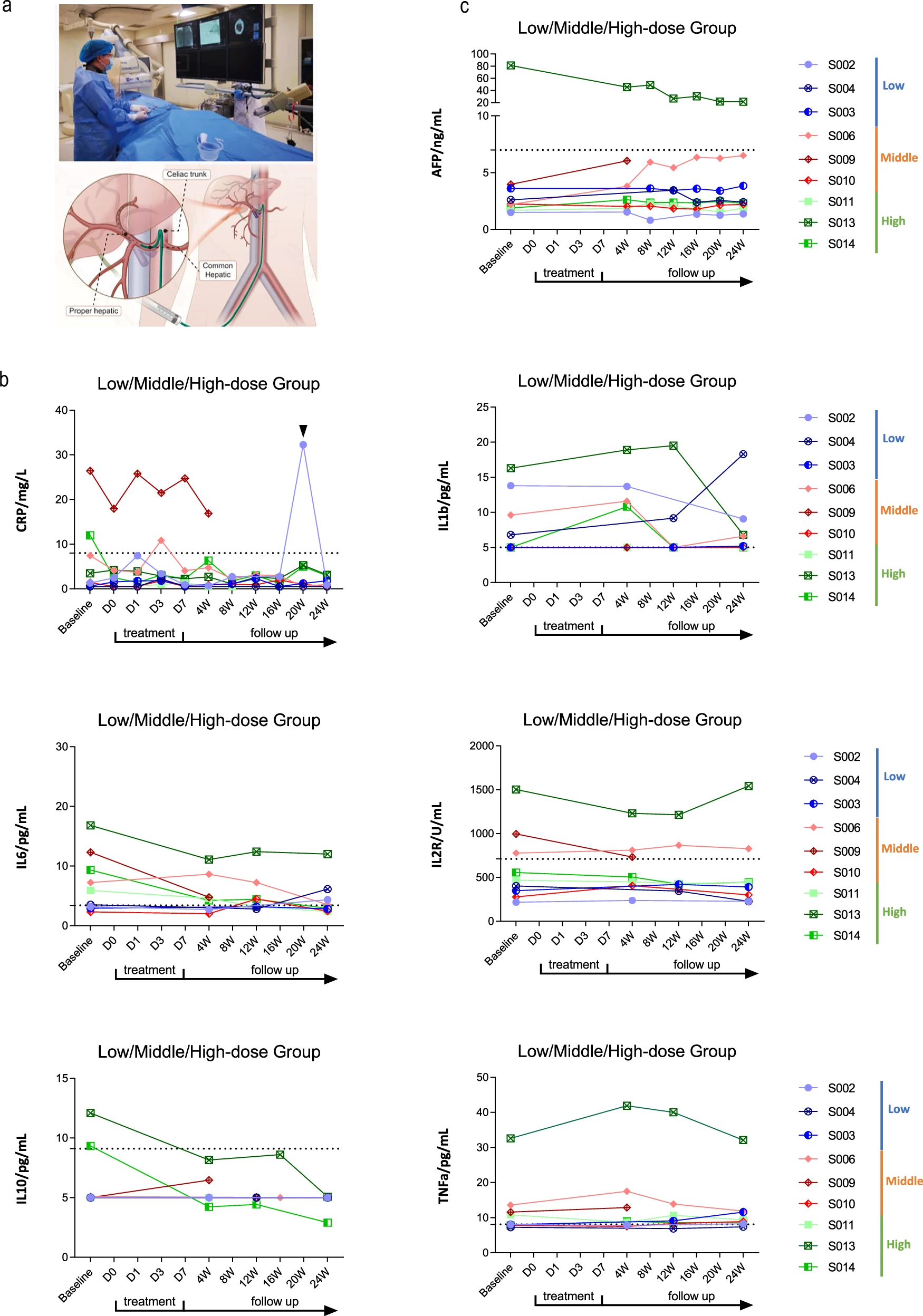
a.HepLPC輸注途徑示意圖。b.HepLPC治療患者血清中CRP、IL-1β、IL-2R、IL-6、IL-10和TNF-α水平。2號(hào)患者出現(xiàn)流感樣癥狀,并伴有短暫的CRP水平升高。虛線代表正常值。c.HepLPC治療前后AFP水平的評(píng)估。
在整個(gè)治療過程中,得益于臨床前研究已證實(shí)的HepLPCs低免疫原性特性,所有接受治療的患者均未使用免疫抑制劑,且未觀察到任何免疫排斥或炎癥反應(yīng)。尤為重要的是,治療期間所有患者均未出現(xiàn)急性輸血反應(yīng)或劑量限制性毒性,初步證明了該療法在肝硬化患者中應(yīng)用的良好安全性與耐受性。
HepLPCs治療肝硬化卓越的安全性
HepLPCs治療展現(xiàn)出卓越的安全性,主要體現(xiàn)在三個(gè)方面:
1. 嚴(yán)重不良事件與治療無關(guān),且治療前期已顯現(xiàn)安全性信號(hào):研究中唯一一例嚴(yán)重不良事件(急性膽囊炎導(dǎo)致的肝移植)被證實(shí)與HepLPC治療本身無關(guān)。
這一判斷的關(guān)鍵依據(jù)在于:輸注的細(xì)胞在體內(nèi)存留時(shí)間短暫,且在該事件發(fā)生前(治療后1個(gè)月),該患者的多項(xiàng)關(guān)鍵肝功能指標(biāo)(如血氨、凝血功能、前白蛋白等)已顯示出改善趨勢(shì)。這一方面排除了治療的直接責(zé)任,另一方面反而凸顯了細(xì)胞輸注初期的良好耐受性和潛在益處,強(qiáng)化了其安全性 。
2. 不良事件輕微可控,且未引發(fā)免疫或炎癥風(fēng)暴:研究期間記錄的其他不良事件(如便秘、瘙癢等)均為常見臨床癥狀,被評(píng)估與HepLPC或其輸注方式無關(guān),且患者耐受良好。
更重要的是,通過對(duì)血清細(xì)胞因子(包括CRP、IL-6等)的密切監(jiān)測(cè),證實(shí)所有患者均未發(fā)生細(xì)胞因子釋放綜合征等嚴(yán)重的免疫炎癥反應(yīng)。多數(shù)患者IL-6水平在治療后甚至有所下降,這從免疫學(xué)角度提供了強(qiáng)有力的證據(jù),表明該療法即使在不使用免疫抑制劑的情況下,也具有卓越的免疫兼容性和炎癥安全性。
3. 無血液學(xué)毒性或腫瘤發(fā)生風(fēng)險(xiǎn),顯示出長期的生物安全性:治療未導(dǎo)致血細(xì)胞下降,反而改善了貧血狀況。全程監(jiān)測(cè)未發(fā)現(xiàn)甲胎蛋白(AFP)水平升高或肝臟腫瘤跡象,排除了長期風(fēng)險(xiǎn)。
顯著的治療效果:肝功能、凝血、纖維化及影像學(xué)改善
1. 肝功能與合成功能顯著改善:治療后,患者的整體肝功能得到有效恢復(fù)。具體表現(xiàn)為:37.5%(3/8)的患者終末期肝病模型(MELD)和Child-Pugh評(píng)分下降,其中一名重癥患者甚至因此從肝移植等待名單中被移除。更為普遍的是,75%(6/8)的患者血清白蛋白(ALB)和前白蛋白(pre-ALB)水平升高,直接證明了肝臟合成蛋白質(zhì)的功能增強(qiáng)。同時(shí),所有患者的血清氨水平均持續(xù)改善,表明肝臟的解毒能力也得到了有效恢復(fù)(圖6)。
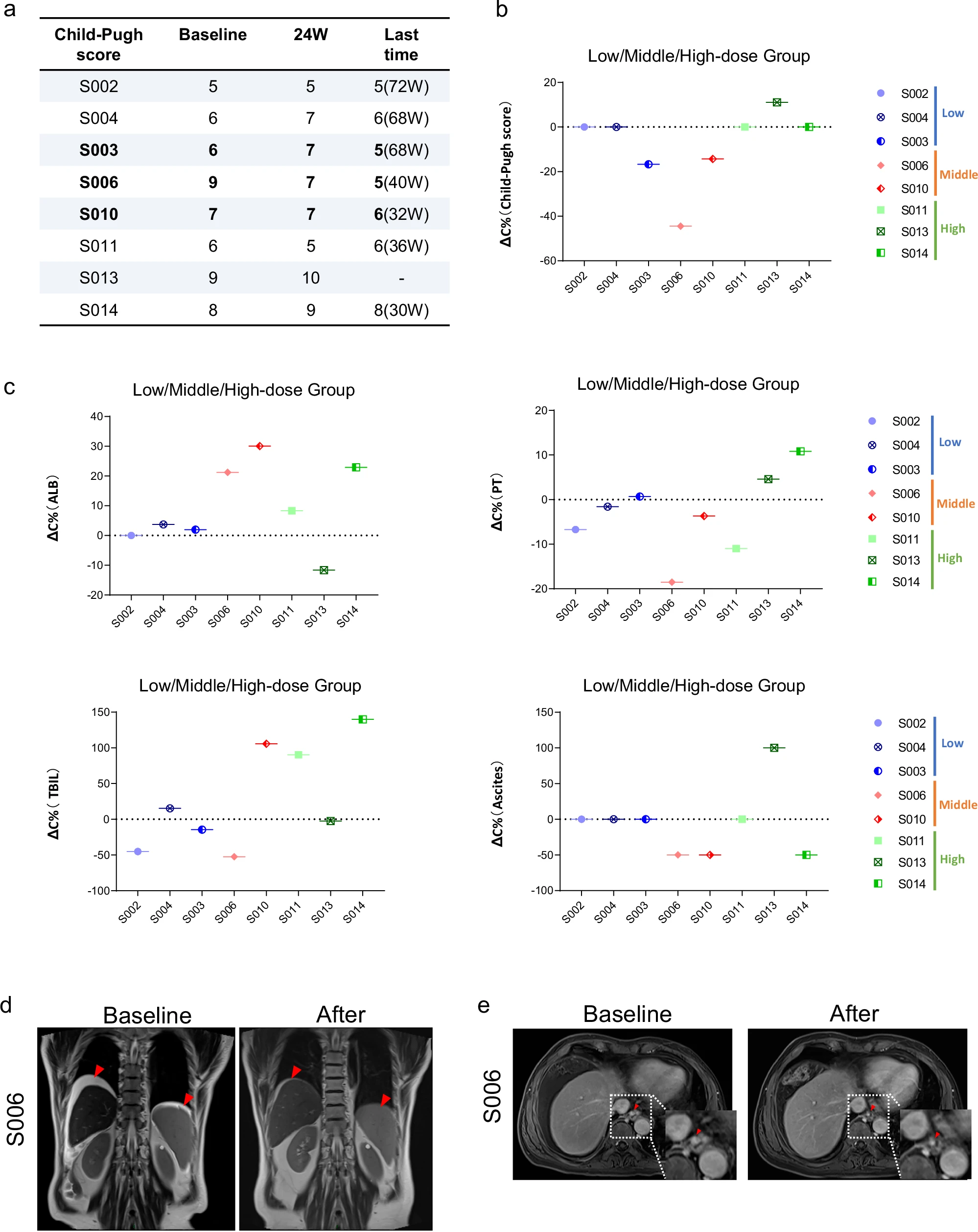
a.HepLPC治療前后Child-Pugh評(píng)分的評(píng)估。
b?、c?.?HepLPC治療患者的Child-Pugh評(píng)分、白蛋白(ALB)、凝血酶原時(shí)間(PT)、總膽紅素(TB)和腹水程度的變化。
d.6號(hào)患者HepLPC治療前后的腹水情況。e.6號(hào)患者食管下端靜脈曲張血管直徑的變化。紅色方框內(nèi)顯示的是肝硬化改善的指標(biāo)。
2. 凝血功能全面恢復(fù):評(píng)估凝血功能的多個(gè)關(guān)鍵參數(shù)均顯示出積極變化。其中,62.5%(5/8)患者的凝血酶原時(shí)間(PT)縮短,而87.5%(7/8)患者的活化部分凝血活酶時(shí)間(APTT)下降,這表明機(jī)體的凝血機(jī)制趨于正常。此外,62.5%(5/8)患者的纖維蛋白原水平顯著升高,進(jìn)一步印證了肝臟合成凝血因子的能力在治療后得到了有效增強(qiáng)。
3. 肝纖維化與硬度呈現(xiàn)逆轉(zhuǎn)趨勢(shì):通過直接和間接的測(cè)量方法,均觀察到肝纖維化的緩解。在影像學(xué)上,50%(4/8)的患者通過彈性成像檢測(cè)的肝臟硬度值(LSM)出現(xiàn)下降。在血清學(xué)指標(biāo)上,尤其是低劑量組的輕度肝硬化患者,其透明質(zhì)酸(HA)等肝纖維化標(biāo)志物水平顯著且持續(xù)降低。這些數(shù)據(jù)共同表明,HepLPC治療對(duì)逆轉(zhuǎn)肝臟的纖維化病理改變具有積極影響。
4. 門靜脈高壓顯著緩解與肝臟再生跡象:影像學(xué)檢查(如彈性成像和磁共振)提供了治療有效的有力結(jié)構(gòu)證據(jù)。75%(6/8)的患者觀察到脾臟體積縮小,這是門靜脈高壓得到改善的直接標(biāo)志。尤為重要的是,有患者的下段食管靜脈曲張血管直徑減小,證實(shí)了門體分流的減少。此外,同樣有75%(6/8)的患者肝臟體積出現(xiàn)增大,這強(qiáng)烈提示肝細(xì)胞可能發(fā)生了增殖,為HepLPs能夠促進(jìn)肝臟再生提供了關(guān)鍵的臨床證據(jù)。
討論與結(jié)論
低免疫原性賦予HepLPCs優(yōu)異的安全性:本研究證實(shí),HepLPCs在臨床應(yīng)用中具備出色的安全性。其所采用的細(xì)胞劑量與既往肝干細(xì)胞及間充質(zhì)干細(xì)胞治療研究相當(dāng),但在整個(gè)劑量范圍內(nèi)均未出現(xiàn)治療相關(guān)不良事件或免疫毒性跡象。特別值得關(guān)注的是,在未使用免疫抑制劑的情況下,所有患者均未出現(xiàn)轉(zhuǎn)氨酶或炎癥細(xì)胞因子水平升高,這直接驗(yàn)證了臨床前研究所揭示的低免疫原性特征——HepLPCs不表達(dá)MHC II類抗原,并可抑制T細(xì)胞增殖與促炎因子表達(dá),從而實(shí)現(xiàn)了無需免疫抑制支持的安全應(yīng)用。
肝動(dòng)脈輸注途徑具備高安全性與細(xì)胞植入效率:在給藥途徑方面,本研究采用的經(jīng)肝動(dòng)脈輸注展現(xiàn)出明顯優(yōu)勢(shì)。相較于脾內(nèi)移植或門靜脈輸注等傳統(tǒng)方式,肝動(dòng)脈途徑具有血流速度快、血栓風(fēng)險(xiǎn)低、不受門靜脈高壓影響等特點(diǎn),并能提供更高的細(xì)胞植入效率與持久性。臨床結(jié)果進(jìn)一步證實(shí)了該途徑的可靠性,研究期間所有患者均未發(fā)生出血或血栓事件,為此輸注方式的未來應(yīng)用提供了有力的安全性依據(jù)。
肝功能改善提示旁分泌機(jī)制主導(dǎo)治療效應(yīng):盡管在組織學(xué)層面尚未觀察到肝硬化逆轉(zhuǎn)的直接證據(jù),但HepLPC治療確實(shí)帶來了多項(xiàng)關(guān)鍵肝功能指標(biāo)的顯著改善。患者的前白蛋白、凝血功能等合成指標(biāo)迅速提升,解毒能力增強(qiáng),門靜脈高壓相關(guān)臨床表現(xiàn)(如脾腫大、腹水)也得到緩解。尤為重要的是,這些療效在患者體內(nèi)已檢測(cè)不到供體細(xì)胞的情況下依然持續(xù)存在,強(qiáng)烈提示HepLPCs主要通過旁分泌機(jī)制發(fā)揮作用,即通過分泌活性因子促進(jìn)宿主自身肝臟的再生與修復(fù),從而實(shí)現(xiàn)疾病修飾效應(yīng)。
總之,我們的研究表明,經(jīng)肝動(dòng)脈輸注肝硬化患者肝臟來源的肝細(xì)胞(HepLPCs)安全、可行,且可能有效治療肝硬化。這種新型治療方法在肝硬化的臨床治療中具有巨大的應(yīng)用前景。
令人鼓舞的結(jié)果為推進(jìn)下一階段的臨床試驗(yàn)提供了強(qiáng)有力的理論依據(jù),并有望將該療法的應(yīng)用范圍從肝硬化擴(kuò)展到急性加重型慢性肝衰竭。
參考資料:
[1]He, K., Zhu, XJ., Shi, YP. et al. Treatment of liver cirrhosis using hepatocyte-derived liver progenitor-like cells: a prospective, open-label, single-arm, safety trial. Cell Discov 11, 88 (2025). https://doi.org/10.1038/s41421-025-00831-y
免責(zé)說明:本文僅用于傳播科普知識(shí),分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請(qǐng)隨時(shí)聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信