Meta描述:躍賽生物UX-GIP001獲中美雙批臨床試驗,成為全球首款iPSC來源治療難治性癲癇的通用型細胞療法。動物實驗顯示癲癇波消失率達90%。解讀技術原理、臨床前數據與監管意義。
全球首款!躍賽生物iPSC來源癲癇細胞療法UX-GIP001獲中美雙批臨床試驗
核心速覽
| 項目 | 關鍵信息 |
|---|---|
| 產品名稱 | UX-GIP001注射液 |
| 研發企業 | 上海躍賽生物科技有限公司(UniXell Biotechnology) |
| 細胞類型 | iPSC來源的GABA能神經祖細胞 |
| 適應癥 | 藥物難治性癲癇(尤其是內側顳葉癲癇MTLE) |
| FDA批準 | 2026年3月12日 |
| CDE批準 | 2026年4月8日 |
| 全球地位 | 首款同時在中美獲批臨床的iPSC來源癲癇細胞療法 |
| 技術原理 | 移植后分化為GABA能中間神經元,修復興奮-抑制失衡 |
| 臨床前數據 | 動物實驗中,約90%癲癇相關腦活動消失,8個月后癲癇波幾乎檢測不到 |
| 研發階段 | I期臨床試驗即將啟動 |
| 上市預期 | 5-8年(若I-III期順利) |
一、全球7000萬患者的希望:難治性癲癇的新解法
全球約有7000萬癲癇患者,其中大約30%——也就是超過2000萬人——對現有的抗癲癇藥物沒有反應。這種情況被稱為藥物難治性癲癇。
在成人中,最常見的局灶性癲癇類型是內側顳葉癲癇(MTLE),約占70%。它的典型病理特征是海馬硬化——海馬區的神經元大量丟失,膠質細胞增生,導致腦內興奮-抑制嚴重失衡。簡單說就是“油門太猛,剎車太軟”。
現有治療手段都有各自的短板:
- 藥物:對30%的患者無效,而且長期服用有認知障礙、骨質疏松等副作用
- 手術:切除癲癇灶,但創傷大,可能損傷記憶功能
- 神經刺激:效果有限,需要植入設備
所以,科學家一直在尋找一種能從根源上修復神經網絡的方法——不是“控制發作”,而是“修復大腦”。
二、里程碑事件:全球首款中美雙批的iPSC癲癇細胞療法
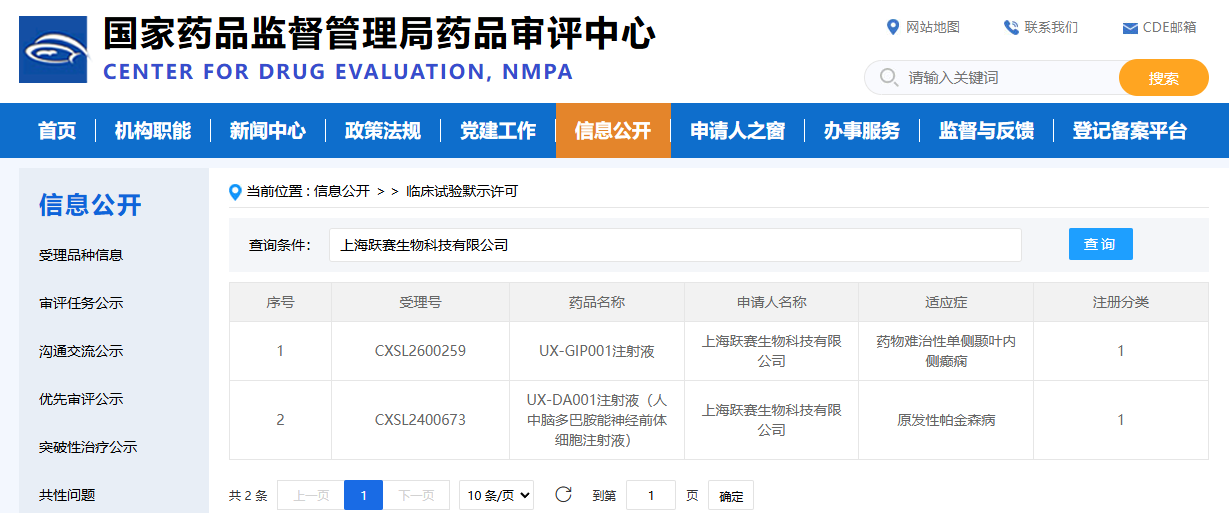
2026年4月8日,上海躍賽生物科技有限公司宣布,其自主研發的UX-GIP001注射液獲得中國國家藥監局藥品審評中心(CDE)臨床試驗默示許可。
就在不到一個月前(3月12日),該藥已經獲得美國FDA的臨床試驗批準。
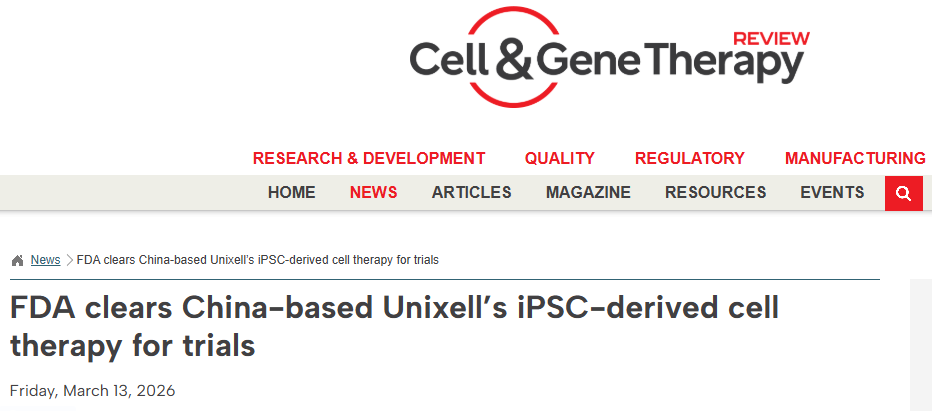
至此,UX-GIP001成為全球首款同時在中美兩國獲批進入臨床試驗的iPSC來源、用于治療藥物難治性癲癇的通用型細胞療法。
這標志著中國在干細胞治療難治性癲癇領域,已經從“跟跑”進入了“領跑”行列。
三、技術原理:用“剎車細胞”修復失衡的大腦
UX-GIP001的核心技術是:用人類誘導多能干細胞(iPSC)定向分化制備GABA能神經祖細胞。
GABA(γ-氨基丁酸)是大腦中最重要的抑制性神經遞質——它就像汽車的剎車。癲癇的本質,就是大腦的“油門”(興奮性神經元)太強,“剎車”(GABA能中間神經元)太弱。
躍賽生物的做法是:
- 在體外用iPSC大規模生產GABA能神經祖細胞
- 把這些細胞移植到患者的海馬區
- 細胞在體內成熟為功能性GABA能中間神經元
- 它們與宿主神經元建立突觸連接,修復失衡的興奮-抑制網絡
- 從而抑制癲癇異常放電,同時保留海馬的正常功能
最關鍵的一點:這不是“控制癥狀”,而是“修復神經回路”——屬于疾病修復性療法(Disease-modifying therapy),有可能從根源上治療MTLE。
而且,該產品采用異體通用型設計,不需要從患者自身取材,可以實現規模化生產,降低成本。
四、臨床前數據:90%癲癇波消失
動物實驗的數據相當亮眼:
- 干細胞植入小鼠約6個月后,約90%?的癲癇相關腦活動消失
- 8個月后,癲癇波幾乎檢測不到
這些數據表明,移植的GABA能神經祖細胞不僅存活了,還成功整合進了宿主神經網絡,并且長期發揮抑制作用。
臨床前研究已經充分驗證了安全性和有效性,這也是中美兩國藥監機構敢于批準進入人體試驗的基礎。
五、研發進度:接下來會發生什么?
5.1 I期臨床試驗(即將啟動)
I期試驗的主要目標是評估安全性、耐受性和初步療效。將在中美兩國同步或分別開展。入組患者通常是藥物難治性癲癇患者,對現有治療反應不佳。
5.2 后續時間線
如果I期結果積極,后續需要推進II期(擴大樣本,評估療效)和III期(多中心,隨機雙盲對照)試驗。
從I期到上市,通常需要5-8年。當然,如果數據特別突出,可能會獲得突破性療法認定或優先審評,加速上市。
六、研發主體:躍賽生物是誰?
躍賽生物由中國科學院腦科學與智能技術卓越創新中心高級研究員陳躍軍博士于2021年創立,總部位于上海張江。
2025年2月,公司完成了1.4億元人民幣(約2050萬美元)的A+輪融資,投資方包括高瓴創投、天士力、浦東創投等知名機構。
公司在上海自貿試驗區設有4000平方米的研發中心及GMP級生產設施。
值得注意的是,躍賽生物還有另一款iPSC衍生細胞療法(用于治療帕金森病),已于2025年啟動I期臨床。這說明其iPSC分化技術平臺具有強大的拓展性——可以針對不同疾病生產不同類型的神經細胞。
七、監管意義:為什么“中美雙批”很重要?
同時獲得FDA和NMPA的臨床試驗批準,意味著什么?
第一,科學性和創新性得到全球最嚴格審評體系的認可。 美國FDA和中國CDE對細胞治療產品的審評標準都非常嚴格,能同時通過,說明產品的臨床前數據扎實、生產工藝可控、安全性風險可控。
第二,中國CDE通過“創新藥30日審批通道”快速獲批,體現了國家對具有臨床價值的創新療法的優先支持。
第三,中美雙批可以實現全球同步臨床研發,加速上市進程,也為中國創新藥“出海”提供了成功范例。

八、展望與挑戰
UX-GIP001為全球數千萬難治性癲癇患者帶來了從“控制發作”到“修復大腦”的曙光。
但我們也必須清醒地看到,細胞療法仍然面臨一些挑戰:
- 長期安全性:致瘤風險(iPSC來源細胞的殘留未分化細胞)、免疫排斥(異體細胞)
- 手術移植風險:細胞需要直接注射到海馬區,屬于侵入性操作
- 可及性和定價:細胞藥物的生產成本高,未來上市后的價格和醫保覆蓋是實際問題
盡管如此,這一里程碑事件的意義不可否認——它標志著中國在干細胞治療領域,已經從“跟跑”進入了“領跑”行列。
九、常見問題解答(FAQ)
參考資料
- 躍賽生物官方公告(2026年4月8日)
- 中國國家藥監局藥品審評中心(CDE)公開信息
- FDA臨床試驗批準信息(2026年3月12日)
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信