概述:自身免疫性風濕病(AIRDs)的治療正經歷從“長期免疫抑制”向“持續緩解乃至治愈”的范式轉移。2026年4月,發表于《臨床風濕病學》(Clinical Rheumatology)的最新綜述指出[1]:MSC、Treg、CAR-T 及外泌體療法正成為精準管理炎癥性疾病的新前沿。本文將結合2026年初發布的CASTLE等核心臨床試驗,深度解析這一領域的革命性進展。
重塑免疫平衡:MSC、Treg、CAR-T及外泌體在治療自身免疫性風濕病中的最新臨床突破

核心速覽
| 療法類型 | 核心機制 | 關鍵臨床數據 | 主要挑戰 |
|---|---|---|---|
| 間充質干細胞(MSC) | 旁分泌+細胞接觸,免疫調節、組織修復 | 42項RCT薈萃分析:SLE患者SLEDAI顯著改善;RA總有效率54%;聯合IFN-γ使ACR20達93.3% | 來源、劑量、方案標準化 |
| 調節性T細胞(Treg) | 恢復免疫耐受,抑制自身反應T細胞 | CHILL I/II期試驗(QEL-005 CAR-Treg)啟動;IL-2mutein IIa期進行中 | 成本高、體外擴增難、致癌風險 |
| CAR-T細胞 | 基因改造T細胞清除致病B細胞 | CASTLE試驗(Nature Med,2026):24例難治性SLE/SSc/IIM,91.7%達療效終點,無藥緩解;relma-cel I期:8例SLE均達SRI-4 | CRS、神經毒性、B細胞長期耗竭、成本 |
| 外泌體(無細胞) | 攜帶miRNA/蛋白,免疫調節、組織修復 | 臨床前RA/SLE模型有效;MESAE試驗(NCT07131683)探索鼻內給藥 | 標準化分離、規模化生產、長期安全性 |
一、為什么自身免疫性風濕病需要細胞免疫療法?
類風濕關節炎(RA)、系統性紅斑狼瘡(SLE)、幼年特發性關節炎(JIA)、銀屑病關節炎(PsA)、強直性脊柱炎(AS)等自身免疫性風濕病(AIRDs),其核心病理是免疫系統攻擊自身組織,導致慢性炎癥和組織損傷。

傳統治療從非甾體抗炎藥到改善病情抗風濕藥(DMARDs),再到生物制劑和靶向合成DMARDs,雖然取得了長足進步,但仍有相當比例的患者面臨三大困境:
- 疾病控制不佳(部分患者原發無效)
- 無法耐受不良反應
- 無法實現停藥緩解
細胞免疫療法的目標不再是“壓制”免疫系統,而是重建免疫平衡——恢復疾病發生前的生理狀態,甚至實現治愈。間充質干細胞(MSC)、調節性T細胞(Treg)、嵌合抗原受體T細胞(CAR-T)以及外泌體,正成為這場范式轉變的核心力量。
核心特性與總體免疫調節框架
間充質干細胞(MSC)治療自身免疫性疾病的核心在于其強大的免疫調節、組織修復與再生能力。MSC通過旁分泌信號和直接的細胞間相互作用,能夠系統性地減輕炎癥,而非單純抑制免疫。其作用覆蓋固有免疫與適應性免疫,并通過復雜的分泌組、細胞外囊泡以及代謝-表觀遺傳重編程,從多個維度重建免疫耐受,為治療難治性自身免疫病提供了創新策略。
對固有免疫細胞的調控
MSC可顯著影響樹突狀細胞(DC)、巨噬細胞和自然殺傷(NK)細胞。它們通過下調MHC II、CD80/CD86和IL-12抑制DC的分化與成熟,并誘導耐受性DC表型,從而促進調節性T細胞(Treg)擴增。MSC還能增加IL-10、TGF-β、PGE2和IDO活性,將巨噬細胞從促炎的M1型轉變為抗炎修復的M2型,同時下調TNFα、IL-1β和IL-6。此外,通過PGE2、TGF-β、HLA-G及細胞接觸,MSC抑制NK細胞的增殖、細胞毒性和IFN-γ產生,從而減弱驅動自身免疫的早期先天反應。
對適應性免疫(T細胞與B細胞)的調節
在適應性免疫方面,MSC通過IDO、一氧化氮、PGE2、TGF-β及PD-L1/PD-1通路,抑制CD4?和CD8?T細胞增殖,降低Th1/Th17反應;同時促進FoxP3?Treg和Tr1細胞的擴增與功能穩定,恢復外周耐受,減少自身反應性T細胞活性。對于B細胞,MSC通過可溶性因子(如調節IL-6、BAFF,增強IDO)和接觸依賴機制,抑制B細胞增殖、分化為漿細胞及免疫球蛋白產生,從而降低致病性自身抗體滴度。
旁分泌、細胞外囊泡及代謝-表觀遺傳機制
MSC分泌復雜的旁分泌組(含TGF-β、IL-10、HGF、VEGF、PGE2及IDO代謝物),可下調NF-κB信號和促炎因子,促進血管生成與組織修復,并誘導免疫細胞向耐受表型轉變。
此外,MSC釋放的細胞外囊泡(含miR-21、miR-146a、miR-155等)能重現其免疫調節作用,抑制TLR/NF-κB通路和Th17分化,支持Treg穩定性;相比全細胞療法,囊泡免疫原性更低、更易標準化。
最后,MSC還通過IDO-犬尿氨酸通路、腺苷信號(CD39/CD73)和活性氧調節,將T細胞和巨噬細胞從糖酵解促炎狀態轉變為氧化磷酸化調節表型,并通過組蛋白修飾、DNA甲基化穩定耐受相關的轉錄程序。
臨床試驗證據
在機制研究不斷深化的同時,MSC療法的臨床驗證也在持續推進。
一項截至2025年2月的系統性綜述與薈萃分析(納入42項隨機對照試驗、涉及2,183名參與者)評估了MSC移植在RA、SLE、脊柱關節炎、原發性干燥綜合征等多種風濕免疫病中的療效與安全性[2]。

結果顯示,MSC移植可顯著改善SLE患者的系統性紅斑狼瘡疾病活動指數(SLEDAI);在RA中,總臨床有效率達到54%,且應答組CD4?CD25?FoxP3?Treg百分比升高,而CD4?IL-17A?Th17細胞百分比下降。更為重要的是,MSC移植并未增加不良事件的發生率,支持了其在多種風濕免疫病中的安全性。
在臨床研究的最新進展方面,多項I/II期試驗正在積極招募或已完成初步分析。一項人臍帶間充質干細胞(hUC-MSC)治療中重度SLE的I/II期臨床研究(NCT07041801)計劃納入58名受試者,通過低、中、高三個劑量組及安慰劑對照設計,系統評估hUC-MSC注射劑的安全性、藥效動力學和免疫原性。
另一項針對活動性增殖性狼瘡腎炎的IIb期、雙盲、安慰劑對照隨機試驗(NCT03673748)正在評估單次靜脈輸注骨髓來源MSC(2百萬細胞/kg)對難治性LN患者的療效,預計2027年完成主要終點分析。
此外,一項臍帶來源MSC治療RA的I期試驗(NCT05003934)采用單次靜脈輸注1億個細胞,計劃進行長達48個月的隨訪評估。特別值得一提的是,MSC聯合IFN-γ的方案在RA治療中展現出令人矚目的前景:一項臨床試驗(ChiCTR-INR-17012462)報告,聯合治療組在3個月時的ACR20應答率達到93.3%,而MSC單藥組僅為53.3%,且1年隨訪期內未發現重大安全性問題。
挑戰與窗口期
MSC來源(骨髓、脂肪、臍帶)、培養條件、給藥方案差異大,限制療效可比性。最佳治療窗口可能是疾病早期,此時有機會糾正免疫失衡至接近生理狀態。
二、調節性T細胞免疫療法
概念與基本原理
調節性T細胞(Treg)療法的目標是通過在慢性自身免疫性炎癥疾病患者體內擴增或輸注自體、基因工程改造或異體Treg細胞來恢復免疫耐受。在炎癥性風濕病中,調節性T細胞的數量和功能均存在不同程度受損。Treg功能失調被認為是自身免疫性疾病的標志性特征,恢復這種功能障礙可能調節疾病進程并誘導疾病緩解。
近年來,Treg療法已從概念驗證階段進入臨床試驗的實質性探索階段。2026年3月,Quell Therapeutics公司已獲得英國MHRA批準,啟動了名為CHILL的I/II期臨床研究,評估其基于CD19靶向的CAR-Treg產品QEL-005在難治性RA和系統性硬化癥中的安全性與初步療效。該研究計劃在英國、德國和西班牙納入最多16名成年參與者,預計2027年第一季度發布早期臨床數據[3]。

同時,一項評估新型IL-2mutein(MK-6194)選擇性擴增Treg的IIa期試驗也在SLE患者中進行中,旨在解決Treg擴增療法開發中的技術挑戰,預計2027年4月完成主要終點分析。
現有挑戰與未來方向
初步研究表明,Treg免疫療法可以抑制自身反應性免疫應答,并可能提供持久的治療效果。然而,Treg療法的高昂成本和技術挑戰,以及對病原體反應減弱和潛在致癌風險的安全性擔憂,仍在很大程度上限制了其廣泛的臨床應用。未來研究需要進一步優化Treg細胞在體外輸注前的穩定性與擴增效率,以提升治療效果并降低成本。
三、嵌合抗原受體(CAR)-T細胞療法
療法原理與基本流程
CAR-T細胞療法是免疫療法的前沿技術,最初用于血液腫瘤,現正被探索作為自身免疫性疾病的一種變革性手段。其核心是對患者自身的T細胞進行基因工程改造,使其表達嵌合抗原受體(CAR),從而識別并清除驅動疾病病理的自身反應性B細胞或T細胞(圖1)。
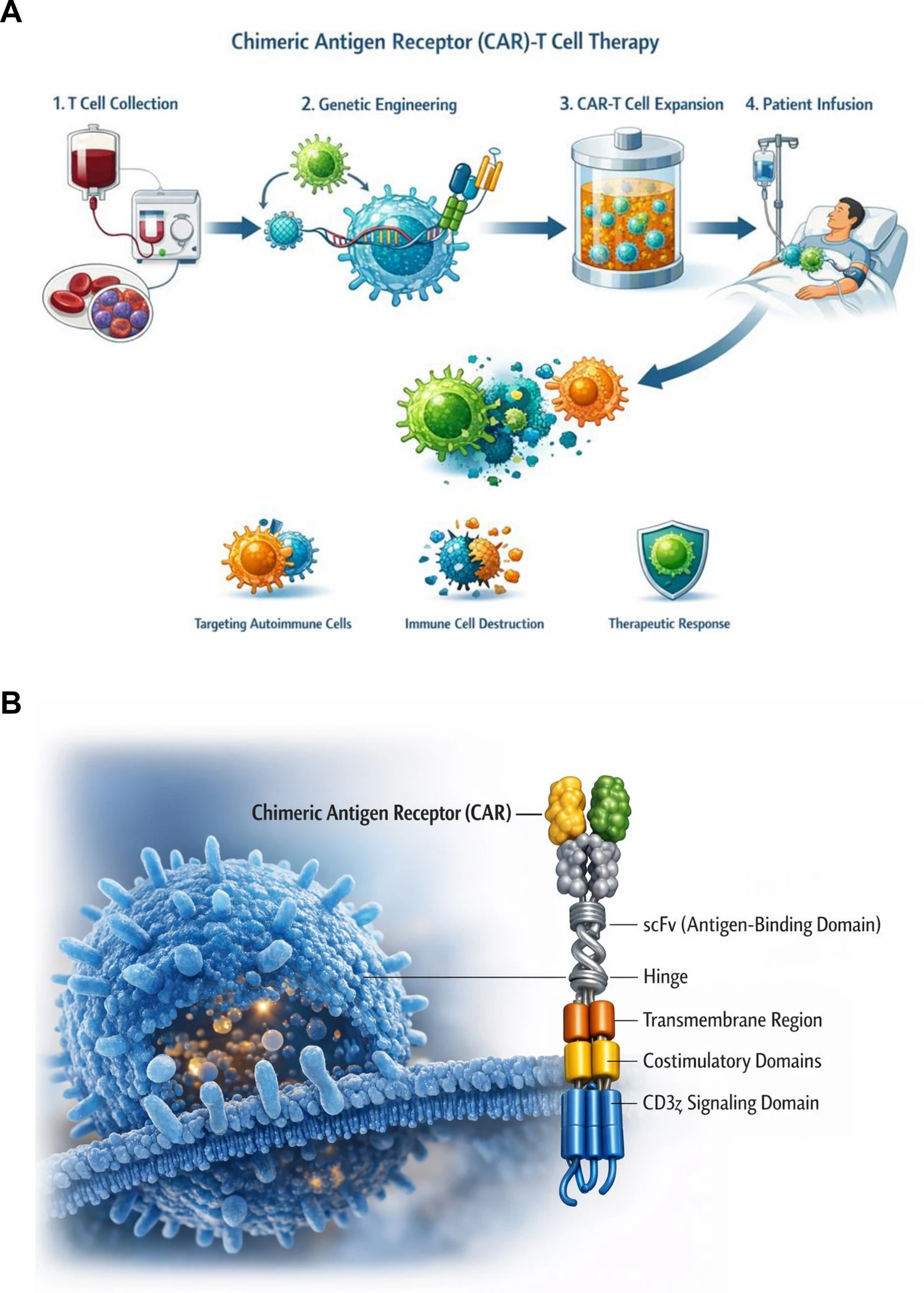
標準流程包括:從患者血液采集T細胞(白細胞分離術);利用病毒或非病毒載體導入CAR構建體;體外擴增修飾后的T細胞至治療劑量;最后將CAR-T細胞回輸患者體內,使其精準尋找并摧毀致病免疫細胞。
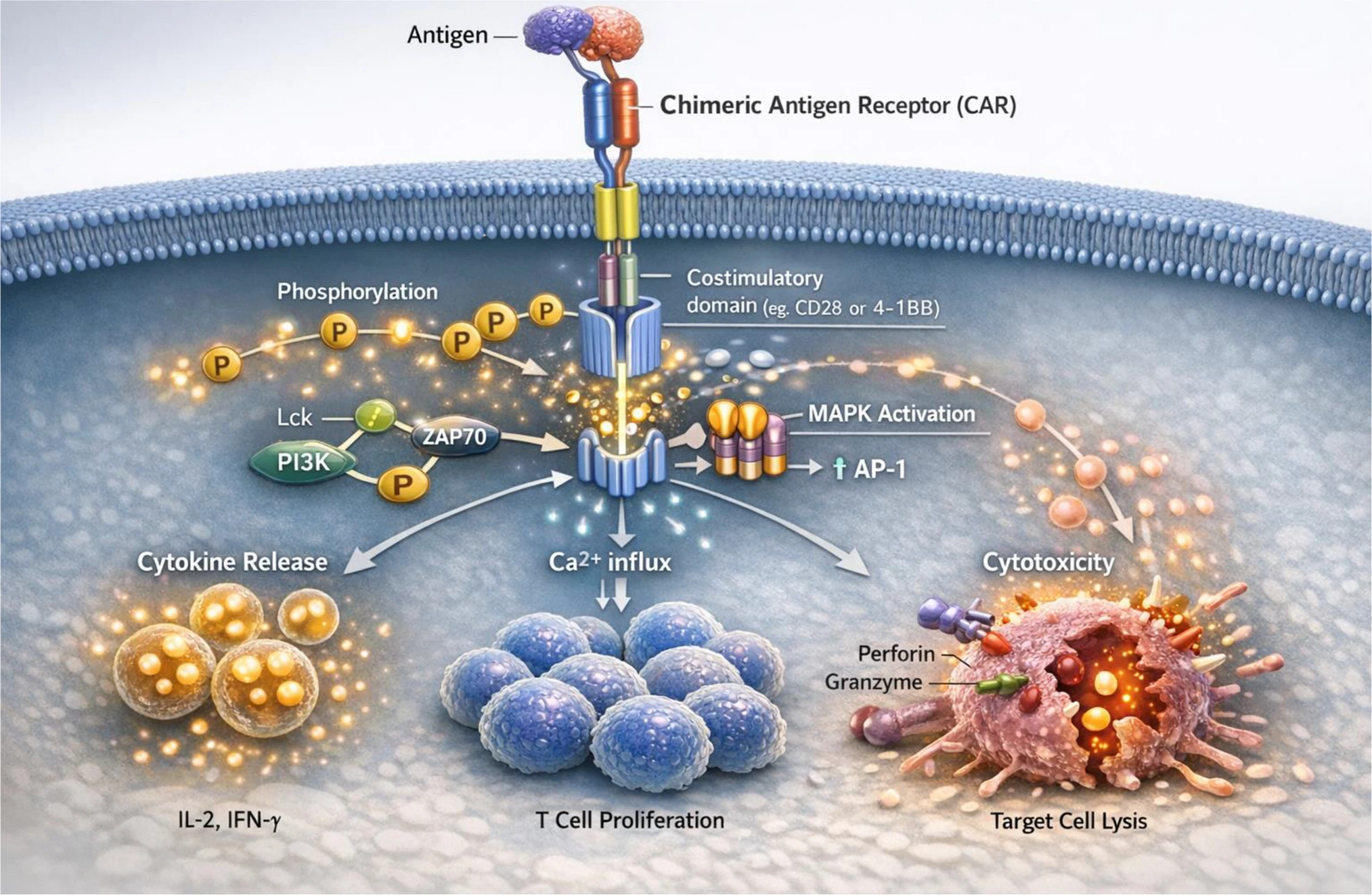
CAR結構與信號激活機制
CAR結構包含細胞外抗原識別域(通常源自單克隆抗體的單鏈可變區scFv)、跨膜域和多個細胞內信號域(含共刺激域和CD3ζ信號域)。當CAR與靶抗原結合后,細胞內CD3ζ和共刺激域(如CD28或4-1BB)會誘導早期信號事件(如Lck、ZAP70、PI3K及磷酸化級聯),進而激活下游通路(Ca2?內流、MAPK/AP-1通路),最終產生細胞因子釋放(IL-2、IFN-γ)、T細胞增殖以及對靶細胞的細胞毒性作用(穿孔素/顆粒酶途徑)。這些效應構成了CAR-T治療自身免疫病的功能基礎。
自身免疫病中的應用靶點與臨床前證據
在自身免疫性疾病中,CAR-T細胞療法正被研究用于選擇性清除致病性免疫細胞。靶向CD19的CAR-T細胞可清除自身反應性B細胞,也有研究探索靶向自身反應性T細胞的策略,從而阻斷自身免疫級聯反應。臨床前研究已證實該概念的有效性,尤其在以致病性B細胞為核心驅動因素的RA和SLE等疾病中展示了明確的治療潛力。
臨床試驗證據
CAR-T療法在自身免疫病中的臨床研究進展尤為迅猛。最為矚目的是CASTLE(CAR-T cells in systemic B cell mediated autoimmune disease)I/IIa期臨床研究,其完整結果已于2026年1月發表于Nature Medicine[4]。

該研究納入了24名治療抵抗的SLE(10例)、系統性硬化癥(9例)和特發性炎性肌病(5例)患者,所有患者均接受單次輸注自體CD19 CAR-T細胞(Zorpo-cel)。
主要安全性終點方面,未發生2級以上CRS,也未出現ICANS。主要療效終點方面,22/24(91.7%)的患者在24周時達到了預定義的療效終點:9/10的SLE患者達到DORIS緩解,9/9的SSc患者疾病未出現進展,4/5的IIM患者達到ACR主要/中度應答。更重要的是,所有患者在24周的整個觀察期內均未使用糖皮質激素或其他免疫抑制劑。
在SLE領域,2025年12月,另一項I期劑量遞增研究(NCT06551142)評估了relmacabtagene autoleucel(relma-cel)——一種CD19 CAR-T細胞產品——在中重度活動性SLE中的安全性和有效性。8例女性患者在接受氟達拉濱和環磷酰胺預處理后接受了單次CAR-T細胞輸注(劑量范圍為50×10?至100×10?)[5]。

結果顯示,未發生劑量限制性毒性,不良事件可控(7例出現CRS,1例出現ICANS)。所有患者在6個月時均達到SRI-4應答,6例達到LLDAS,5例達到DORIS緩解。平均SLEDAI-2K評分從基線時的12.625降至隨訪時的3.25,腎臟功能和補體水平也獲得顯著改善。
在通用型CAR-T方面,Fate Therapeutics公司的FT819——一種源于誘導多能干細胞系的現貨型CD19 CAR-T細胞產品——在I期臨床試驗中已治療了12例SLE患者和1例SSc患者。數據顯示,FT819在不需強化預處理化療的條件下即實現了持續的B細胞耗竭和臨床應答,SLEDAI-2K評分在劑量2組中從基線的平均14.3降至6個月的4,降幅達78%。
主要安全風險與不良反應
盡管前景廣闊,CAR-T療法伴隨顯著的安全隱患。主要包括:
①靶向腫瘤外效應——CAR-T可能誤傷表達相同抗原的健康細胞,導致非預期組織損傷;
②細胞因子釋放綜合征(CRS)——由大量活化的CAR-T細胞釋放細胞因子引發的全身性炎癥反應,可能危及生命;
③神經毒性——部分患者出現機制尚在研究中的神經系統副作用;
④長期免疫抑制——B細胞耗竭增加感染風險,并可能損害疫苗反應能力。這些風險限制了其廣泛應用。
當前挑戰與未來改進方向
目前CAR-T療法成本高昂且資源密集,需要專門設施進行個體化細胞處理和患者監測,規模化推廣困難。
未來研究方向包括:開發更高特異性的CAR以減少脫靶效應;設計“自殺開關”以便在嚴重不良事件時可控清除CAR-T細胞;探索同種異體(“現成”)CAR-T產品以降低成本和提高可及性;以及研究與其他免疫調節劑的聯合療法來增強療效。隨著技術改進,治療成本有望降低,安全性和有效性將逐步提升。
四、外泌體的基本特征與治療相關功能
外泌體特征與功能
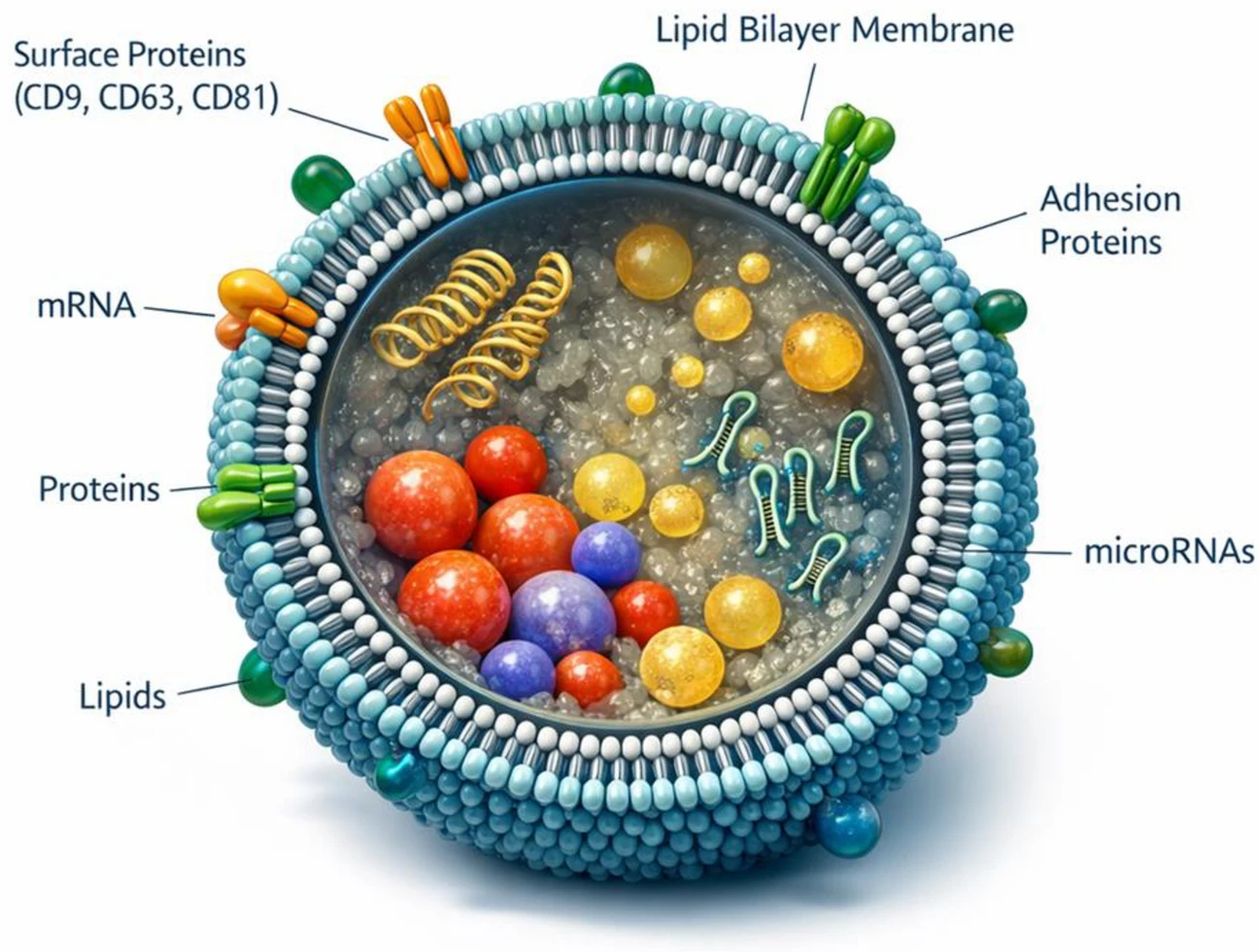
外泌體是直徑30—150納米的納米級細胞外囊泡,幾乎所有細胞類型(包括免疫細胞、間充質干細胞和滑膜成纖維細胞)均可分泌。它們在多囊泡體中形成并釋放至細胞外空間,作為細胞間通訊的重要介質。
外泌體富含多種生物活性分子,例如蛋白質、脂質、mRNA和microRNA(miRNA),這些分子可以調節受體細胞的功能和表型表達。外泌體的雙層脂質結構如圖2所示。外泌體的生物發生途徑包括早期內體、多囊泡體(MVBs)以及腔內囊泡釋放到細胞外空間(圖3A)。
外泌體一旦產生,便會附著在靶細胞上,并通過主要的攝取途徑進入細胞,包括胞吞作用、膜融合以及靶細胞受體介導的內化(圖3B)。
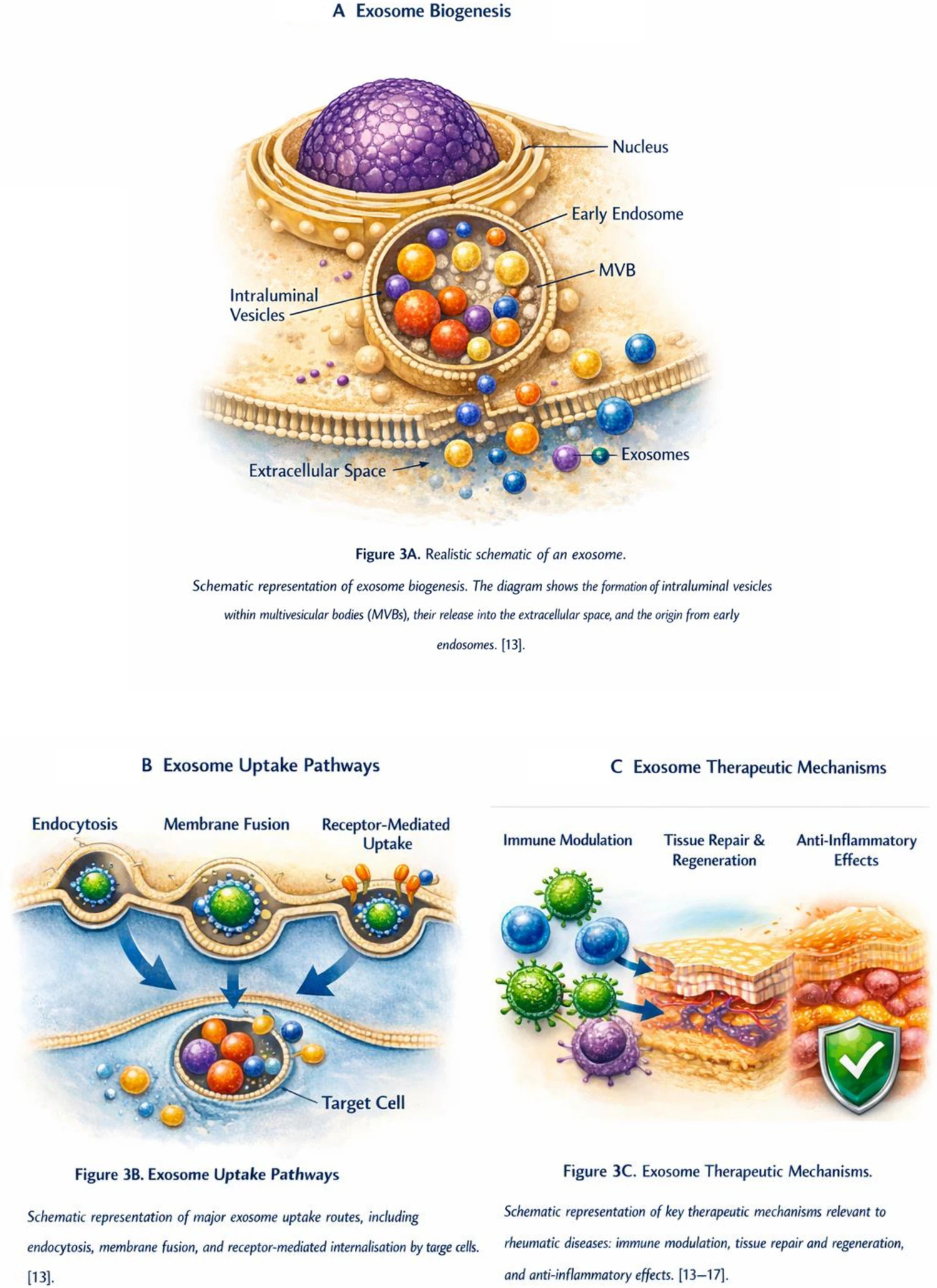
外泌體隨后可以發揮多種關鍵的生物學效應,例如:免疫調節、組織修復和再生以及抗炎作用,所有這些都是與風濕性疾病治療相關的關鍵治療機制(圖3C)。
在風濕病中的具體免疫調節機制
MSC來源的外泌體在自身免疫性風濕病中展現出強大的免疫調節能力。它們攜帶抗炎細胞因子(TGF-β、IL-10)、免疫調節性miRNA及表面分子,能夠抑制自身反應性T細胞和B細胞的活化與增殖,抑制樹突狀細胞成熟并促進耐受性表型,同時誘導巨噬細胞向抗炎性M2表型極化。此外,外泌體還能減少促炎細胞因子(如TNF-α、IL-6)的產生并增強免疫抑制通路,從而系統性地重建免疫平衡(圖4)。
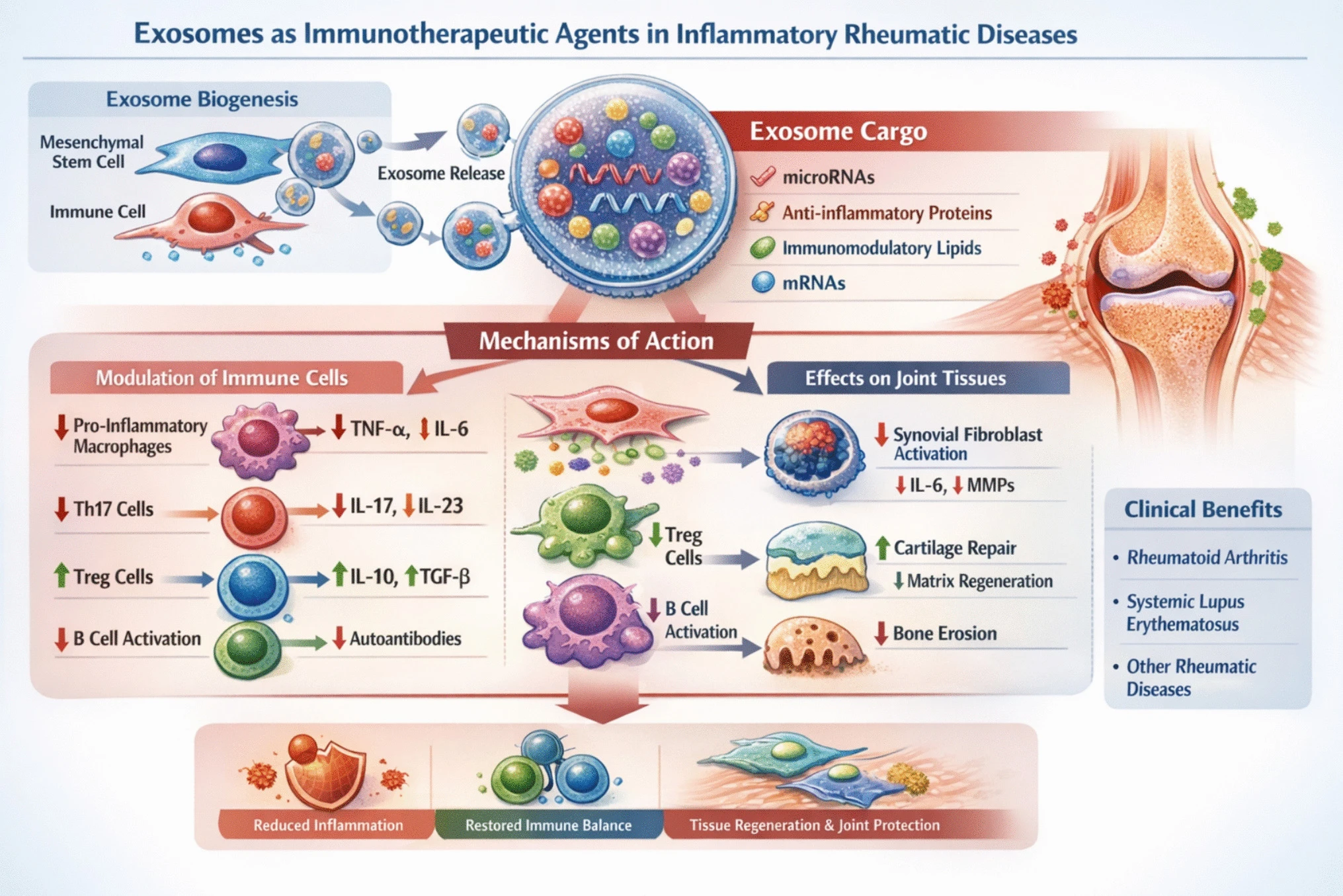
臨床前證據與“無細胞納米免疫療法”概念
在類風濕性關節炎 (RA) 和系統性紅斑狼瘡 (SLE) 的臨床前模型中,間充質干細胞 (MSC) 來源的外泌體已被證明可以抑制滑膜炎癥、減少軟骨退化并促進組織修復,凸顯了其治療潛力。因此,外泌體可以提供一種無細胞的納米細胞免疫療法(圖4)。
臨床試驗進展與前景
盡管臨床前數據令人鼓舞,外泌體療法在風濕病領域的臨床試驗尚處于早期探索階段。目前,一項I/IIA期研究(MESAE,NCT07131683)正在評估人臍帶MSC來源外泌體(HUC-MSC-EXO)在自身免疫性腦炎患者中的安全性和初步療效,采用鼻內給藥方案,包含三個劑量隊列的劑量爬坡階段和一個隨機雙盲安慰劑對照的擴展階段[6]。

該研究為MSC來源外泌體在自身免疫病中的臨床應用提供了重要的可行性參考,但在風濕病領域仍需開展專門的臨床試驗加以驗證。
優勢、挑戰與未來方向
與全細胞療法(如CAR-T、MSC)及單克隆抗體相比,外泌體具有多項優勢:免疫原性降低(缺乏主要組織相容性復合體分子,最大程度減少了免疫排斥風險)、致瘤性較低、易于儲存和標準化(促進“現成”治療產品的開發)、以及具有靶向遞送潛力。
然而,在廣泛臨床應用前仍需解決若干挑戰:包括建立標準化的分離與表征方法以確保純度和效力,確定最佳劑量、給藥頻率與途徑,評估長期安全性和脫靶效應,以及克服規模化生產和質量控制方面的監管與生產障礙。
未來發展方向包括外泌體工程改造(如負載特定miRNA或藥物、表面修飾以實現靶向遞送),以及基于外泌體的液體活檢用于疾病監測和個體化醫療。最終,外泌體療法有望為炎癥性風濕病帶來創新性的無細胞精準治療策略。
六、四大療法對比與未來展望
| 維度 | MSC | Treg | CAR-T | 外泌體 |
|---|---|---|---|---|
| 作用方式 | 旁分泌+接觸 | 免疫抑制 | 清除致病細胞 | 遞送生物活性分子 |
| 細胞來源 | 異體/自體 | 自體(擴增) | 自體(基因改造) | 細胞培養上清 |
| 制備周期 | 數周 | 數周 | 數周 | 可批量生產 |
| 免疫原性 | 低 | 無 | 無(自體) | 極低 |
| 主要風險 | 標準化不足 | 致癌、感染 | CRS、神經毒性、B細胞耗竭 | 長期安全性未知 |
| 成本 | 中等 | 高 | 極高 | 低-中等 |
| 臨床階段 | II/III期 | I/II期 | I/II/III期 | 臨床前/I期 |
共同趨勢:從“免疫抑制”轉向“免疫重建”;從“癥狀控制”轉向“治愈可能”;從“一刀切”轉向“精準靶向”。
七、常見問題解答(FAQ)
參考資料:
[1]:Chikanza, I.C., Sakkas, L.I. Cell immunotherapy in autoimmune rheumatic diseases: a paradigm shift in the therapy of autoimmune inflammatory rheumatic diseases. Clin Rheumatol (2026). https://doi.org/10.1007/s10067-026-08103-0
[2]:Zeng, L., Liu, C., Wu, Y.?et al.?Efficacy and safety of mesenchymal stromal cell transplantation in the treatment of autoimmune and rheumatic immune diseases: a systematic review and meta-analysis of randomized controlled trials.?Stem Cell Res Ther?16, 65 (2025). https://doi.org/10.1186/s13287-025-04184-x
[3]:https://reachmd.com/news/chill-trial-launch-quells-qel005-cartreg-enters-phase-12/2485897/
[4]:Müller, F., Hagen, M., Wirsching, A. et al. CD19 CAR-T cells for treatment-refractory autoimmune diseases: the phase 1/2 CASTLE basket trial. Nat Med 32, 1142–1151 (2026). https://doi.org/10.1038/s41591-025-04185-6
[5]:https://www.sciencedirect.com/science/article/pii/S0896841125001349?via%3Dihub
[6]:https://ichgcp.net/zh/clinical-trials-registry/NCT07131683?hl=it
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信