核心速覽:間充質干細胞(MSC)通過直接細胞接觸與旁分泌雙重機制,調節T細胞、B細胞、NK細胞及樹突狀細胞功能,重塑免疫穩態。臨床研究證實,MSC在系統性紅斑狼瘡(6年隨訪顯示SLEDAI顯著下降)、類風濕關節炎(64例患者3年隨訪,DAS28及HAQ顯著改善)、多發性硬化(II期RCT顯示行走及膀胱功能改善)等自身免疫病中展現出安全性與療效。外泌體(MSC-EVs)作為無細胞替代策略,因其易于保存、標準化及低免疫原性而備受關注。本文系統綜述MSC的免疫調節機制、臨床試驗數據及未來發展方向[1]。
間充質干細胞雙機制協同:免疫調節+旁分泌活性解鎖自身免疫疾病治療新維度
01、自身免疫病的治療困境:為什么需要新策略?
自身免疫性疾病源于免疫系統失衡,免疫細胞錯誤攻擊自身組織,導致類風濕關節炎(RA)、系統性紅斑狼瘡(SLE)、多發性硬化(MS)、1型糖尿病(T1DM)、原發性干燥綜合征(pSS)、銀屑病、炎癥性腸病(IBD)等慢性疾病。這類疾病需要長期甚至終身治療。
傳統的免疫抑制藥物(如糖皮質激素、甲氨蝶呤、生物制劑靶向IL-1、IL-6、TNF-α等)雖然有效,但存在三大問題:
- 藥物耐受性:長期使用后療效下降
- 不良反應:增加感染風險、骨質疏松、代謝紊亂
- 惡性腫瘤風險:長期免疫抑制可能增加淋巴瘤等腫瘤發生率
因此,利用間充質干細胞的免疫調節特性進行輔助治療,已成為一種頗具前景的新型治療策略。

02、間充質干細胞的核心特性
間充質干細胞是一類具有自我更新能力和多向分化潛能的基質細胞,最初在骨髓中發現,后續研究證實其廣泛存在于以下組織:
- 骨髓
- 脂肪組織
- 臍帶(華通氏膠)
- 牙髓
- 胎盤
- 羊水
關鍵特性:
- 可分化為脂肪、軟骨、成骨等中胚層細胞
- 特定條件下可跨胚層分化為外胚層或內胚層組織(發育可塑性)
- 低腫瘤風險,增強臨床應用可行性
- 低免疫原性,異體使用無需嚴格配型
近年來,MSC的免疫調節功能成為研究熱點,其通過直接接觸或旁分泌作用調控免疫細胞活性,為治療自身免疫性疾病提供了新思路。
03、間充質干細胞的免疫調節機制
MSC通過雙重機制發揮免疫調節作用:①直接細胞接觸;②旁分泌活性(細胞因子、趨化因子、生長因子及外泌體)。
3.1 直接細胞接觸:與免疫細胞的物理相互作用
MSC可以直接與以下免疫細胞相互作用,調節其活化、增殖和分化:
| 免疫細胞類型 | MSC的調節作用 |
|---|---|
| T細胞 | 抑制效應T細胞(Th1、Th17)增殖和活化;促進調節性T細胞(Treg)生成和功能 |
| B細胞 | 影響B細胞分化、抗體產生和存活 |
| 自然殺傷細胞(NK) | 改變NK細胞的細胞毒活性和細胞因子產生 |
| 樹突狀細胞(DC) | 影響DC的成熟、抗原呈遞和細胞因子分泌 |
| 巨噬細胞(Mφ) | 促進M1(促炎)向M2(抗炎)表型極化 |
| 中性粒細胞 | 調節其募集和功能 |
這些相互作用共同維持免疫平衡,防止過度免疫反應。我們總結了MSCs在治療自身炎癥疾病中的作用機制,如圖1所示。
3.2 旁分泌機制:細胞因子與外泌體
MSC分泌多種生物活性分子,以旁分泌方式影響免疫細胞行為:
- 細胞因子:IL-10、TGF-β(抗炎)、PGE2(免疫調節)
- 生長因子:HGF、VEGF(組織修復)
- 趨化因子:調節免疫細胞遷移
MSC來源的細胞外囊泡(MSC-EVs) 近年受到高度關注。外泌體是直徑30-150nm的小囊泡,內含蛋白質、脂質、mRNA及miRNA。
MSC-EVs的優勢:更易保存、運輸和生產(-80℃或凍干),可標準化、批量生產,使用更安全(無成瘤風險、無活細胞排斥),特定miRNA負載賦予靶向治療潛力。
3.3 作用機制總結(圖1)
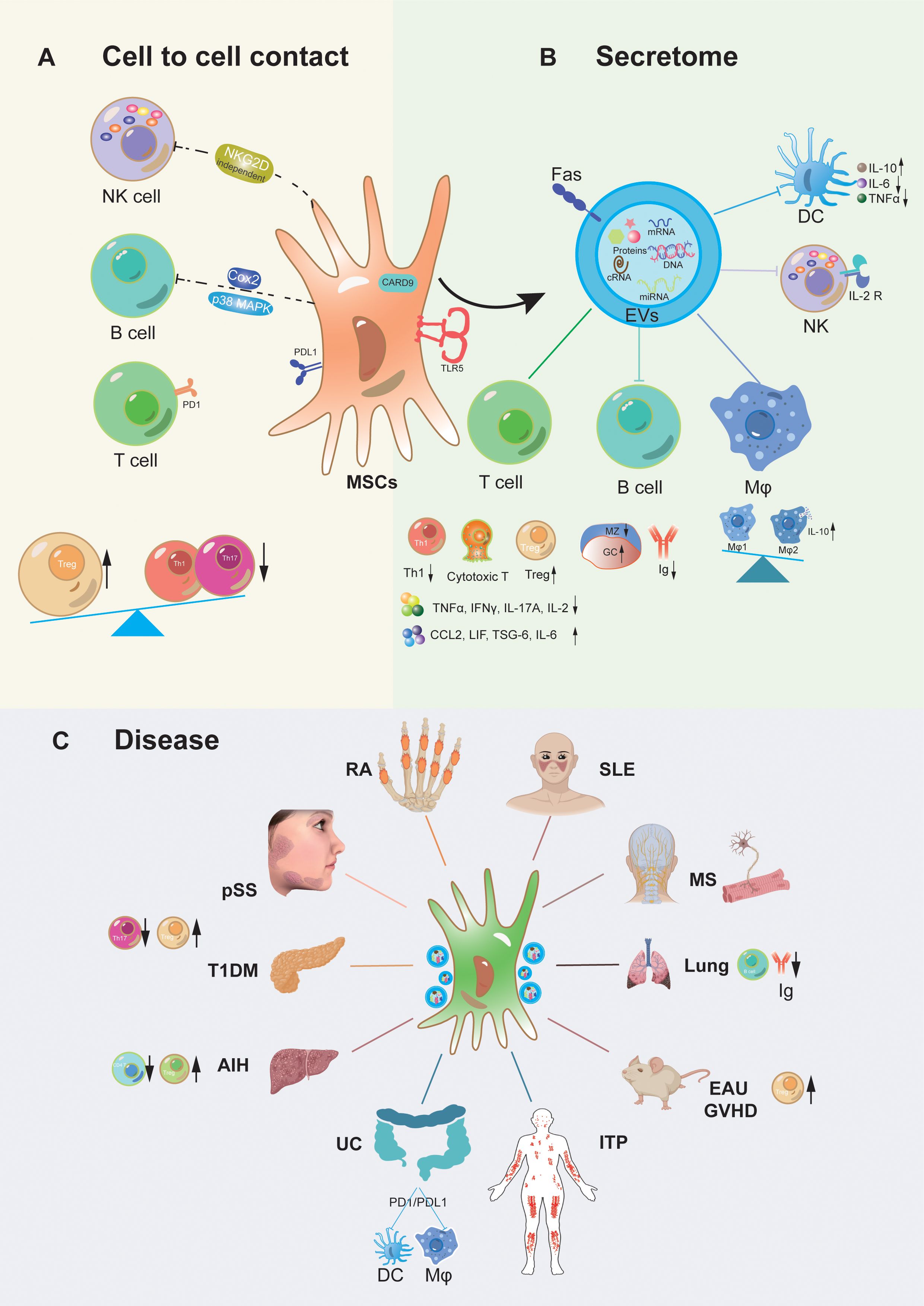
圖1:MSC移植治療自身炎癥性疾病的作用機制
- A. 直接接觸途徑:MSC與T細胞、B細胞、NK細胞、DC、巨噬細胞直接相互作用
- B. 旁分泌途徑:MSC分泌外泌體/細胞外囊泡,內含趨化因子、細胞因子、生長因子,靶向作用于各類免疫細胞
- C. 組織來源多樣性:骨髓、脂肪、臍帶、胎盤等來源的MSC均具有免疫調節功能
04、間充質干細胞通過免疫調節機制在治療自身免疫炎癥疾病中的臨床應用
我們在表1中總結了MSCs在治療自身免疫性疾病方面已完成和正在進行的臨床試驗。這些注冊研究的結果均證明了MSCs在治療自身免疫性疾病方面的安全性和有效性。

05、間充質干細胞通過免疫調節機制治療系統性紅斑狼瘡
2016年,國際期刊雜志《臨床與實驗醫學》發表了一篇“臍帶間充質干細胞移植治療系統性紅斑狼瘡的長期安全性:6年隨訪研究”的文章。

該研究是由孫凌云團隊對9例難治性SLE患者進行臍帶MSCs輸注,隨訪6年發現患者系統性紅斑狼瘡活動指數(SLEDAI)顯著下降,未出現嚴重不良反應,且肝腎功能和腫瘤標志物保持正常。
2018年,一項針對81例難治性SLE患者的II期臨床試驗顯示,接受異體MSCs治療后,患者5年總生存率達84%,34%達到臨床緩解,且多器官功能(如肺出血、間質性肺炎)改善。
作用機制:MSCs通過分泌TGF-β上調調節性T細胞(Treg)表達,通過前列腺素E2(PGE2)下調輔助性T細胞17(Th17)活性,從而平衡Th17/Treg比例,抑制炎癥反應。
06、間充質干細胞通過免疫調節機制治療類風濕性關節炎
2019年,中國空軍第986醫院的研究團隊從2000年1月至2017年1月期間,從中國空軍第986醫院研究招募了64名年齡在18-64歲之間的RA患者。
治療期間,患者在輸注100mL生理鹽水后立即通過靜脈注,40mLUC-MSC懸浮產品(2×10^7細胞/20mL)。使用血清學標志物測試來評估安全性,使用28關節疾病活動評分 (DAS28) 和健康評估問卷 (HAQ) 來評估UC-MSCs治療RA的長期效果和安全性。研究結果發表在《Dove Press》。
研究結果表明:臍帶間充質干細胞治療類風濕性關節炎(RA)在安全性和有效性方面都表現出長期而穩定。在治療后的1年到3年,患者的血液指標、肝腎功能和免疫球蛋白水平都在正常范圍內。同時,患者的疾病活動評分和健康評估問卷得分也都有顯著下降,這些數據都表明UC-MSCs治療的長期效果。
此外,研究人員還提供了兩位接受臍帶間充質干細胞治療前后的圖片。
第一位患者是一位68歲的男性,治療前關節疼痛、腫脹、變形嚴重,接受UC-MSC治療6個月后癥狀得到緩解,并維持至治療后3年(圖1A)。接受UC-MSC治療3年后,關節變形得到恢復(圖1B),疼痛也消失了,并且能夠自由活動和進行一些體育鍛煉。
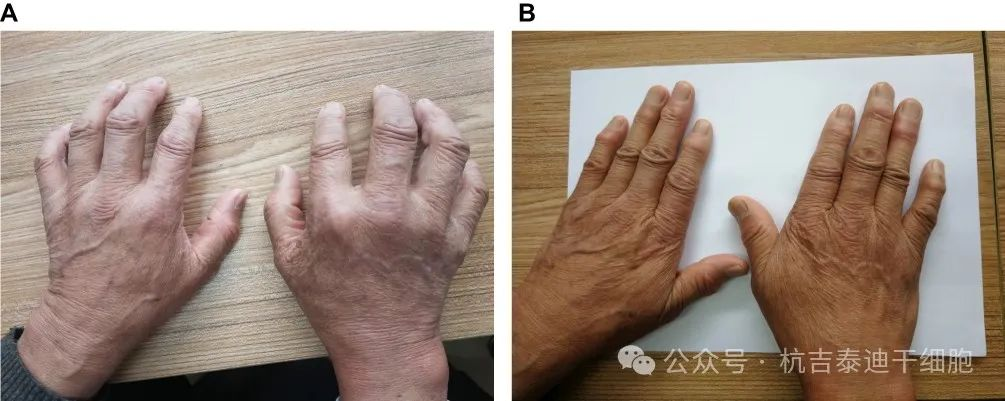
(A)顯示雙手無法伸直。(B)治療后3年,停用抗風濕藥物5年,雙手伸展自如,關節周圍風濕結節逐漸軟化、消退。
另一名33歲女性類風濕性關節炎患者,治療前關節腫脹及畸形較為嚴重(圖2A),治療后病情也獲得緩解。接受UC-MSC治療三年后,其關節畸形得到改善(圖2B),腫脹也得到較好的緩解。此外,她現在有時可以自由奔跑和進行一些體育鍛煉。

( A )咬牙困難,腫脹疼痛,晨僵,( B )經UC-MSC細胞治療1周后,癥狀明顯改善。
總體而言,本研究證明了UC-MSC治療類風濕性關節炎(RA)患者的長期安全性和有效性。UC-MSC的治療效果可維持3年,臨床療效穩定,顯著改善了RA患者的生活質量。
作用機制:MSCs通過抑制Th17細胞分化和促炎因子(如IL-17、TNF-α)分泌,同時促進抗炎因子(如IL-10)釋放,重塑免疫平衡。
07、間充質干細胞通過免疫調節機制治療多發性硬化癥
2024年,國際期刊雜志《干細胞研究與治療》發表了一篇“鞘內間充質干細胞-神經祖細胞治療進展型多發性硬化癥的療效:II期隨機安慰劑對照臨床試驗結”的文章。

這項研究旨在評估一種基于間充質干細胞-神經前體細胞(MSC-NP)的治療方法對進展性MS患者的療效。
結果表明:與生理鹽水相比,鞘內注射MSC-NP療法與需要輔助行走的患者群體的行走能力改善相關。此外,鞘內注射MSC-NP療法與膀胱功能改善相關,膀胱功能是影響MS患者生活質量的重要因素。其次,我們還發現了間接證據,表明該療法具有神經保護作用,具體表現為腦磁共振成像(MRI)皮質灰質體積變化。
最后,我們的研究也進一步證實了多次鞘內注射細胞的安全性和耐受性。臨床觀察結果顯示,治療后腦脊液(CSF)生物標志物發生了顯著的生物學變化。我們的研究提供了多項臨床和實驗室證據,證明了鞘內注射MSC-NP療法對進展型多發性硬化癥(MS)的有效性。
作用機制:MSCs通過調節Th1/Th2平衡,減少促炎因子(如IFN-γ),并促進髓鞘修復。
08、間充質干細胞治療其他自身免疫性疾病
炎癥性腸病(IBD):2021年,期刊雜志《Biomolecules》生物分子發表了一篇間充質干細胞/基質細胞治療炎癥性腸病的療效和安全性:最新系統評價的文章,該綜述旨在介紹有關MSC療法在IBD中的安全性和有效性的最新研究。

在PubMed上對MSC和IBD的臨床試驗進行了詳細的搜索策略,并選出了32項研究納入本綜述。最終綜述研究表明局部間充質干細胞注射治療肛周瘺管性克羅恩病(PFCD)具有長期療效,同時保持良好的安全性。
作用機制:MSCs通過分化為腸道上皮細胞修復屏障功能,并分泌抗炎因子(如IL-10)抑制過度免疫反應。
銀屑病:中南大學湘雅醫院對17例銀屑病患者進行臍帶MSCs治療,6個月后47.1%患者皮損面積改善超40%,且無嚴重副作用。
作用機制:MSCs抑制角質細胞過度增殖,調控Th1/Th17通路,減少促炎因子釋放。
09、間充質干細胞的免疫調節機制治療自身免疫性疾病的潛力
間充質干細胞(MSCs)通過雙重機制——與免疫細胞(如T細胞、B細胞、巨噬細胞)的直接接觸及旁分泌活性(細胞因子、外泌體等)——發揮免疫調節作用。其抑制PD-1/PD-L1通路、調控T細胞分化平衡(如增強Treg細胞、抑制Th1/Th17細胞),并重編程巨噬細胞向抗炎表型極化,從而重塑免疫穩態。
此外,炎性預處理可動態增強MSCs的免疫抑制能力,凸顯其精準調控潛力。這些特性使MSCs不僅能增強傳統療法的療效(如減少藥物耐藥性和毒副作用),還能促進組織修復,改善患者功能恢復與生活質量。
010、間充質干細胞的旁分泌活性與外泌體治療自身炎癥疾病的前景
MSCs的旁分泌效應,尤其是外泌體(MSC-EVs),已成為其免疫調控的核心機制。MSC-EVs通過遞送抗炎因子(如IL-10)、抑制促炎信號通路(MAPK/ERK、PERK/CHOP),調節T細胞分化并抑制B細胞過度活化,誘導免疫耐受環境。表達PD-L1的外泌體在自身免疫病及癌癥免疫治療中展現出靶向潛力。
研究還表明,MSC-EVs可重編程巨噬細胞功能并抑制NK細胞毒性,為炎癥和纖維化疾病的治療提供新策略。然而,需進一步闡明其分子機制以優化臨床應用。
011、間充質干細胞治療自身免疫性疾病的臨床進展與未來挑戰
多項臨床試驗驗證了MSCs在自身免疫病(如GVHD、紅斑狼瘡)中的安全性和療效。例如,重復輸注臍帶MSCs顯著降低慢性GVHD發生率,聯合療法可提升激素抵抗型急性GVHD的緩解率。基因修飾MSCs及TLR激動劑預處理等新興策略進一步增強了其免疫抑制功能。
然而,多發性硬化癥等疾病的II期試驗結果參差不齊,提示需針對性優化。未來研究需聚焦細胞來源標準化、最佳劑量與給藥途徑,以及長期安全性評估,同時探索MSCs與生物材料或靶向藥物的聯合應用,以實現更精準的免疫調控治療。
012、結論
間充質干細胞通過雙重機制——與免疫細胞的直接接觸及旁分泌活性(細胞因子、外泌體等)——發揮免疫調節作用。其通過抑制PD-1/PD-L1通路調控、調控T細胞分化平衡(增強Treg、抑制Th1/Th17)、重編程巨噬細胞向抗炎表型極化,從而重塑免疫穩態。
多項臨床試驗驗證了MSC在自身免疫病(如SLE、RA、MS、GVHD、銀屑病、IBD)中的安全性和療效。例如:
- SLE:6年隨訪顯示SLEDAI顯著下降,5年生存率84%
- RA:64例患者3年隨訪顯示DAS28及HAQ顯著改善,部分患者關節畸形恢復
- MS:II期RCT顯示行走及膀胱功能改善
常規療法與MSC的協同作用是治療自身免疫性炎癥疾病的可行策略,有望提升治療效果并減輕患者負擔。MSC為免疫介導疾病提供了有前景的治療選擇,其免疫調節和耐受性誘導是潛在機制。
未來仍需開展進一步研究和更大規模的試驗,以驗證其在不同患者群體和疾病背景下的療效和安全性。隨著研究的不斷深入,深入探究MSC復雜的作用機制并優化其在臨床環境中的應用至關重要,最終為更有針對性和更有效的治療干預鋪平道路。
013、常見問題解答(FAQ)
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。
主要參考資料:[1]Chen B, Chen Z, He M, Zhang L, Yang L and Wei L (2024) Recent advances in the role of mesenchymal stem cells as modulators in autoinflammatory diseases. Front. Immunol. 15:1525380. doi: 10.3389/fimmu.2024.1525380



 掃碼添加官方微信
掃碼添加官方微信