在過去20年中,干細胞療法被認為是治療多種疾病,特別是神經退行性疾病的一種很有前景的選擇。干細胞通過分泌神經營養因子、細胞置換、激活內源性干細胞和減少神經炎癥等不同機制,發揮保護神經和神經退行性疾病的作用。人們提出了多種干細胞來源,用于移植和修復受損組織。
近幾十年來,深入研究的重點是妊娠干細胞,認為它是細胞移植療法的新資源。本綜述介紹了最近臨床前/臨床應用妊娠干細胞治療神經退行性疾病的最新情況,包括阿爾茨海默病(AD)、帕金森病(PD)、亨廷頓病(HD)和肌萎縮側索硬化癥(ALS)[1]。不過,應鼓勵開展進一步的研究,以便將這種前景廣闊的治療方法應用于臨床。
圍產期組織的干細胞成為治療神經退行性疾病的新興策略
什么是神經退行性疾病:神經退行性疾病(NDDs)是指一組以大腦或脊髓神經元缺失為特征的病理狀態,通常與認知、精神和運動障礙等多種臨床表現相關。
NDD可由急性或慢性事件引發。急性病例,如缺血性中風和創傷性腦或脊髓損傷,是由創傷事件導致損傷部位神經元缺失引起的。另一方面,慢性病例與細胞群的選擇性喪失有關,如帕金森病(PD)中的多巴胺能神經元和肌萎縮性脊髓側索硬化癥(ALS)中的運動神經元。
大多數神經退行性疾病的特征是折疊錯誤的蛋白質(理化性質改變的蛋白質)堆積,這是疾病的標志。蛋白質積聚的例子有:
- (i) a-突觸核蛋白(a-syn),這是一種14kDa的小蛋白,由SNCA基因編碼,是路易體沉積物的主要成分,存在于帕金森病患者的大腦中;
- (ii) 在ALS患者的運動神經元中觀察到的43kDa的轉錄反應DNA結合蛋白的泛素化蛋白質內含物;
- (iii) Aβ斑塊(由39至42-aa長的Aβ肽片段組成)和神經纖維纏結(由 tau 寡聚體形成),在阿爾茨海默病(AD)中,tau寡聚體分別存在于神經元外部和內部;
- (iv) 突變的亨廷頓蛋白聚集體,據報道這是亨廷頓氏病(HD)的主要特征之一,存在于整個大腦神經細胞的細胞質和細胞核中;
- (v) 朊病毒蛋白PrPSc累積,這是一種由位于20號染色體上的PrP(PRNP)基因編碼的253氨基酸蛋白,也顯示出一種突觸沉積模式,在所謂的 “朊病毒疾病 “中被檢測到;
- (vi) FET蛋白,這是一個蛋白家族,包括FUS(融合肉瘤蛋白)、EWSR(尤文肉瘤RNA結合蛋白1)和TAF15(TATA結合蛋白相關因子,TAF15),據報道,在神經系統疾病(如額顳葉變性(FTLD)和漸凍人性脊髓側索硬化癥)中會形成細胞質聚集體。
遺憾的是,迄今為止還沒有成功治療神經退行性疾病的方法。由于神經退行性疾病的病理生理學性質復雜,可能需要一種多模式治療方法。其目的是補充丟失的神經細胞,清除有毒沉積物,并保證為這些細胞的存活和可塑性提供必要的安全環境。近年來,干細胞療法被認為是治療神經退行性疾病的一種新的潛在治療策略。
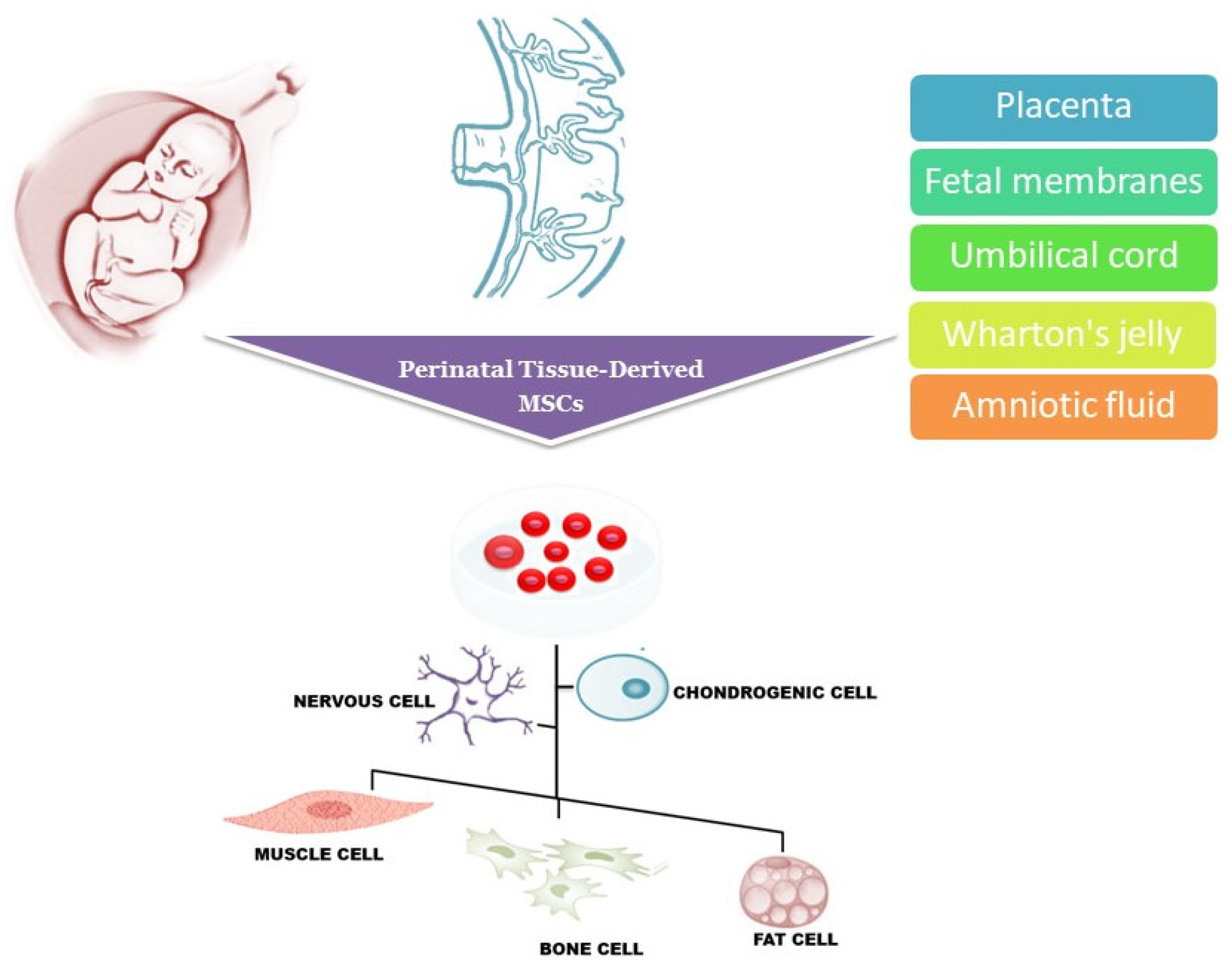
不同的細胞類型,如胚胎干細胞 (ESC)、成體干細胞和誘導多能干細胞 (iPS) 已被測試其在移植后替代受損細胞和恢復組織功能的能力。在過去的幾年中,圍產期組織源性間充質干細胞(MSC),包括胎盤源性、絨毛膜源性和臍帶源性MSCs,由于其可獲取性大、能夠分化為多種細胞譜系而引起了極大的興趣。圖1),移植后不存在致瘤性,重要的是,缺乏倫理問題最初限制了胚胎干細胞的可用性。
從胎兒材料中分離干細胞不會引起倫理問題,因為這些組織在分娩后立即被視為醫療廢物并且很容易獲得。研究材料可以從整個懷孕期間、計劃終止妊娠以及足月陰道分娩或剖腹產后的侵入性診斷和治療程序中獲得的組織中收集。
世界各地都在進行針對圍產期干細胞的研究。美國和中國等幾個國家已經制定了再生醫學產品的法規。目前,每個歐盟成員國都有針對胚胎干細胞和圍產期組織研究的具體規定。圍產期干細胞臨床試驗必須得到當地生物倫理委員會的批準,并按照歐盟臨床試驗注冊法進行。
截至2024年1月,全球已有2630項注冊臨床試驗使用間充質干細胞療法;然而,只有12種間充質干細胞療法獲得監管機構批準商業化。MSC批準的12種產品中有9種來自亞洲,而韓國是批準療法最多的國家。其中,有NeuroNata-R,一種自體骨髓間充質干細胞療法,具有神經保護作用,可以緩解ALS的進展。
圍產期組織的干細胞成為治療神經退行性疾病的新興策略
本綜述總結了關于圍產期組織來源的間充質干細胞在治療神經退行性疾病中的潛在用途及其臨床局限性的生物學和轉化研究的最新進展。
阿爾茨海默病的細胞療法:臨床試驗的主要發現
| 試用ID | 階段 | MSC型 | 學習規劃 | 路線 | 數量 | 發現 |
|---|---|---|---|---|---|---|
| NCT01297218 | 完全的 | hUCB-MSCs | 第一階段開放標簽、單中心 | 單次腦室內輸注 | 劑量A—每1個進入位點每5μL250,000個細胞,每個大腦300 萬個細胞 劑量B—每1個進入位點每5μL 500,000個細胞,每個大腦600萬個細胞 | 通過立體定向手術將 hUCB-MSC注射到海馬和楔前葉 是安全且耐受性良好的,但無法對AD病理生理過程產生有益影響 |
| NCT01696591 | 未知 | hUCB-MSCs | NCT01297218的長期安全性和 有效性 隨訪 | 與NCT01297218相同 | ||
| NCT02054208 | 完全的 | hUCB-MSCs | 1/2a期,雙盲,單中心 | Ommaya 水庫腦室內 注射 | n=42每隔4 周 注射3次低劑量:1× 107 個細胞/2 mL高劑量:3×107 個細胞/2mL安慰劑組生理鹽水 | 重復腦室內給藥足夠安全且 耐受性相對良好; 需要重復給藥 以維持 治療效果 |
| NCT03172117 | 未知 | hUCB-MSCs | NCT02054208 1期和2期長期隨訪 (隨機四盲對照) | 與NCT01297218相同 | ||
| NCT04040348 | 積極的 | 同種異體 hUCB-MSC | 第一階段,前瞻性、開放標簽試驗 | 鞘內 | n = 6一年內 每 13 周注射 4 劑 1 億個 UCB-MSC | 不適用 |
| NCT04684602 | 招聘 | AM- 和 UC-MSC | 多中心、前瞻性、開放標簽臨床試驗 | 通過特定情況的 給藥途徑注射 | n = 5000 | 不適用 |
| NCT01547689 | 未知 | 人臍帶間充質干細胞 | 1/2 期、開放標簽、單中心、自我對照臨床試驗 | 8 次靜脈 輸液 | n = 30 0.5 × 10 6 UC-MSCs/kg 每季度第一個月每兩周一次 時間間隔: 兩個半月 | 不適用 |
| NCT02672306 | 未知 | 人臍帶間充質干細胞 | 多中心、隨機、雙盲、安慰劑對照試驗 | 8 次靜脈 輸液 | n = 16 實驗組:0.5 × 10 6 UCMSCs/kg,每兩周一次 安慰劑組: 生理鹽水,每兩周一次 | 不適用 |
| NCT03899298 | 尚未 招募 | AM-和 UC-MSC | 階段1 | 靜脈 輸注和鼻內手術 | n = 5000 | 不適用 |
盡管已經進行或正在進行多項臨床試驗來評估間充質干細胞治療神經退行性疾病的療效和安全性,但已發表的結果很少。
在NCT01297218和NCT01696591研究中,通過立體定向注射將同種異體hUCB-MSCs注射到AD患者的海馬和楔前葉,在2年的隨訪期間沒有出現劑量限制性毒性。常見的不良事件是手術過程中的傷口疼痛、頭痛、頭暈和術后譫妄,因此支持間充質干細胞移植的安全性和可行性。
Kim等人進行的I期臨床試驗。對9名輕至中度AD患者的研究也表明,人UCB-MSC腦室內移植是安全可行的。常見的不良事件是發燒、頭痛、惡心和嘔吐,并在36小時內緩解。總之,已經進行了多項臨床試驗來解決神經退行性疾病患者間充質干細胞移植的安全性。
總體而言,這些研究的結果支持自體和同種異體間充質干細胞移植的安全性和可行性。已發表的報告顯示,移植并未形成腫瘤,治療干預也未導致死亡。然而,盡管各種臨床試驗的療效及其經過驗證的安全性和可行性取得了令人鼓舞的結果。
干細胞治療亨廷頓病
多項研究表明間充質干細胞在治療亨廷頓病(HD)方面具有潛在功效。最近的一項薈萃分析證實了MSC對亨廷頓病動物模型的總體積極影響,反映在形態變化、運動協調性、肌肉力量、神經肌肉肌電圖活動、皮質相關運動功能和紋狀體相關運動功能上,而認知方面則沒有。
MSC療法改變了這一點。在不同的MSC來源中,骨髓MSC是研究最多的細胞,可有效改善運動協調性。然而,雖然能夠減少HDR6/2小鼠模型的行為和組織學缺陷,但骨髓來源的MSC移植到小鼠紋狀體后不會產生新的神經元。因此,其他來源的干細胞(主要是妊娠干細胞)越來越受到人們的關注。
埃布拉希米等人。(2018) 研究了UC-MSC在體外和體內對抗HD相關氧化應激的功效。他們發現這些細胞可以預防3-NP損傷的HD大鼠模型,這種模型會導致紋狀體萎縮和行為障礙。他們還檢測到UC-MSC中GDNF和VEGF的合成,其中GDNF在HD模型中顯示出神經保護作用,而VEGF以劑量依賴性方式顯示出神經存活特性。
| MSC型 | 細胞 數量 | 通道 數 | 鼠標 模型 | 移植途徑 | 主要發現 | 參考號 |
|---|---|---|---|---|---|---|
| 間充質干細胞 | 20萬 | P3 至 P8 或 P40 至 P50 | R6/2 和 WT 小鼠 | 紋狀體內 | 移植小鼠的短暫行為保留; 高傳代 UC-MSC 移植小鼠的神經病理學 (?) (↓); 營養因子和免疫調節細胞因子的釋放(+),行為缺陷(?) | [ 142 ] |
| 間充質干細胞 | 250,000 | P4 | 3-硝基丙酸損傷小鼠 | 雙側紋狀體 | 移植的MSC的存活和遷移(+); 紋狀體體積和紋狀體的平均樹突長度 (+) | [ 129 ] |
| CM-hAMSC | 50萬 | – | R6/2鼠標 | 腹膜內 | 緊握反射(↑); 運動協調和活動(↑); 紋狀體神經病理學(↑); 對抗炎癥的神經保護 | [ 114 ] |
總體而言,到目前為止,間充質干細胞治療對亨廷頓病動物模型的積極作用已經顯現,體現在形態變化、運動協調性、肌肉力量、神經肌肉肌電活動、皮質相關運動功能和紋狀體相關運動功能上,即使MSC治療并未顯著影響認知能力。
然而,動物研究的數據并沒有完全闡明移植細胞如何調節炎癥細胞因子、趨化因子和神經營養因子的表達。這些問題也應該在臨床試驗之前得到解決。最后,需要強調的是,使用干細胞治療亨廷頓病方案不僅應設計用于治療亨廷頓病的臨床發作,還應用于疾病預防。
干細胞治療帕金森病的細胞療法
帕金森病 (PD) 是由大腦黑質中多巴胺能神經元的喪失引起的。PD更常見于老年患者,影響70歲以上人口的約1-2%。目前的藥物治療包括施用多巴胺前體,可以改善癥狀但不能阻止疾病進展。
最近的研究進展表明細胞替代療法是治療帕金森病患者的一種強大的創新策略。近年來,再生醫學領域取得了巨大進展,基于干細胞的療法旨在替代丟失的多巴胺能神經元。
關于移植,多巴胺替代可以遵循兩種不同的方案:
- 干細胞體外預分化為多巴胺能神經元和
- 植入后體內分化為多巴胺能神經元。
從文獻報道的研究來看,干細胞治療帕金森病的機制可分為兩類修復:
- 直接修復途徑,包括通過移植到神經元的細胞分化和/或整合來增加內源性神經發生。大腦神經回路受損;
- 通過營養因子進行間接修復,因為干細胞表達多種能夠促進局部干細胞神經元分化的神經營養因子。
幾項研究表明,妊娠干細胞移植到帕金森病動物模型后,可以改善功能,并具有神經保護和神經退行性作用。在PD大鼠模型中,已顯示未分化的UC-MSCs阻止了48.4%的多巴胺神經元的退化和56.9%的多巴胺末端的喪失。其他研究人員描述了分化的hUC-MSC移植到多巴胺能神經元的功能益處,能夠減輕運動癥狀。
總而言之,這些發現提供了證據表明必須解決有關細胞療法的許多挑戰和問題:
- 干細胞在宿主大腦中的長期存活;
- 將移植細胞主動整合到局部神經網絡中;
- 副作用風險低;
- 患者大腦中多巴胺的生理釋放。
| MSC型 | 細胞 數量 | 通道 數 | 鼠標模型 | 移植途徑 | 主要發現 | 參考號 |
|---|---|---|---|---|---|---|
| 間充質干細胞 | 2×3.2×10 5 | P3 | PD大鼠模型 | 注射到紋狀體的兩個部位 | 旋轉 不對稱(↑); 多巴胺能分化 (+) | [ 152 ] |
| 人臍帶間充質干細胞 | 1×10 3 | P9 | PD大鼠模型 | 單次立體定向注射 | 旋轉次數(?); 阿撲嗎啡引起的旋轉 (↑) | [ 155 ] |
| 人臍帶間充質干細胞 | 1×10 6 | – | 偏側帕金森病嚙齒動物模型 | 紋狀體注射 | 旋轉次數(?);hUC-MSCs在病變腦組織中 的遷移;分化為神經元樣細胞;hUC-MSCs 歸巢至病變腦組織的能力 | [ 156 ] |
| hUVMSC 衍生的多巴胺能樣細胞 | 1×10 6 | P2-P5 | PD大鼠模型 | 立體定向注射入大鼠紋狀體 | 移植細胞整合到紋狀體中(+);腦組織中的 多巴胺水平(+);橫向旋轉(?);行為缺陷 (↑) | [ 159 ] |
| 人臍帶間充質干細胞 | 1×10 6 | – | PD大鼠模型 | 立體定位注射至黑質 | 阿撲嗎啡引起的旋轉(↑); 改進旋轉;人核特異性抗體(HNA)和酪氨酸羥化酶(TH) 的表達 | [ 160 ] |
| hUVMSC 衍生的多巴胺能樣細胞 | 1×10 5 | P3 | PD大鼠模型 | 立體定向注射入大鼠紋狀體 | 分化的 hUVMSC移植后存活率 (+); 大鼠腦中TH的表達; 阿撲嗎啡引起的旋轉 (↑) | [ 161 ] |
| 人AMSCs | – | – | PD大鼠模型 | 單側 黑上注射 | hAMSCs移植細胞的存活率及hAMSCs對大鼠黑質多巴胺神經元 的保護作用 | [ 164 ] |
| 人AMSCs | 2×4×10 4 | – | PD大鼠模型 | 紋狀體立體定向注射 | 阿撲嗎啡引起的旋轉不對稱性恢復 (↑); hAMSCs 在紋狀體中的存活 | [ 162 ] |
| hp-MSC 衍生的神經表型細胞 | 2×1.5×10 5 | – | PD大鼠模型 | 單側注射至右側內側前腦束 | 運動缺陷的康復; 多巴胺能神經元損失 (?); 保護DA神經元損失; 移植細胞的存活和移植部位 分化為神經元;DLL-1、MASH1和NRTN(+) 的表達;調節受損大腦的免疫反應;神經保護和抑制神經炎癥 | [ 166 ] |
| hUC-MSC 來源的多巴胺能樣神經元 | 1×10 6 | P3 | PD大鼠模型 | 右側紋狀體立體定向注射 | 阿撲嗎啡引起的旋轉(↑); 紋狀體中GFAP、Iba-1、TH、Nurr1、Pitx3、BDNF、TrkB、PI3K、p-Akt、Hsp60、TLR4 和 MyD88的表達 (+); 抑制黑質和紋狀體的神經細胞凋亡; 神經保護和抗神經元炎癥的可能機制 | [ 167 ] |
| WJ-MSCs | 2×1×10 6 | – | PD大鼠模型 | 注射至內側前腦束 | 運動活動(↑); DA和TH濃度(+); | [ 168 ] |
| 試用ID | 階段 | MSC型 | 學習規劃 | 路線 | 數量 | 發現 |
|---|---|---|---|---|---|---|
| NCT03684122 | 主動, 不招聘 | 人臍帶間充質干細胞 | 第一階段 第二階段 | 鞘內和靜脈 注射 | – | 不適用 |
| NCT05691114 | 招聘 | 人干細胞 | 階段1 | Ommaya 儲庫植入側腦室 | 劑量A(5×107細胞/劑量) 劑量B(1.0×108細胞/劑量) 劑量C(1.5×108細胞/劑量)。 | 不適用 |
| NCT04414813 | 完全的 | 人干細胞 | 第一階段早期 | hAESCs 立體定向移植 | 移植5000萬個hAESC | 不適用 |
| NCT05435755 | 尚未 招募 | 人干細胞 | 第一階段早期 | hAESCs精確移植至心室 | 總共將進行6例hAESC移植。 總共5000萬個(2mL)hAESC將 通過Ommaya囊移植到參與者的心室中 (試驗開始時設為第0天)。 隨后,在第一次細胞移植后1個月±5天、2個月±5天、3個月±5天、6個月±5天、9個月±5天進行hAESC心室移植,體積為50每次百萬個細胞(2 mL)。 | 不適用 |
| NCT04876326 | 未知 | 人臍帶間充質干細胞 | 不適用 | 同種異體臍帶間充質干細胞移植 | 脂肪組織來源的自體間充質干細胞植入 ,劑量為2×5000萬個,間隔1個月 | 不適用 |
干細胞治療肌萎縮側索硬化癥
目前再生醫學的進展已提出以細胞為基礎的療法作為治療ALS的新療法。盡管處于臨床轉化的早期階段,但許多臨床前研究已經在動物模型中研究了干細胞的神經保護機制。最有希望用于此目的的是hUC-MSC,它在移植后很容易存活并且具有良好的遷移潛力。
2008年,Rizvanov等人。將轉基因hUC-MSC移植到用作ALS動物模型的轉基因G93A小鼠中。結果表明,移植細胞成功移植到神經組織中,并能分化為內皮細胞,形成新血管。在這份報告中,假設神經保護作用可能來自于新形成的血管輸送各種神經營養因子。
| MSC型 | 細胞數量 | 通道數 | 鼠標 模型 | 移植途徑 | 主要發現 | 參考號 |
|---|---|---|---|---|---|---|
| hUCBC | 100,000 | P4 | ALS小鼠模型 | 鞘內干細胞移植 | 對癥狀前運動表現的有益影響 (↑); 中樞神經系統內有大量移植細胞 | [172] |
| hUCBC | 1×10 6 | – | 轉基因小鼠模型 | 椎管內注射 | 生存時間(+); 運動表現 (↑) 運動神經元損失和 脊髓星形膠質細胞增生 (?); | [174] |
| 表達 VEGF 的 hUCBC | 1×10 6 | – | ALS小鼠模型 | 眶后注射 | 移植到ALS小鼠神經組織中的HUCB整合; 存活時間超過3個月; 修飾后的HUCB細胞 在脊髓實質內遷移、增殖、分化為內皮細胞;神經保護作用 | [175] |
| SPIO標記的hUC-MSC | 4×10 5 | P5 | 成年大鼠模型 | 注射至背側脊髓 | 受損大鼠脊髓內廣泛的人類細胞存活 和植入(+); 促進運動恢復(↑); 移植后在宿主脊髓中的遷移 | [176] |
| SPIO 標記的 hUCBC | 100,000 | – | ALS小鼠模型 | 椎管內注射 | MRI檢測ALS模型中SPIO標記的hUCBC ; 注射細胞無遷移 或脊髓錯位 | [177] |
| hAFC | 100,000 | – | PD大鼠模型 | 搖擺器側腦室移植 | 死亡率(?); 沒有炎癥反應和心室系統的 粗略改變 | [178] |
| 人AMSCs | 1×10 6 | P6-P8 | ALS小鼠模型 | 靜脈給藥 | 延緩疾病進展,延長生存時間(↑); 旋轉桿上的運動性能 (↑) 防止體重減輕 (↑); 神經炎癥(-); 脊髓腹角運動神經元損失(?); 小膠質細胞激活 (?) | [180] |
| 試用ID | 階段 | MSC型 | 學習規劃 | 路線 | 數量 | 發現 |
|---|---|---|---|---|---|---|
| NCT04651855 | 主動, 不招聘 | WJ-MSCs | 第一階段 第二階段 | 鞘內給藥 | 每位入組患者3次 | 不適用 |
| NCT05003921 | 暫停(修改協議) | AlloRx UC-MSCs | 階段1 | 鞘內注射 | 每隔兩個月鞘內注射3次 5000萬個細胞 | 不適用 |
| NCT01494480 | 狀態未知 | 間充質干細胞 | 階段2 | 干細胞移植 | 腰椎穿刺干細胞移植四次,兩次治療間隔3-5天 | 不適用 |
盡管多項研究表明間充質干細胞移植能改善疾病,但人們對間充質干細胞療法產生有益影響的機制并不完全清楚。目前已觀察到多種修復和支持機制,包括細胞替代、營養因子或基因遞送以及免疫調節,有時這些機制會同時出現。間充質干細胞可發揮多種免疫調節作用,這可能是其對ALS有益的原因之一。
間充質干細胞可減少β細胞、T細胞和自然殺傷細胞的增殖,并損害樹突狀細胞的成熟。此外,間充質干細胞還可通過減少:
- β細胞產生抗體;
- 樹突狀細胞和T細胞的活化以及;
- 自然殺傷細胞的分泌來影響免疫細胞的功能。
在中樞神經系統中,間充質干細胞會遷移到炎癥區域,減輕炎癥。在漸凍癥的實驗模型中,間充質干細胞可減輕小膠質細胞的活化并減少星形膠質細胞的增生。
結論和未來展望
以細胞為基礎的療法被認為是治療多種人類神經退行性疾病的一種很有前途的工具。值得注意的是,臨床前研究已經證明,細胞移植在神經領域的功能性益處令人鼓舞,并且已經開展了多項工作,成功地將細胞療法應用于神經退行性疾病。
目前,細胞療法產生有益效果的分子機制與移植細胞產生神經營養因子、增強神經元可塑性、激活局部祖細胞和細胞替代相關(圖3)。

圖3:間充質干細胞移植在神經領域的功能益處的機制可能與其激活局部祖細胞和細胞替代、產生神經營養因子的能力有關,包括成纖維細胞生長因子 (FGF)、表皮生長因子 (EGF)、神經生長因子 (NGF)、腦源性神經營養因子 (BDNF)、膠質細胞源性神經營養因子 (GDNF),增強神經元可塑性和多種因子介導的免疫調節,包括吲哚胺 2、3-雙加氧酶 (IDO)、前列腺素 E 2 (PGE 2 )、一氧化氮(NO)、轉化生長因子(TGF)-β這些限制。
它們潛在的臨床優勢與(1)這些細胞的廣泛可及性有關;(2) 是否有大量可用于移植的資源;(3)缺乏道德關注;(4)移植后無致瘤性;(5)分化成多個譜系的能力。
然而,關于分化神經元產生的功能狀態仍然缺乏令人信服的證據。近年來,這些限制有力地促進了神經膠質細胞分化新方法的開發,最終可以治療有需要的患者,包括通過局部電刺激和基于MSC的基因傳遞策略引導MSC分化為神經元的高度特異性系統。
因此,盡管需要解決一些問題和限制,但干細胞代表了臨床治療疑難雜癥的一種有前途的治療方法,有望延長和改善許多患者的生命。
參考資料:[1]:Bruno, A.; Milillo, C.; Anaclerio, F.; Buccolini, C.; Dell’Elice, A.; Angilletta, I.; Gatta, M.; Ballerini, P.; Antonucci, I. Perinatal Tissue-Derived Stem Cells: An Emerging Therapeutic Strategy for Challenging Neurodegenerative Diseases. Int. J. Mol. Sci. 2024, 25, 976. https://doi.org/10.3390/ijms25020976.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我.



 掃碼添加官方微信
掃碼添加官方微信