隨著生物醫(yī)學(xué)技術(shù)的持續(xù)突破,細(xì)胞療法已實(shí)現(xiàn)從理論探索到臨床轉(zhuǎn)化的跨越,成為一種獨(dú)特的治療模式。其核心優(yōu)勢(shì)在于利用活細(xì)胞作為“活體藥物”,通過(guò)動(dòng)態(tài)執(zhí)行攻擊癌細(xì)胞、促進(jìn)組織再生或恢復(fù)生理功能,在治療機(jī)制上與傳統(tǒng)藥物形成本質(zhì)區(qū)別。根據(jù)細(xì)胞來(lái)源與功能,細(xì)胞療法主要分為免疫細(xì)胞療法、干細(xì)胞療法及其他體細(xì)胞療法;而依據(jù)是否進(jìn)行基因修飾,又可分為基因修飾型與非基因修飾型——這一分類亦是各國(guó)監(jiān)管政策的重要依據(jù)。
10373項(xiàng)臨床試驗(yàn)透視:中國(guó)如何實(shí)現(xiàn)免疫與干細(xì)胞療法的雙輪驅(qū)動(dòng)
在此背景下,2026年2月9日,《Frontiers in Pharmacology》旗下《Sec. Experimental Pharmacology and Drug Discovery》 發(fā)表題為“全球細(xì)胞療法臨床研究全景分析:臨床試驗(yàn)概況、上市產(chǎn)品和監(jiān)管趨勢(shì)”的研究綜述[1]。

該文對(duì)全球10,373項(xiàng)細(xì)胞療法臨床試驗(yàn)的系統(tǒng)梳理顯示:全球研發(fā)格局高度集中,美國(guó)(3,563項(xiàng))、中國(guó)(3,365項(xiàng))和歐洲(1,584項(xiàng))三分天下。值得關(guān)注的是,自2016年起,中國(guó)在年度臨床試驗(yàn)啟動(dòng)數(shù)量上保持全球領(lǐng)先,尤其在CAR-T等免疫細(xì)胞治療領(lǐng)域表現(xiàn)突出,已成為全球細(xì)胞療法研發(fā)的核心引擎之一。
本文基于該綜述的核心數(shù)據(jù),聚焦中國(guó)細(xì)胞療法的臨床研究進(jìn)展。我們將重點(diǎn)分析本土臨床試驗(yàn)概況、上市產(chǎn)品格局及監(jiān)管政策演變,旨在為國(guó)內(nèi)研究人員與從業(yè)者提供一幅清晰的本土發(fā)展圖景,助力把握機(jī)遇、應(yīng)對(duì)挑戰(zhàn)。
一、臨床試驗(yàn)開(kāi)發(fā)概述:規(guī)模躍升與結(jié)構(gòu)優(yōu)化
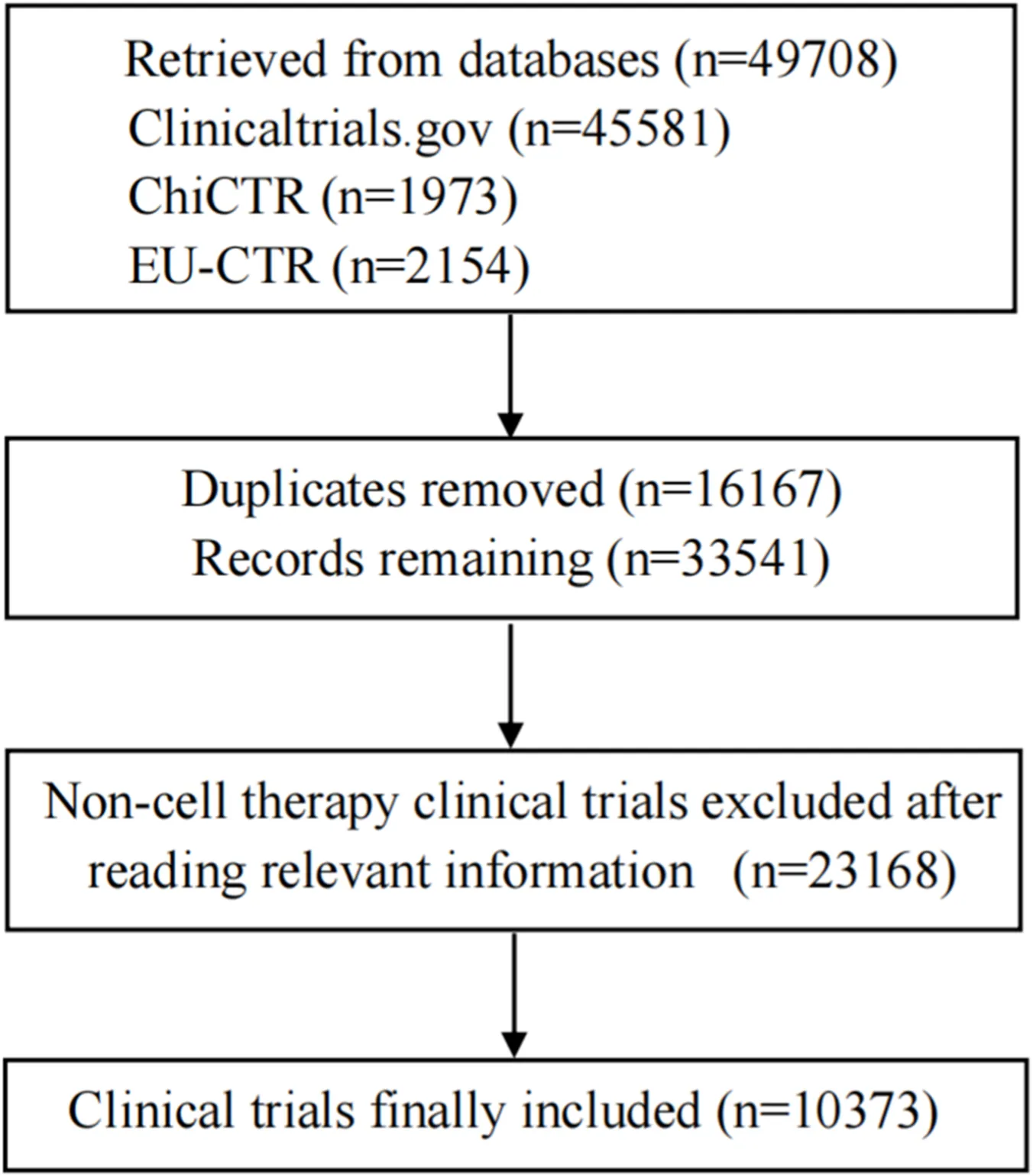
全球細(xì)胞療法臨床試驗(yàn)已形成美、中、歐三足鼎立之勢(shì),中國(guó)后發(fā)優(yōu)勢(shì)顯著。截至2025年10月31日,使用關(guān)鍵詞“細(xì)胞療法”、“T細(xì)胞”、“干細(xì)胞”、“CAR”、“TCR”、“TIL”、“DC”和“NK”在美國(guó)ClinicalTrials.gov、中國(guó)臨床試驗(yàn)注冊(cè)中心(ChiCTR)和歐盟臨床試驗(yàn)注冊(cè)中心(EU-CTR)進(jìn)行檢索,共檢索到32380條記錄。經(jīng)審查試驗(yàn)標(biāo)題和干預(yù)措施描述后,確認(rèn)其中10373項(xiàng)為細(xì)胞療法臨床試驗(yàn)(圖1)。
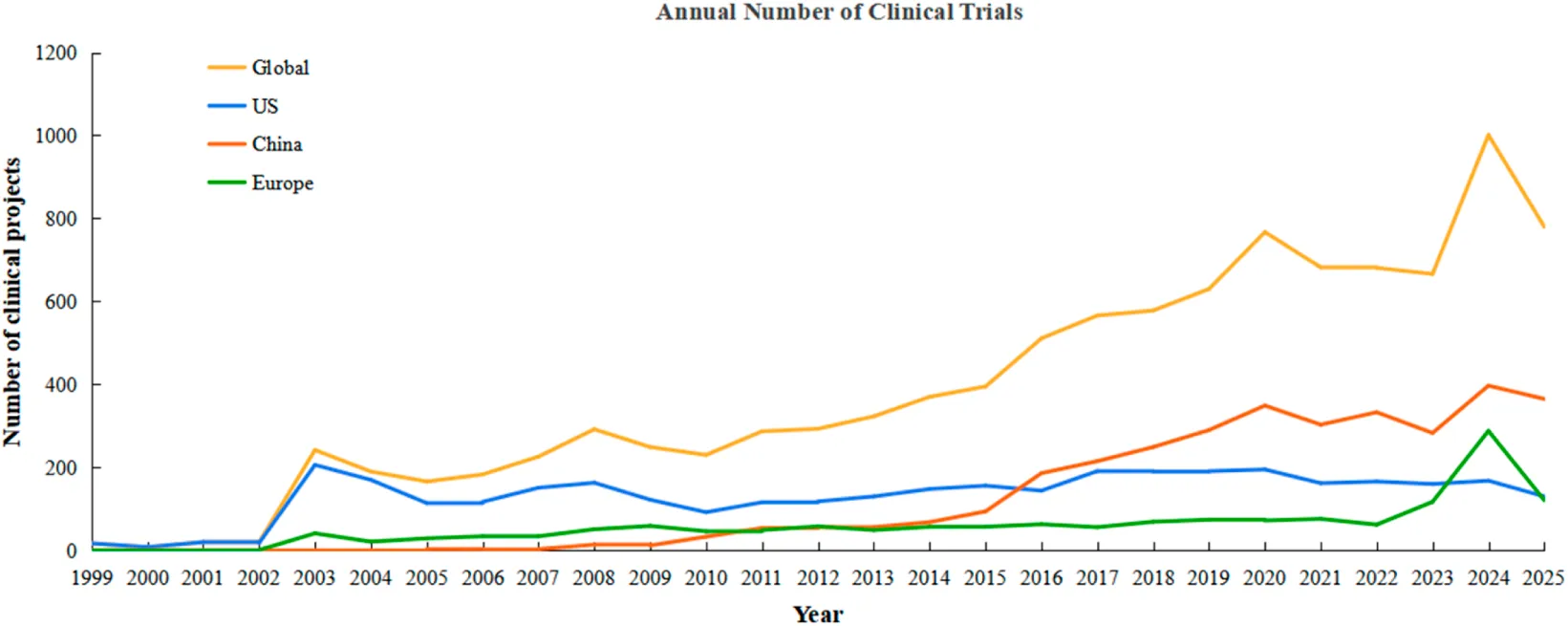
其中,美國(guó)以3,563項(xiàng)(占比34.3%)居首,中國(guó)以3,365項(xiàng)(占比32.4%)緊隨其后,歐洲以1,584項(xiàng)(占比15.3%)位列第三。從發(fā)展歷程觀之,美國(guó)自1999年率先起步,中國(guó)于2005年進(jìn)入該領(lǐng)域,此后項(xiàng)目數(shù)量持續(xù)攀升,并于2016年超越美國(guó),成為全球年度啟動(dòng)臨床試驗(yàn)數(shù)量最多的國(guó)家,展現(xiàn)出強(qiáng)勁的后發(fā)優(yōu)勢(shì)與發(fā)展活力(圖2)。
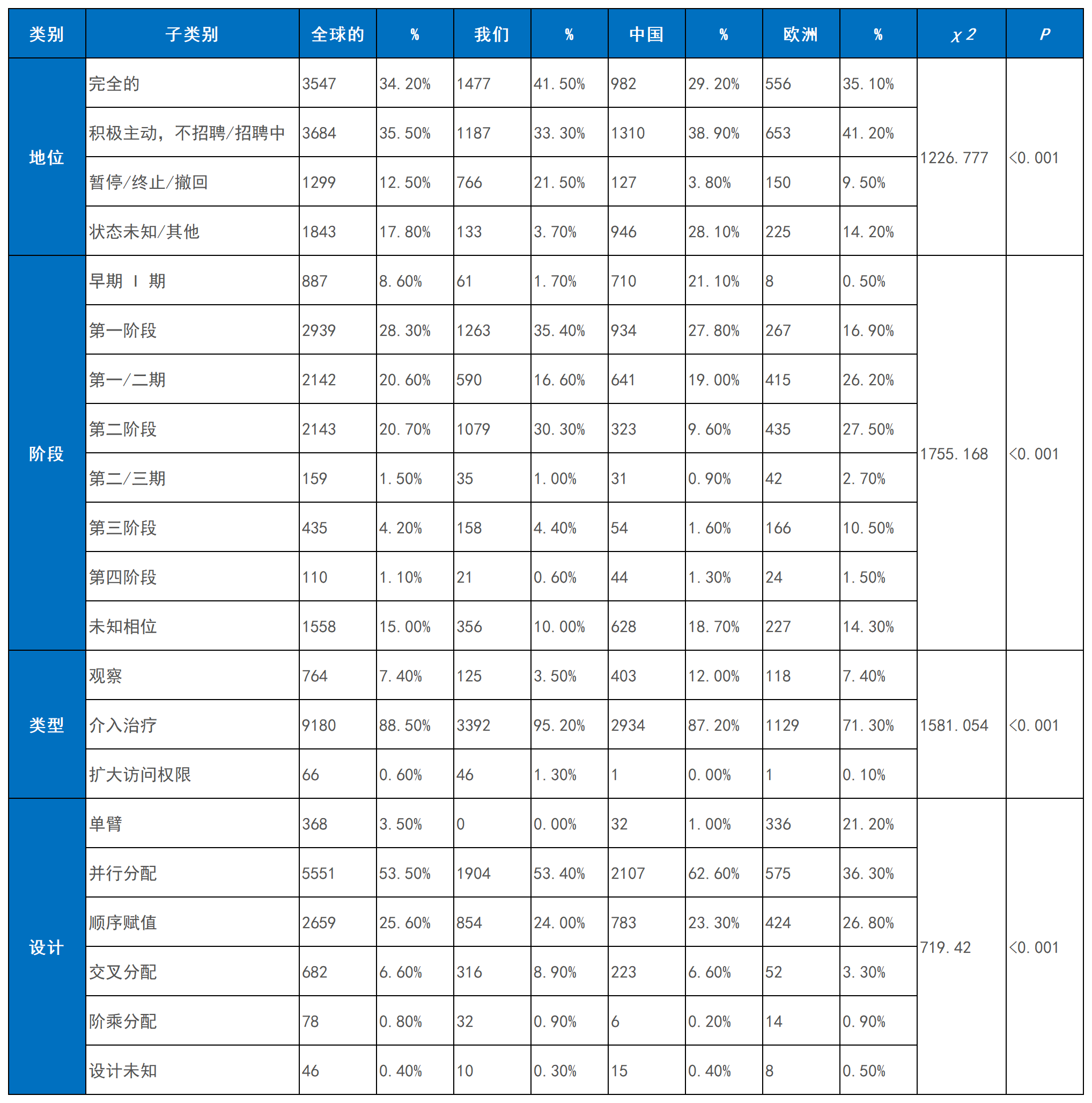
在推進(jìn)狀態(tài)與設(shè)計(jì)質(zhì)量上,主要地區(qū)呈現(xiàn)差異化特征。全球范圍內(nèi),“已完成”研究占比最高,美國(guó)和歐洲的完成率均高于全球平均水平,而中國(guó)相對(duì)較低;但中國(guó)和歐洲“進(jìn)行中”試驗(yàn)比例高于美國(guó),表明后續(xù)產(chǎn)出潛力較大。值得注意的是,中國(guó)臨床試驗(yàn)中止或終止比例顯著低于美國(guó)和歐洲,顯示項(xiàng)目管理與執(zhí)行更具穩(wěn)健性。
從試驗(yàn)階段看,全球I期和II期試驗(yàn)占主導(dǎo)地位,但歐洲III期試驗(yàn)比例(6.4%)顯著高于中國(guó)(1.4%)、美國(guó)(1.7%)及全球平均水平(2.3%),凸顯其在后期研發(fā)的布局深度。在試驗(yàn)設(shè)計(jì)上,美國(guó)干預(yù)性試驗(yàn)比例(88.1%)顯著高于中國(guó)(72.3%)和歐洲(72.2%);歐洲則在平行設(shè)計(jì)和析因設(shè)計(jì)等嚴(yán)謹(jǐn)方法上領(lǐng)先,而中美更傾向于單臂和序貫設(shè)計(jì),設(shè)計(jì)差異具有統(tǒng)計(jì)學(xué)意義(表1)。
二、技術(shù)路徑與適應(yīng)癥布局:免疫與干細(xì)胞雙輪驅(qū)動(dòng)
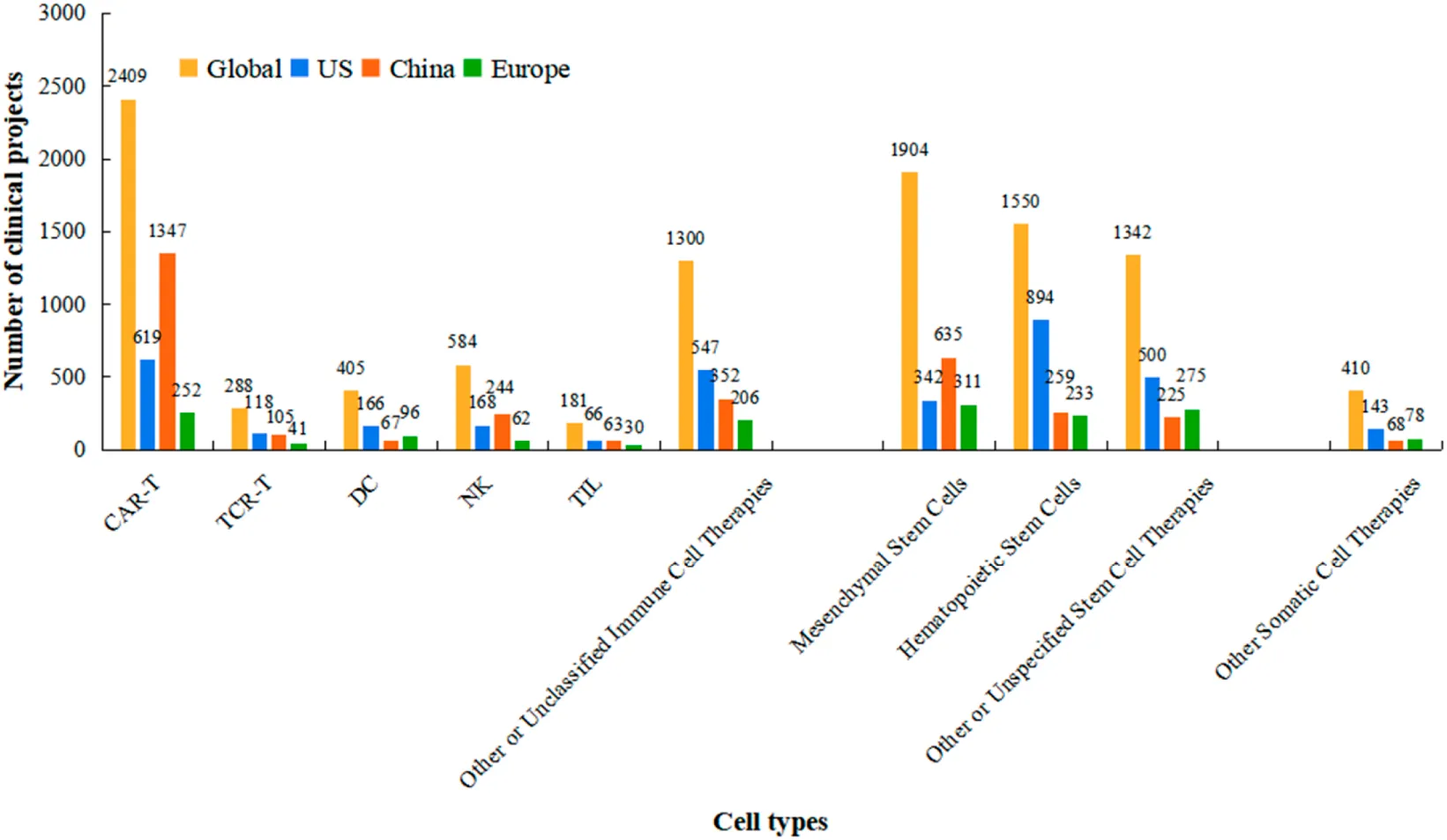
免疫細(xì)胞療法與干細(xì)胞療法并駕齊驅(qū),CAR-T和間充質(zhì)干細(xì)胞成兩大核心支柱。全球范圍內(nèi),免疫細(xì)胞療法(5,167項(xiàng),占49.8%)與干細(xì)胞療法(4,796項(xiàng),占46.2%)構(gòu)成研發(fā)雙核。在細(xì)分領(lǐng)域,CAR-T療法以2,409項(xiàng)試驗(yàn)成為絕對(duì)熱點(diǎn),占免疫細(xì)胞療法的46.6%;間充質(zhì)干細(xì)胞和造血干細(xì)胞分別以1,904項(xiàng)(占干細(xì)胞療法39.7%)和1,550項(xiàng)(占32.3%)引領(lǐng)干細(xì)胞研究。
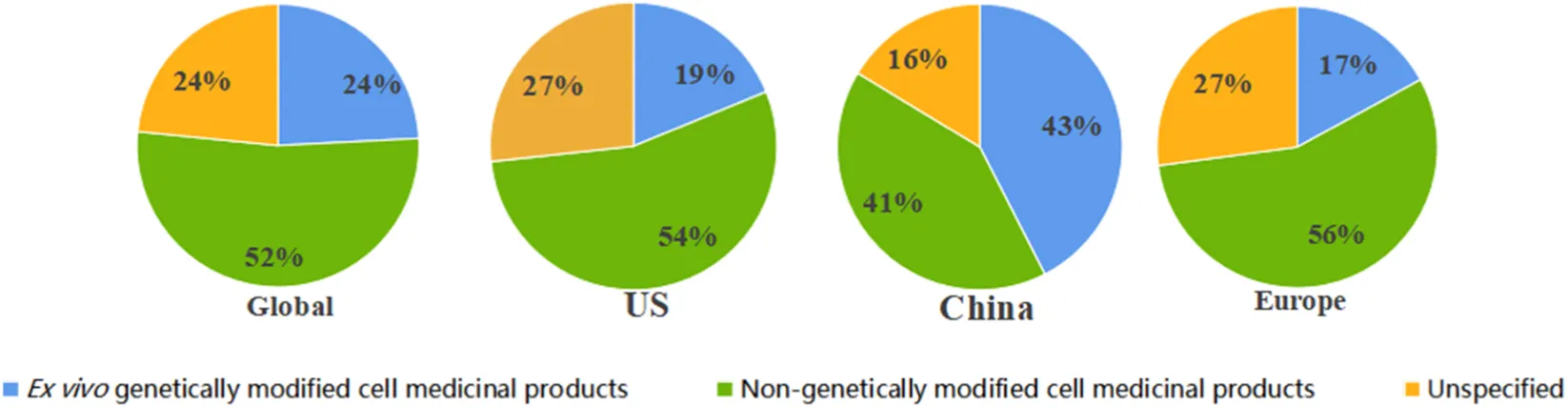
國(guó)家間技術(shù)偏好差異顯著:中國(guó)在CAR-T、NK細(xì)胞和MSC領(lǐng)域試驗(yàn)數(shù)量均超越美國(guó),其中CAR-T研究(1,283項(xiàng))遠(yuǎn)超美國(guó)(671項(xiàng));而美國(guó)在HSC領(lǐng)域(628項(xiàng))則顯著多于中國(guó)(312項(xiàng))(圖3)。 在基因修飾技術(shù)應(yīng)用上,美國(guó)和歐洲非基因修飾項(xiàng)目數(shù)量遠(yuǎn)超基因修飾項(xiàng)目,而中國(guó)兩類項(xiàng)目數(shù)量基本持平,未呈現(xiàn)顯著差異(圖4)。
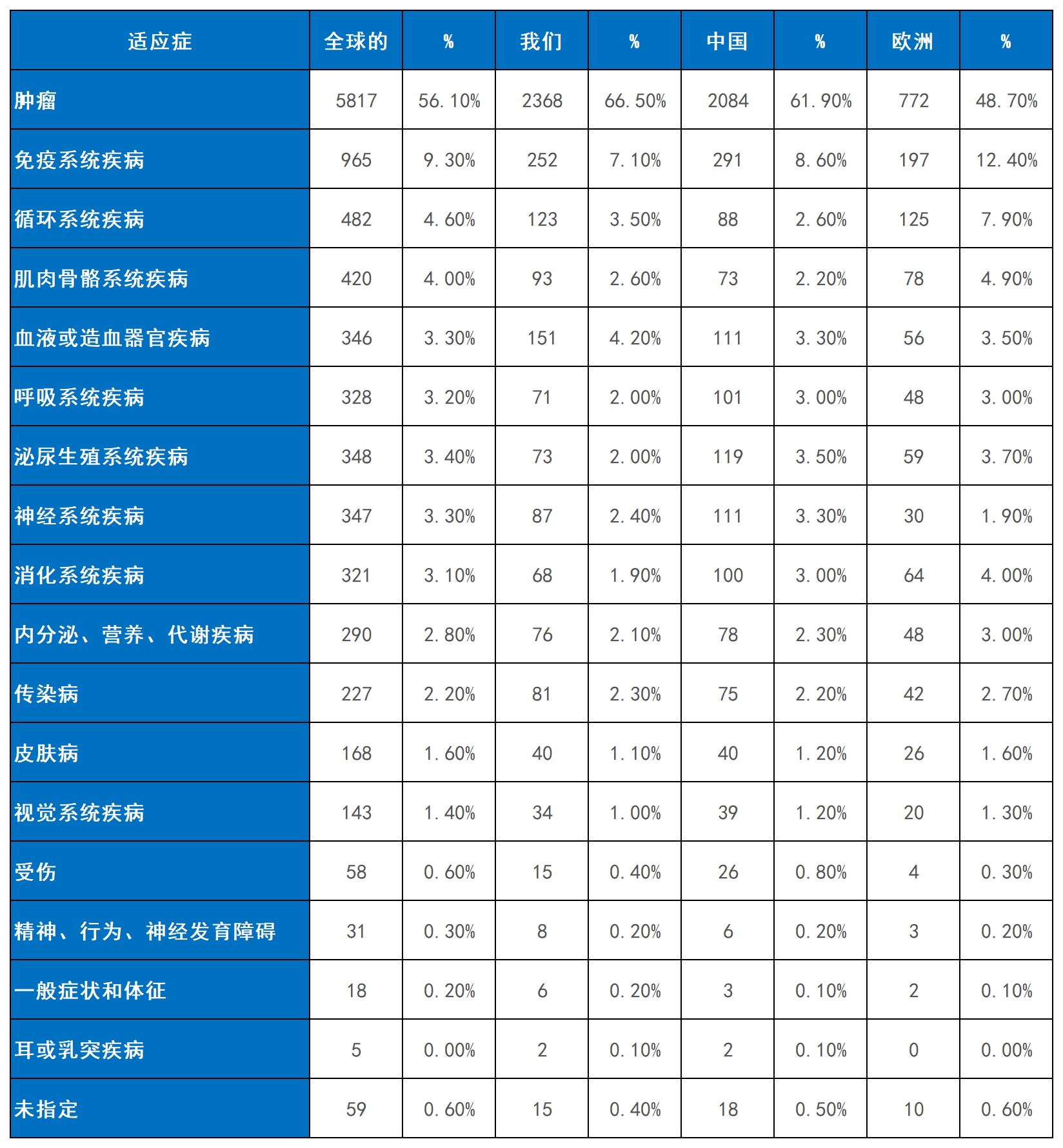
適應(yīng)癥布局方面,腫瘤學(xué)仍為絕對(duì)核心,歐洲則在再生醫(yī)學(xué)和自身免疫病領(lǐng)域形成差異化布局。全球細(xì)胞療法已滲透至全身多個(gè)系統(tǒng),腫瘤學(xué)試驗(yàn)占比56.1%(5,819項(xiàng))。中美對(duì)腫瘤領(lǐng)域聚焦程度更高,分別達(dá)66.5%(2,238項(xiàng))和61.9%(2,204項(xiàng)),顯著高于全球平均水平。相比之下,歐洲疾病分布更為多元,其在免疫系統(tǒng)疾病(14.2% vs 中國(guó)6.9%、美國(guó)7.3%)、循環(huán)系統(tǒng)疾病(5.2% vs 中國(guó)1.6%、美國(guó)2.5%)及肌肉骨骼疾病(3.9%vs中國(guó)1.0%、美國(guó)1.3%)等領(lǐng)域的研究比例均顯著高于中美,體現(xiàn)了其在再生醫(yī)學(xué)領(lǐng)域的戰(zhàn)略側(cè)重(表2)。
三、上市產(chǎn)品格局:從零的突破到多元覆蓋
近年來(lái),中國(guó)細(xì)胞療法產(chǎn)品上市呈現(xiàn)加速態(tài)勢(shì),國(guó)產(chǎn)自主研發(fā)成果斐然。截至2025年底,中國(guó)已批準(zhǔn)8種細(xì)胞治療產(chǎn)品上市(表3)。其中,兩種為中外企業(yè)合作研發(fā):復(fù)星醫(yī)藥與基特藥業(yè)合作的Yescarta?國(guó)產(chǎn)化版本,以及強(qiáng)生旗下楊森制藥與傳奇生物合作的Ciltacabtagene Autoleucel(商品名Carvykti?)。此外,6種為中國(guó)自主研發(fā)產(chǎn)品,含5種CAR-T療法和1種干細(xì)胞療法。
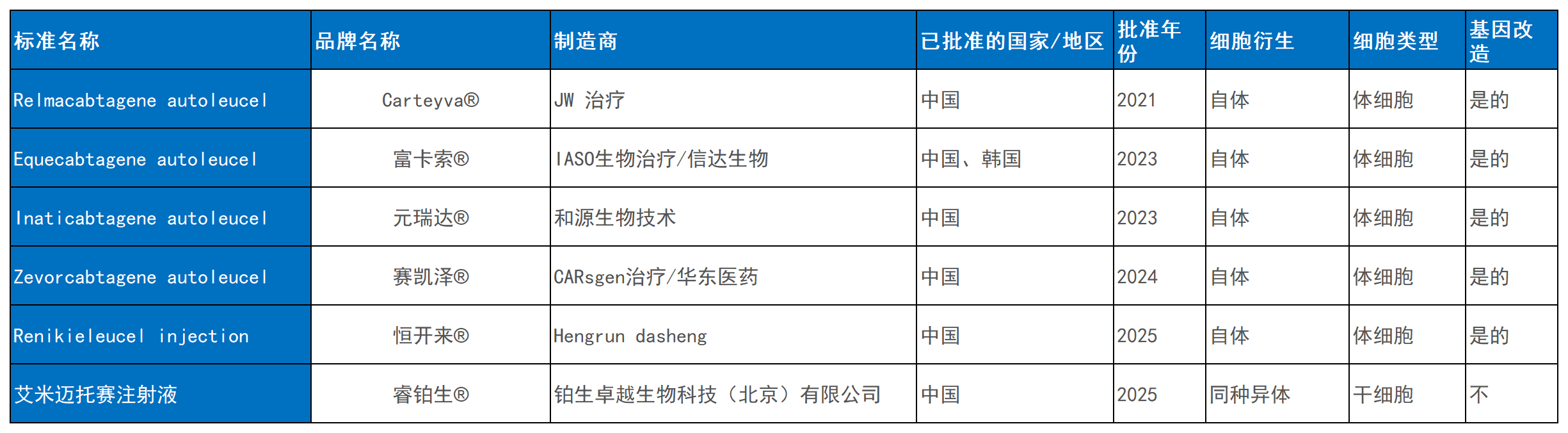
2021年,JW Therapeutics開(kāi)發(fā)的Relmacabtagene autoleucel(商品名Carteyva?)獲批,用于治療某些類型非霍奇金淋巴瘤。作為首個(gè)中國(guó)公司自主研發(fā)并獲批的CAR-T療法,該產(chǎn)品被歸為I類生物制品,其臨床試驗(yàn)顯示出顯著療效,標(biāo)志著中國(guó)在CAR-T治療領(lǐng)域?qū)崿F(xiàn)零的突破。
2023年,兩款CAR-T療法相繼獲批。其一,IASO Bio和信達(dá)生物共同研發(fā)的Equecabtagene Autoleucel,用于治療復(fù)發(fā)/難治性多發(fā)性骨髓瘤,在103例患者中僅1例出現(xiàn)3級(jí)細(xì)胞因子釋放綜合征且經(jīng)治療緩解,展現(xiàn)良好安全性。其二,河北森朗生物研發(fā)的Inaticabtagene Autoleucel(商品名源瑞達(dá)?)獲批,成為國(guó)內(nèi)首個(gè)用于治療白血病的CAR-T產(chǎn)品;在兒童復(fù)發(fā)/難治性B細(xì)胞急性淋巴細(xì)胞白血病臨床試驗(yàn)中,12例患者均達(dá)客觀緩解,其中5例完全緩解;該藥為目前市場(chǎng)上價(jià)格最低的CAR-T療法,并被納入中國(guó)國(guó)家醫(yī)保,費(fèi)用約14萬(wàn)美元,大幅減輕患者經(jīng)濟(jì)負(fù)擔(dān)。
2024年,嘉實(shí)基制藥和華東醫(yī)藥聯(lián)合研發(fā)的澤沃基奧侖賽注射液(商品名賽凱澤?)獲批,用于治療復(fù)發(fā)/難治性多發(fā)性骨髓瘤。對(duì)14例患者的隨訪顯示,中位無(wú)進(jìn)展生存期達(dá)25個(gè)月,中位緩解持續(xù)時(shí)間為24.1個(gè)月,表明該藥具有顯著且持久的療效。另一款CAR-T產(chǎn)品瑞基奧侖賽注射液在非霍奇金淋巴瘤II期臨床試驗(yàn)中表現(xiàn)優(yōu)異:81例患者數(shù)據(jù)顯示,最佳療效時(shí)客觀緩解率達(dá)74.1%,完全緩解率49.4%,中位緩解持續(xù)時(shí)間為339天,中位無(wú)進(jìn)展生存期為176天,且安全性可控。
除免疫細(xì)胞療法外,干細(xì)胞療法亦取得重要進(jìn)展。睿鉑勝?注射液(商品名艾米邁托賽注射液)作為國(guó)內(nèi)首個(gè)獲批的間充質(zhì)干細(xì)胞療法,用于治療激素?zé)o效的急性移植物抗宿主病。多中心隨機(jī)對(duì)照試驗(yàn)顯示,治療組第28天客觀緩解率顯著高于對(duì)照組(71.9% vs46.7%),且不良反應(yīng)無(wú)顯著差異。
值得注意的是,2025年12月,國(guó)家醫(yī)保局發(fā)布《商業(yè)健康保險(xiǎn)創(chuàng)新藥品目錄(2025年)》,首次將5款已上市的CAR-T藥物納入商保報(bào)銷范圍。此舉標(biāo)志著細(xì)胞療法支付體系取得重大突破,為提升患者可及性打開(kāi)新通道。
四、監(jiān)管框架與政策演變:雙軌驅(qū)動(dòng)與加速審評(píng)
中國(guó)國(guó)家藥品監(jiān)督管理局已逐步構(gòu)建起一套兼具國(guó)際規(guī)范與本土特色的細(xì)胞治療產(chǎn)品監(jiān)管體系。其核心特征在于“雙軌制”管理模式,即由藥品監(jiān)管機(jī)構(gòu)和衛(wèi)生行政部門(mén)并行監(jiān)管,將細(xì)胞療法劃分為“藥品”和“醫(yī)療技術(shù)”兩條路徑進(jìn)行管理。
作為藥品開(kāi)發(fā)時(shí),細(xì)胞治療產(chǎn)品須嚴(yán)格遵守《藥品注冊(cè)管理辦法》等相關(guān)法規(guī),注冊(cè)為生物制品;基因改造產(chǎn)品還需遵循特定的非臨床研究技術(shù)指導(dǎo)原則。作為醫(yī)療技術(shù)途徑,則主要適用于醫(yī)療機(jī)構(gòu)內(nèi)開(kāi)展的探索性、非商業(yè)性臨床研究,必須通過(guò)嚴(yán)格的學(xué)術(shù)和倫理審查,特別是干細(xì)胞臨床研究需遵循《干細(xì)胞臨床研究管理辦法(試行)》。值得注意的是,監(jiān)管層鼓勵(lì)在醫(yī)療技術(shù)途徑中初步驗(yàn)證安全有效性的項(xiàng)目適時(shí)轉(zhuǎn)入藥品開(kāi)發(fā)軌道以實(shí)現(xiàn)商業(yè)化上市,從而打通從臨床探索到產(chǎn)品轉(zhuǎn)化的通道。
在審批機(jī)制與市場(chǎng)準(zhǔn)入方面,NMPA通過(guò)加入國(guó)際人用藥品注冊(cè)技術(shù)協(xié)調(diào)會(huì),推動(dòng)藥品審評(píng)標(biāo)準(zhǔn)與國(guó)際全面接軌。同時(shí),為加速滿足臨床急需,NMPA設(shè)立了“突破性療法認(rèn)定”、“附條件批準(zhǔn)”和“優(yōu)先審評(píng)”等快速審批程序,顯著縮短創(chuàng)新細(xì)胞療法的上市周期。2025年9月,國(guó)家藥監(jiān)局發(fā)布《關(guān)于優(yōu)化創(chuàng)新藥臨床試驗(yàn)審評(píng)審批有關(guān)事項(xiàng)的公告》,進(jìn)一步壓縮審批時(shí)限。
在市場(chǎng)端,國(guó)家醫(yī)保談判政策通過(guò)“以價(jià)換量”策略,大幅降低已上市細(xì)胞療法價(jià)格,顯著提升患者用藥可及性。2025年出臺(tái)的《支持創(chuàng)新藥高質(zhì)量發(fā)展的若干措施》明確提出“三除外”政策——不納入醫(yī)保自費(fèi)率指標(biāo)、不強(qiáng)制用集采低價(jià)藥替代、相關(guān)病例可不納入病種打包付費(fèi)范圍,為醫(yī)院使用高價(jià)創(chuàng)新藥掃清制度障礙。
這一系列政策組合拳,雖然在短期內(nèi)壓縮了企業(yè)的利潤(rùn)空間,但也有效倒逼企業(yè)通過(guò)持續(xù)技術(shù)創(chuàng)新與工藝優(yōu)化來(lái)降低成本、提升效率,為行業(yè)長(zhǎng)期健康發(fā)展注入了內(nèi)生動(dòng)力。
結(jié)語(yǔ): 中國(guó)細(xì)胞療法歷經(jīng)二十年發(fā)展,從跟跑到并跑乃至局部領(lǐng)跑,已在臨床試驗(yàn)規(guī)模、技術(shù)布局多元性、產(chǎn)品上市速度及監(jiān)管體系完善度等方面取得長(zhǎng)足進(jìn)步。展望未來(lái),隨著政策紅利持續(xù)釋放、技術(shù)創(chuàng)新不斷突破、支付體系逐步完善,中國(guó)有望從細(xì)胞療法研發(fā)大國(guó)邁向創(chuàng)新強(qiáng)國(guó),為全球患者提供更多元、可及的治療選擇。
參考資料:
[1]:Wang M, Zhou T, Liu S, Xiang W, Xie K, Zhang X, Hu W, Fang M, Zhang Z, Chen M, Wang X and Wu J (2026) Global Panoramic analysis of clinical research in cell therapy: clinical trial landscape, marketed products, and regulatory trends. Front. Pharmacol. 17:1715984. doi: 10.3389/fphar.2026.1715984
免責(zé)說(shuō)明:本文僅用于傳播科普知識(shí),分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問(wèn),請(qǐng)隨時(shí)聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信