Meta描述:神經(jīng)干細胞(NSC)與間充質(zhì)干細胞(MSC)如何協(xié)同促進神經(jīng)再生?本文基于《細胞》雜志最新綜述,系統(tǒng)解析NSC與MSC的生物學(xué)特性、相互作用機制(Notch信號、旁分泌)、聯(lián)合移植策略及臨床轉(zhuǎn)化挑戰(zhàn),附對比表格與未來方向。
引言:神經(jīng)再生的挑戰(zhàn)與干細胞聯(lián)合策略
神經(jīng)系統(tǒng)疾病和損傷(如腦卒中、帕金森病、脊髓損傷)是再生醫(yī)學(xué)領(lǐng)域最難攻克的堡壘之一。成年中樞神經(jīng)系統(tǒng)(CNS)內(nèi)源性修復(fù)能力極其有限,主要因為:
- 神經(jīng)干細胞(NSC)數(shù)量稀少且多處于靜息狀態(tài)
- 損傷后微環(huán)境充滿炎癥因子和抑制再生的分子
- 成熟神經(jīng)元無法分裂替代
干細胞移植為神經(jīng)再生帶來了希望。其中,神經(jīng)干細胞(NSC) 因其能夠分化為功能性神經(jīng)元和膠質(zhì)細胞,被視為最直接的細胞替代來源;而間充質(zhì)干細胞(MSC) 則憑借免疫調(diào)節(jié)、旁分泌支持和低免疫原性,成為改善損傷微環(huán)境的理想輔助細胞。
神經(jīng)干細胞(NSC)與間充質(zhì)干細胞(MSC)協(xié)同治療神經(jīng)系統(tǒng)疾病:機制、策略與前景(2025年綜述解讀)
近期,國際期刊雜志《細胞》發(fā)表了一篇神經(jīng)干細胞 (NSC) 和間充質(zhì)干細胞 (MSC) 的相互作用作為大腦研究和神經(jīng)再生的一種有前途的方法的綜述,在這篇綜述中,我們討論了與雙邊MSC-NSC相互作用、環(huán)境條件下MSC向神經(jīng)細胞(嵴衍生細胞亞群)分化、生物支架或通過重建與NSC共培養(yǎng)相關(guān)的各種治療策略和激活機制。

一、間充質(zhì)干細胞和神經(jīng)干細胞合作的潛在能力
間充質(zhì)干細胞可以遷移到大腦受損部位,產(chǎn)生神經(jīng)保護和血管保護作用。此外,它們可以促進受損大腦皮層的細胞再生,而它們的分泌組對腦外傷后的神經(jīng)元具有有利的影響。
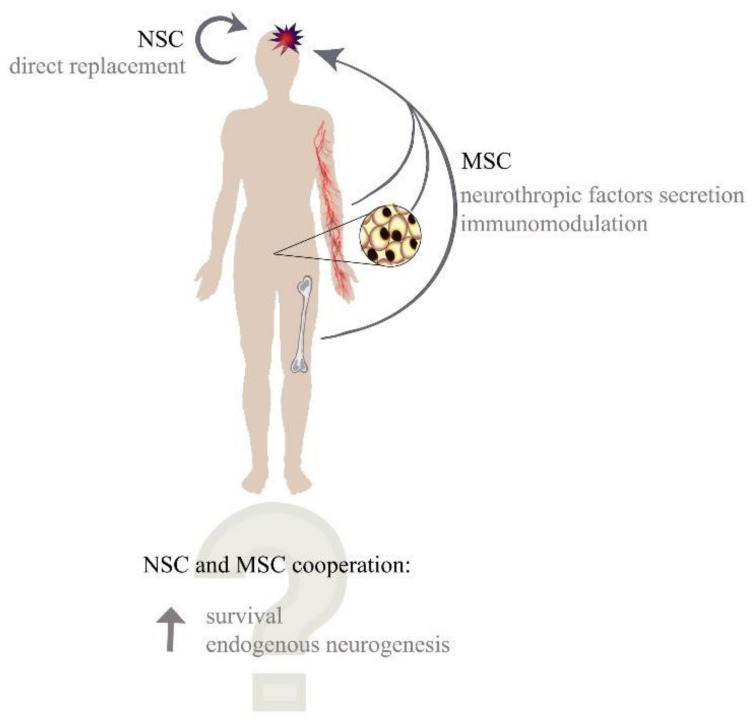
然而,關(guān)于MSC是否可以與NSC或其生態(tài)位相互作用以提高NSC分化為成熟和功能性神經(jīng)元的再生能力的研究仍在進行中。間充質(zhì)干細胞和神經(jīng)干細胞單獨在中樞神經(jīng)系統(tǒng)中的再生潛力較低,但它們獨特的功能可以建立協(xié)同關(guān)系,這對于增強治療效果至關(guān)重要。神經(jīng)干細胞移植可以提供新的神經(jīng)祖細胞,而MSC可以通過佐劑效應(yīng)和細胞間接觸來免疫微環(huán)境并支持新生成的神經(jīng)母細胞的存活和分化(圖1)。
二、神經(jīng)干細胞到底是什么?從分子標志物到來源困境
很多人把NSC和NPC混著用,但嚴格來說不一樣。真正的NSC有三個特征:一是可以對稱分裂(自我擴增)和不對稱分裂(產(chǎn)生一個NSC和一個NPC);二是可以分化為三大神經(jīng)譜系(神經(jīng)元、星形膠質(zhì)細胞、少突膠質(zhì)細胞);三是在連續(xù)傳代后仍能保持多向分化能力。
分子標志物上,目前公認的是Sox2、Nestin、Pax6。Sox2是維持干性的核心轉(zhuǎn)錄因子,敲掉它NSC就會分化。Nestin是中間絲蛋白,在神經(jīng)前體細胞中高表達,成熟神經(jīng)元里沒有。Pax6主要調(diào)控皮層發(fā)育,在成人SVZ的NSC中也表達。
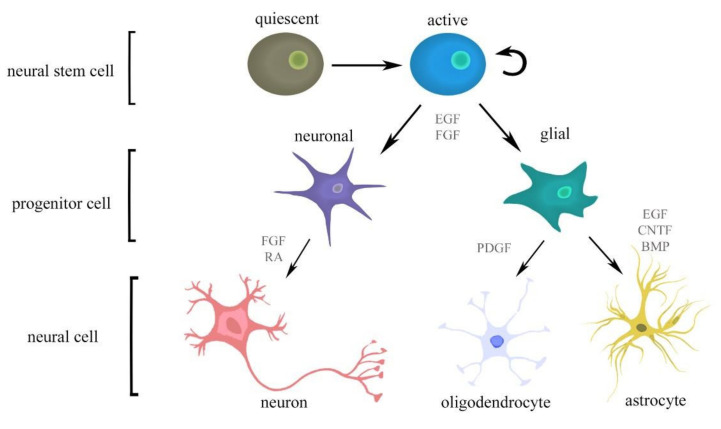
但NSC在體內(nèi)的狀態(tài)不是一成不變的。它有兩種狀態(tài):活躍(active)和靜息(quiescent)。靜息的NSC高表達BMP信號通路相關(guān)基因,低表達細胞周期蛋白。當(dāng)受到VEGF、BDNF、Wnt、Shh等信號刺激時,靜息NSC會退出靜息期,進入細胞周期。這個“喚醒”過程是神經(jīng)發(fā)生的第一限速步驟(圖2)。
NSC的來源主要有四種,各有各的爛攤子:
第一,胎兒/胚胎來源。這是最經(jīng)典的方式。從流產(chǎn)胎兒或胚胎小鼠的腦組織中分離。優(yōu)點是這些細胞是真的、活的NSC,分化潛能最高。缺點是倫理爭議越來越大——美國NIH對胎兒組織研究已經(jīng)有嚴格限制,國內(nèi)雖然沒那么嚴,但公眾輿論壓力也在增大。而且一個胎兒的量也有限,不可能工業(yè)化生產(chǎn)。
第二,成體腦組織來源。從SVZ或DG取一小塊,體外擴增。優(yōu)點是可以自體移植,沒有免疫排斥。缺點是要開顱取腦組織——為了取細胞先切一刀,這種侵入性操作對患者來說代價太大。而且隨著年齡增長,成人NSC的數(shù)量和功能都在下降。60歲以上患者取自己的NSC,擴增出來的細胞活力遠不如年輕人。
第三,多能干細胞分化。用ESC或iPSC定向誘導(dǎo)為NSC。這是目前工業(yè)化生產(chǎn)最有希望的方向。日本京都大學(xué)已經(jīng)用iPSC-NSC治療脊髓損傷,2024年又報了帕金森病的I/II期結(jié)果(就是之前那篇Nature文章)。但問題也很實在:誘導(dǎo)效率不穩(wěn)定(有的批次90%以上陽性,有的不到50%)、殘留未分化iPSC有致瘤風(fēng)險(雖然可以通過流式分選或自殺基因清除)、成本極高(一個批次幾十萬人民幣)。
第四,直接重編程(iNSC)。用轉(zhuǎn)錄因子(比如Sox2、Pax6、Brn2)直接將成纖維細胞轉(zhuǎn)分化為NSC,繞過iPSC中間階段。2011年就有文章做了,但效率低得可憐,而且得到的細胞更像NPC而不是真正的NSC。這些年進展不大。
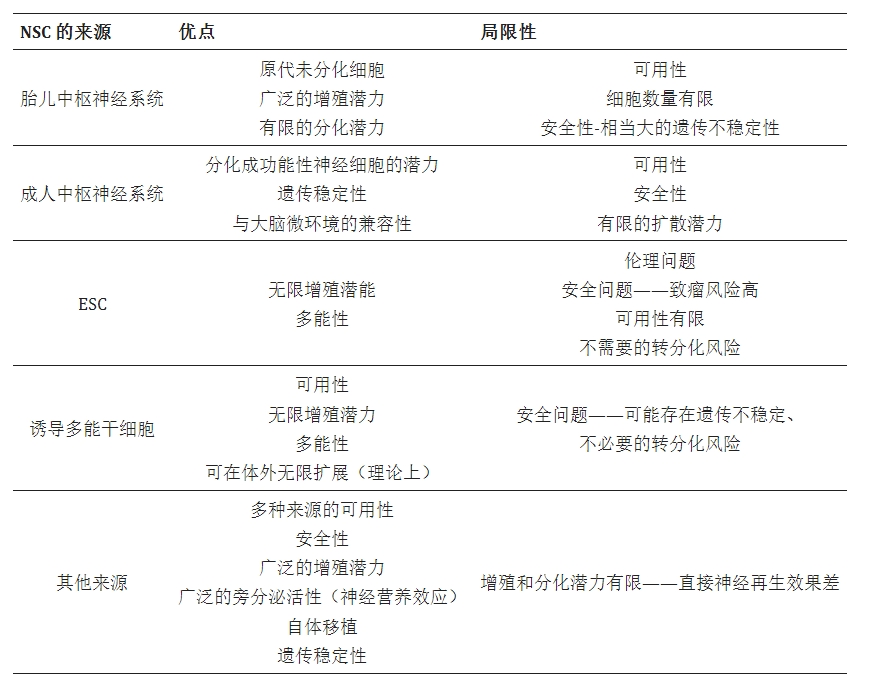
目前,在ClinicalTrials.gov上注冊的臨床研究多達74項。人們對應(yīng)用這些干細胞治療神經(jīng)系統(tǒng)疾病越來越感興趣,包括缺血性中風(fēng)、帕金森病和阿爾茨海默病、肌萎縮側(cè)索硬化癥 (ALS) 或脊髓損傷 (SCI)。由于內(nèi)源性神經(jīng)干細胞的恢復(fù)能力無效,因此對多種來源的NSC進行了測試,包括胎兒和成人CNS衍生的NSC、來自多能干細胞的神經(jīng)祖細胞以及非神經(jīng)干細胞:表格1)。
到目前為止,尚未選擇理想的可用來源。每個來源都有其優(yōu)點和缺點,下表總結(jié)了這些優(yōu)點和缺點。
三、MSC在神經(jīng)修復(fù)中的角色:不是分化,是“當(dāng)保姆”
MSC在神經(jīng)系統(tǒng)疾病中的研究遠遠多于NSC,注冊的臨床試驗數(shù)量是NSC的好幾倍。但MSC的作用機制跟大眾想象的不一樣——它不是靠變成神經(jīng)元來修復(fù)大腦。
2000年代初期確實有一批文章聲稱MSC可以在腦內(nèi)轉(zhuǎn)分化為神經(jīng)元,表達NeuN、MAP2等神經(jīng)元標志物。但后來幾個實驗室用更嚴格的譜系追蹤(比如用Cre-Lox系統(tǒng)標記MSC然后移植)發(fā)現(xiàn),那些所謂的“神經(jīng)元”要么是細胞融合形成的雜合細胞,要么是自發(fā)熒光假陽性,要么是MSC內(nèi)吞了周圍死亡神經(jīng)元的碎片。目前的主流共識是:MSC在體內(nèi)基本不轉(zhuǎn)分化為功能性神經(jīng)元。即使有,比例也低到?jīng)]有臨床意義。
那MSC憑什么治腦病?靠三條腿:
第一條,免疫調(diào)節(jié)。MSC不表達MHC-II類分子(HLA-DR陰性),也不表達CD80、CD86等共刺激分子,所以不會激活CD4+ T細胞。更關(guān)鍵的是,MSC能主動抑制免疫反應(yīng)。機制包括:分泌IDO(indoleamine 2,3-dioxygenase)消耗色氨酸,導(dǎo)致T細胞周期阻滯;分泌PGE2、TGF-β、IL-10等抗炎因子;直接接觸誘導(dǎo)Treg生成;把巨噬細胞從促炎的M1型掰成抗炎的M2型。在脊髓損傷或腦卒中的動物模型中,移植MSC后,損傷部位的IFN-γ、TNF-α、IL-1β顯著下降,IL-10上升。
第二條,旁分泌營養(yǎng)支持。MSC分泌一堆神經(jīng)營養(yǎng)因子:BDNF(促進神經(jīng)元存活和突觸可塑性)、GDNF(對多巴胺能神經(jīng)元尤其重要)、NGF、NT-3、bFGF、VEGF(促血管新生)、HGF(抗凋亡)。這些因子可以保護瀕死的神經(jīng)元,促進軸突生長,誘導(dǎo)血管再生。一個經(jīng)典的實驗是:把MSC的條件培養(yǎng)基(就是養(yǎng)過MSC的培養(yǎng)基,里面都是它們分泌的東西)打進中風(fēng)大鼠的腦子里,效果跟打細胞本身差不多。這說明旁分泌是MSC的主要作用通路。
第三條,外泌體(EVs)介導(dǎo)的遠程調(diào)控。最近五年的熱點。MSC分泌的外泌體(30-150nm的小囊泡)里面裝了miRNA、mRNA、蛋白質(zhì),可以被受體細胞內(nèi)吞,從而調(diào)控受體細胞的基因表達。比如MSC外泌體里的miR-133b可以促進神經(jīng)突生長,miR-17-92簇可以促進少突膠質(zhì)前體細胞增殖和髓鞘形成。外泌體的優(yōu)勢是:沒有活細胞,所以不會有致瘤或栓塞風(fēng)險;可以凍干保存,不用液氮;可以通過表面修飾實現(xiàn)靶向遞送。目前已經(jīng)有一些臨床前研究用MSC外泌體治療中風(fēng)、脊髓損傷、帕金森病,結(jié)果跟用MSC本身差不多。將來很可能MSC外泌體會取代MSC,變成“無細胞治療”的主力。
但MSC也不是沒有副作用。靜脈輸注MSC時,由于細胞體積較大(直徑15-30μm),大部分會被肺部毛細血管床截留,只有一小部分能到達腦部。這種“肺首過效應(yīng)”本身不是問題——被截留在肺部的MSC反而可以分泌抗炎因子,通過全身循環(huán)間接影響腦部。但有研究報道,高劑量靜脈輸注MSC可能引起微栓塞,尤其是在肺功能不好的患者身上。還有研究擔(dān)心MSC在某些條件下可能促進腫瘤生長(比如給荷瘤小鼠打MSC,腫瘤長得更快),但這個爭議很大,不同實驗室結(jié)果相反。2024年FDA批準的Ryoncil(MSC治療兒童GVHD)是基于幾十個臨床試驗的數(shù)據(jù),沒有發(fā)現(xiàn)明顯的促瘤信號。所以風(fēng)險可能被夸大了,但也不是零。
四、MSC和NSC怎么互動?分子機制層面的事
這篇綜述最有價值的部分,是系統(tǒng)梳理了MSC和NSC之間的相互作用機制,而不是只說“1+1>2”這種空話。
第一個機制:MSC通過Notch信號維持NSC的干性。
Notch信號在發(fā)育神經(jīng)生物學(xué)里是老面孔了。當(dāng)Notch受體(Notch1-4)被配體(Jagged1/2、DLL1/3/4)激活后,Notch受體會被γ-secretase切割,釋放胞內(nèi)段NICD(Notch intracellular domain)。NICD進入細胞核,與轉(zhuǎn)錄因子RBP-J結(jié)合,激活下游靶基因(如Hes1、Hes5)。Hes1和Hes5是堿性螺旋-環(huán)-螺旋轉(zhuǎn)錄因子,它們抑制 proneural 基因(如Ascl1、Neurogenin)的表達,從而抑制分化、維持干性。
MSC表面表達Jagged1和DLL1。當(dāng)NSC和MSC共培養(yǎng)時,MSC通過直接接觸激活NSC的Notch信號。有實驗顯示,在沒有EGF和bFGF的培養(yǎng)基里,單獨培養(yǎng)的NSC很快就會分化——細胞變得扁平,Nestin下調(diào),βIII-tubulin(神經(jīng)元標志物)上調(diào)。但跟MSC共培養(yǎng)的NSC,即使沒有EGF/bFGF,仍然維持Nestin陽性,Hes1和Hes5的表達水平跟有EGF/bFGF時差不多。這說明MSC可以直接替代外源性生長因子的作用,通過Notch信號維持NSC的未分化狀態(tài)。
第二個機制:MSC通過旁分泌因子促進NSC的存活和神經(jīng)元分化。
這個聽起來跟上面有點矛盾——MSC既維持NSC的干性,又促進分化?其實不矛盾,取決于微環(huán)境和時間點。
在NSC剛移植進去的時候,MSC分泌的BDNF、GDNF、HGF可以抑制凋亡通路。具體的分子通路:BDNF結(jié)合TrkB受體,激活PI3K/Akt通路,Akt磷酸化后抑制Bad和caspase-9,從而阻斷線粒體凋亡途徑。HGF結(jié)合c-Met受體,同樣激活PI3K/Akt,還激活MAPK/ERK通路,促進細胞增殖。在氧-葡萄糖剝奪(OGD)模型中(模擬缺血性中風(fēng)),與MSC共培養(yǎng)的NSC,凋亡細胞比例比單獨培養(yǎng)的NSC低40-60%。
而在需要分化的時候,MSC分泌的BDNF和GDNF又可以促進NSC向神經(jīng)元方向分化。具體的機制涉及:BDNF/TrkB激活下游的Ras-MAPK通路,磷酸化CREB,CREB進入細胞核促進 proneural 基因(如NeuroD1)的表達。有研究用微流控芯片做共培養(yǎng),發(fā)現(xiàn)NSC跟MSC共培養(yǎng)7天后,βIII-tubulin陽性的神經(jīng)元比例比對照組高出2倍以上,而且這些神經(jīng)元有動作電位(電生理記錄證實)。
第三個機制:MSC通過免疫調(diào)節(jié)為NSC移植創(chuàng)造“免疫豁免”微環(huán)境。
這是聯(lián)合移植最直觀的好處。異體NSC移植后,宿主的免疫系統(tǒng)會攻擊它們——CD8+ T細胞會直接殺傷,巨噬細胞會吞噬。MSC可以通過前面說的IDO、PGE2、TGF-β等機制抑制T細胞活化,把巨噬細胞掰成M2型,減少IFN-γ和TNF-α的釋放。這樣一來,NSC的存活率可以大幅提升。
有一個經(jīng)典的動物實驗:在脊髓損傷大鼠模型中,單獨移植NSC的組,8周后存活的NSC只有移植量的5-10%。而NSC+MSC聯(lián)合移植的組,存活率提升到30-40%。而且聯(lián)合移植組中,NSC分化為神經(jīng)元的比例也更高——可能是因為MSC分泌的BDNF、GDNF提供了分化信號。
第四個機制:NSC反過來也能影響MSC——誘導(dǎo)MSC向神經(jīng)譜系分化。
這個方向的證據(jù)比前三個弱一些,但確實有報道。有研究發(fā)現(xiàn),NSC分泌的Shh(Sonic hedgehog)可以誘導(dǎo)MSC表達神經(jīng)前體細胞標志物(Nestin、Pax6)。還有研究用transwell共培養(yǎng)(不讓細胞直接接觸,只共享培養(yǎng)基),發(fā)現(xiàn)NSC的條件培養(yǎng)基也能讓MSC表達一些神經(jīng)元樣的標志物。但問題是,這些MSC到底有沒有變成真正的功能性神經(jīng)元?目前沒有電生理證據(jù)。大多數(shù)研究者認為,即使MSC被誘導(dǎo)表達一些神經(jīng)標志物,它們也很難形成動作電位和突觸。所以這條機制在聯(lián)合移植中的貢獻可能不大,主要貢獻還是MSC支持NSC,而不是反過來。
五、總結(jié)
干細胞與伴生/支持細胞之間的相互作用對平衡和組織再生至關(guān)重要。在許多器官中,間充質(zhì)干細胞維持干細胞的存活和轉(zhuǎn)運增殖細胞(TAC)的增殖,然后分化成目標細胞類型。雖然證據(jù)尚不充分,但間質(zhì)作為生態(tài)位的組成部分,似乎在靜止的間充質(zhì)干細胞與增殖、分化和從細胞龕遷移的祖細胞之間的平衡中發(fā)揮作用。
神經(jīng)干細胞和間充質(zhì)干細胞之間也存在同樣的相互作用。
- 由于神經(jīng)干細胞可能是所有神經(jīng)細胞類型的無限來源,而間充質(zhì)干細胞則顯示出高度的旁分泌活性,因此將它們聯(lián)合用于治療神經(jīng)系統(tǒng)疾病似乎極具前景。
根據(jù)現(xiàn)有的科學(xué)文獻,間充質(zhì)干細胞和神經(jīng)干細胞的結(jié)合似乎代表了一個有前途的治療前景(圖4)。
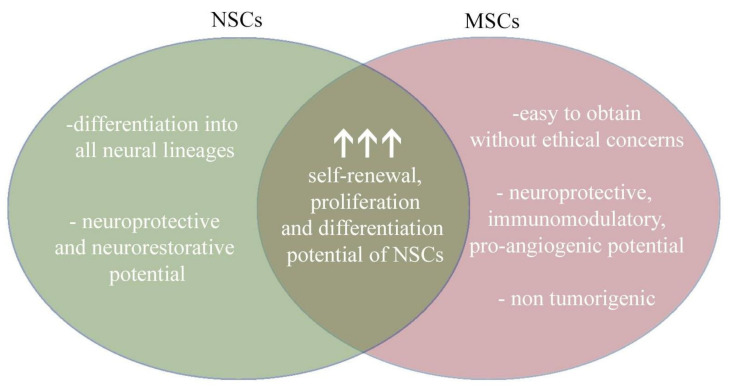
- 神經(jīng)干細胞可以作為分化成成熟神經(jīng)細胞和神經(jīng)膠質(zhì)細胞的細胞來源。
- 反過來,間充質(zhì)干細胞可以通過神經(jīng)保護、免疫調(diào)節(jié)和促血管生成活性支持神經(jīng)干細胞的移植。使用間充質(zhì)干細胞的另一個優(yōu)點是易于從多個來源分離并且不產(chǎn)生腫瘤。
盡管這種相互作用的機制尚未被探索,但其效果已經(jīng)非常有希望。盡管如此,仍然需要對這種組合的使用進行更多研究,特別是在動物模型和人體臨床試驗中。
六、常見問題解答(FAQ)
參考資料:Kaminska A, Radoszkiewicz K, Rybkowska P, Wedzinska A, Sarnowska A. Interaction of Neural Stem Cells (NSCs) and Mesenchymal Stem Cells (MSCs) as a Promising Approach in Brain Study and Nerve Regeneration. Cells. 2022 Apr 26;11(9):1464. doi: 10.3390/cells11091464. PMID: 35563770; PMCID: PMC9105617.
免責(zé)說明:本文僅用于傳播科普知識,分享行業(yè)觀點,不構(gòu)成任何臨床診斷建議!杭吉干細胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請及時跟本公眾號聯(lián)系,我們將在第一時間處理。



 掃碼添加官方微信
掃碼添加官方微信