Meta描述:神經干細胞(NSC)與間充質干細胞(MSC)如何協同促進神經再生?本文基于《細胞》雜志最新綜述,系統解析NSC與MSC的生物學特性、相互作用機制(Notch信號、旁分泌)、聯合移植策略及臨床轉化挑戰,附對比表格與未來方向。
引言:神經再生的挑戰與干細胞聯合策略
神經系統疾病和損傷(如腦卒中、帕金森病、脊髓損傷)是再生醫學領域最難攻克的堡壘之一。成年中樞神經系統(CNS)內源性修復能力極其有限,主要因為:
- 神經干細胞(NSC)數量稀少且多處于靜息狀態
- 損傷后微環境充滿炎癥因子和抑制再生的分子
- 成熟神經元無法分裂替代
干細胞移植為神經再生帶來了希望。其中,神經干細胞(NSC) 因其能夠分化為功能性神經元和膠質細胞,被視為最直接的細胞替代來源;而間充質干細胞(MSC) 則憑借免疫調節、旁分泌支持和低免疫原性,成為改善損傷微環境的理想輔助細胞。
神經干細胞(NSC)與間充質干細胞(MSC)協同治療神經系統疾病:機制、策略與前景(2025年綜述解讀)
近期,國際期刊雜志《細胞》發表了一篇神經干細胞 (NSC) 和間充質干細胞 (MSC) 的相互作用作為大腦研究和神經再生的一種有前途的方法的綜述,在這篇綜述中,我們討論了與雙邊MSC-NSC相互作用、環境條件下MSC向神經細胞(嵴衍生細胞亞群)分化、生物支架或通過重建與NSC共培養相關的各種治療策略和激活機制。

一、間充質干細胞和神經干細胞合作的潛在能力
間充質干細胞可以遷移到大腦受損部位,產生神經保護和血管保護作用。此外,它們可以促進受損大腦皮層的細胞再生,而它們的分泌組對腦外傷后的神經元具有有利的影響。
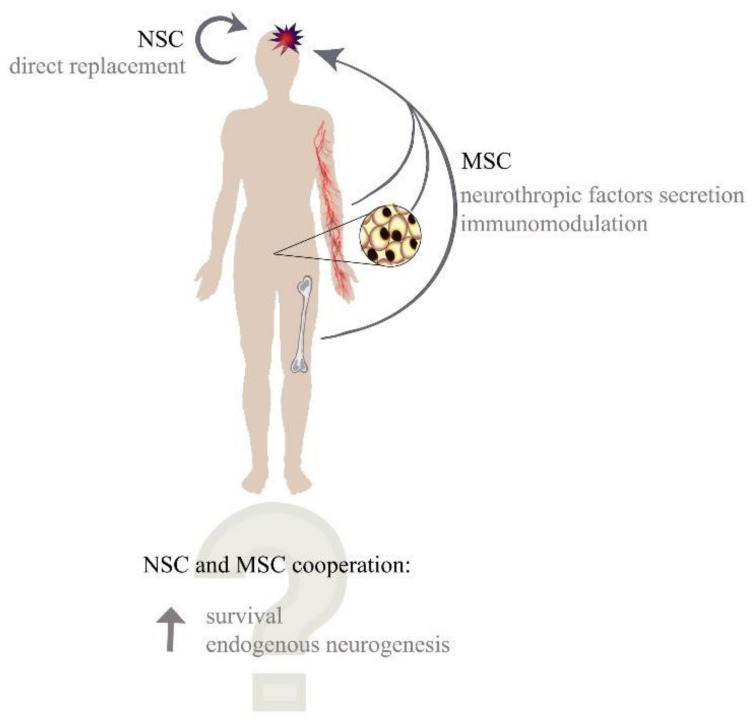
然而,關于MSC是否可以與NSC或其生態位相互作用以提高NSC分化為成熟和功能性神經元的再生能力的研究仍在進行中。間充質干細胞和神經干細胞單獨在中樞神經系統中的再生潛力較低,但它們獨特的功能可以建立協同關系,這對于增強治療效果至關重要。神經干細胞移植可以提供新的神經祖細胞,而MSC可以通過佐劑效應和細胞間接觸來免疫微環境并支持新生成的神經母細胞的存活和分化(圖1)。
二、神經干細胞到底是什么?從分子標志物到來源困境
很多人把NSC和NPC混著用,但嚴格來說不一樣。真正的NSC有三個特征:一是可以對稱分裂(自我擴增)和不對稱分裂(產生一個NSC和一個NPC);二是可以分化為三大神經譜系(神經元、星形膠質細胞、少突膠質細胞);三是在連續傳代后仍能保持多向分化能力。
分子標志物上,目前公認的是Sox2、Nestin、Pax6。Sox2是維持干性的核心轉錄因子,敲掉它NSC就會分化。Nestin是中間絲蛋白,在神經前體細胞中高表達,成熟神經元里沒有。Pax6主要調控皮層發育,在成人SVZ的NSC中也表達。
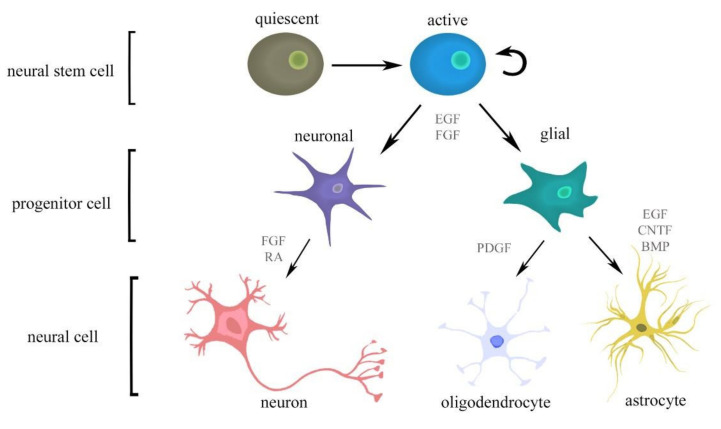
但NSC在體內的狀態不是一成不變的。它有兩種狀態:活躍(active)和靜息(quiescent)。靜息的NSC高表達BMP信號通路相關基因,低表達細胞周期蛋白。當受到VEGF、BDNF、Wnt、Shh等信號刺激時,靜息NSC會退出靜息期,進入細胞周期。這個“喚醒”過程是神經發生的第一限速步驟(圖2)。
NSC的來源主要有四種,各有各的爛攤子:
第一,胎兒/胚胎來源。這是最經典的方式。從流產胎兒或胚胎小鼠的腦組織中分離。優點是這些細胞是真的、活的NSC,分化潛能最高。缺點是倫理爭議越來越大——美國NIH對胎兒組織研究已經有嚴格限制,國內雖然沒那么嚴,但公眾輿論壓力也在增大。而且一個胎兒的量也有限,不可能工業化生產。
第二,成體腦組織來源。從SVZ或DG取一小塊,體外擴增。優點是可以自體移植,沒有免疫排斥。缺點是要開顱取腦組織——為了取細胞先切一刀,這種侵入性操作對患者來說代價太大。而且隨著年齡增長,成人NSC的數量和功能都在下降。60歲以上患者取自己的NSC,擴增出來的細胞活力遠不如年輕人。
第三,多能干細胞分化。用ESC或iPSC定向誘導為NSC。這是目前工業化生產最有希望的方向。日本京都大學已經用iPSC-NSC治療脊髓損傷,2024年又報了帕金森病的I/II期結果(就是之前那篇Nature文章)。但問題也很實在:誘導效率不穩定(有的批次90%以上陽性,有的不到50%)、殘留未分化iPSC有致瘤風險(雖然可以通過流式分選或自殺基因清除)、成本極高(一個批次幾十萬人民幣)。
第四,直接重編程(iNSC)。用轉錄因子(比如Sox2、Pax6、Brn2)直接將成纖維細胞轉分化為NSC,繞過iPSC中間階段。2011年就有文章做了,但效率低得可憐,而且得到的細胞更像NPC而不是真正的NSC。這些年進展不大。
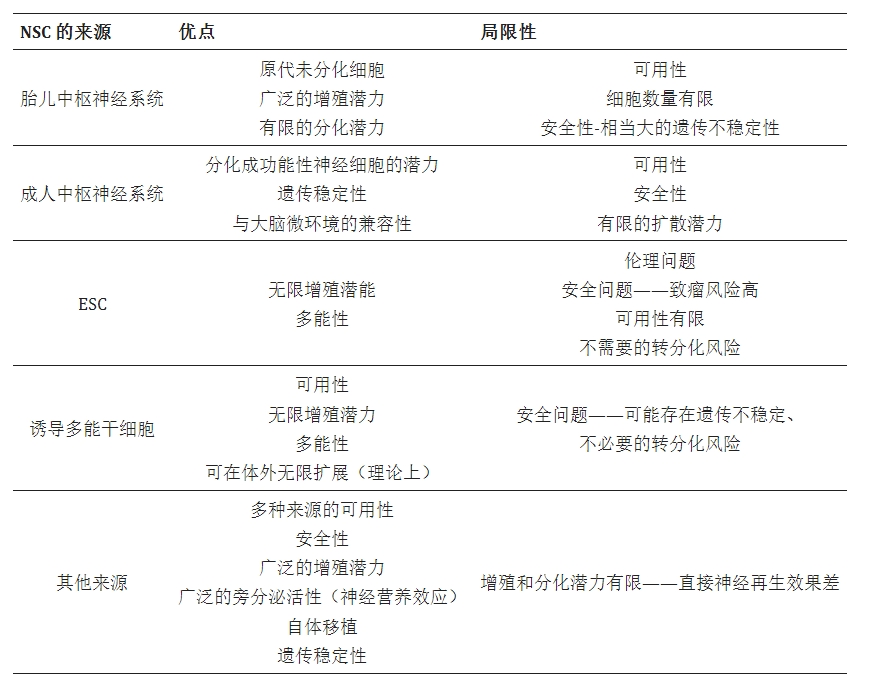
目前,在ClinicalTrials.gov上注冊的臨床研究多達74項。人們對應用這些干細胞治療神經系統疾病越來越感興趣,包括缺血性中風、帕金森病和阿爾茨海默病、肌萎縮側索硬化癥 (ALS) 或脊髓損傷 (SCI)。由于內源性神經干細胞的恢復能力無效,因此對多種來源的NSC進行了測試,包括胎兒和成人CNS衍生的NSC、來自多能干細胞的神經祖細胞以及非神經干細胞:表格1)。
到目前為止,尚未選擇理想的可用來源。每個來源都有其優點和缺點,下表總結了這些優點和缺點。
三、MSC在神經修復中的角色:不是分化,是“當保姆”
MSC在神經系統疾病中的研究遠遠多于NSC,注冊的臨床試驗數量是NSC的好幾倍。但MSC的作用機制跟大眾想象的不一樣——它不是靠變成神經元來修復大腦。
2000年代初期確實有一批文章聲稱MSC可以在腦內轉分化為神經元,表達NeuN、MAP2等神經元標志物。但后來幾個實驗室用更嚴格的譜系追蹤(比如用Cre-Lox系統標記MSC然后移植)發現,那些所謂的“神經元”要么是細胞融合形成的雜合細胞,要么是自發熒光假陽性,要么是MSC內吞了周圍死亡神經元的碎片。目前的主流共識是:MSC在體內基本不轉分化為功能性神經元。即使有,比例也低到沒有臨床意義。
那MSC憑什么治腦病?靠三條腿:
第一條,免疫調節。MSC不表達MHC-II類分子(HLA-DR陰性),也不表達CD80、CD86等共刺激分子,所以不會激活CD4+ T細胞。更關鍵的是,MSC能主動抑制免疫反應。機制包括:分泌IDO(indoleamine 2,3-dioxygenase)消耗色氨酸,導致T細胞周期阻滯;分泌PGE2、TGF-β、IL-10等抗炎因子;直接接觸誘導Treg生成;把巨噬細胞從促炎的M1型掰成抗炎的M2型。在脊髓損傷或腦卒中的動物模型中,移植MSC后,損傷部位的IFN-γ、TNF-α、IL-1β顯著下降,IL-10上升。
第二條,旁分泌營養支持。MSC分泌一堆神經營養因子:BDNF(促進神經元存活和突觸可塑性)、GDNF(對多巴胺能神經元尤其重要)、NGF、NT-3、bFGF、VEGF(促血管新生)、HGF(抗凋亡)。這些因子可以保護瀕死的神經元,促進軸突生長,誘導血管再生。一個經典的實驗是:把MSC的條件培養基(就是養過MSC的培養基,里面都是它們分泌的東西)打進中風大鼠的腦子里,效果跟打細胞本身差不多。這說明旁分泌是MSC的主要作用通路。
第三條,外泌體(EVs)介導的遠程調控。最近五年的熱點。MSC分泌的外泌體(30-150nm的小囊泡)里面裝了miRNA、mRNA、蛋白質,可以被受體細胞內吞,從而調控受體細胞的基因表達。比如MSC外泌體里的miR-133b可以促進神經突生長,miR-17-92簇可以促進少突膠質前體細胞增殖和髓鞘形成。外泌體的優勢是:沒有活細胞,所以不會有致瘤或栓塞風險;可以凍干保存,不用液氮;可以通過表面修飾實現靶向遞送。目前已經有一些臨床前研究用MSC外泌體治療中風、脊髓損傷、帕金森病,結果跟用MSC本身差不多。將來很可能MSC外泌體會取代MSC,變成“無細胞治療”的主力。
但MSC也不是沒有副作用。靜脈輸注MSC時,由于細胞體積較大(直徑15-30μm),大部分會被肺部毛細血管床截留,只有一小部分能到達腦部。這種“肺首過效應”本身不是問題——被截留在肺部的MSC反而可以分泌抗炎因子,通過全身循環間接影響腦部。但有研究報道,高劑量靜脈輸注MSC可能引起微栓塞,尤其是在肺功能不好的患者身上。還有研究擔心MSC在某些條件下可能促進腫瘤生長(比如給荷瘤小鼠打MSC,腫瘤長得更快),但這個爭議很大,不同實驗室結果相反。2024年FDA批準的Ryoncil(MSC治療兒童GVHD)是基于幾十個臨床試驗的數據,沒有發現明顯的促瘤信號。所以風險可能被夸大了,但也不是零。
四、MSC和NSC怎么互動?分子機制層面的事
這篇綜述最有價值的部分,是系統梳理了MSC和NSC之間的相互作用機制,而不是只說“1+1>2”這種空話。
第一個機制:MSC通過Notch信號維持NSC的干性。
Notch信號在發育神經生物學里是老面孔了。當Notch受體(Notch1-4)被配體(Jagged1/2、DLL1/3/4)激活后,Notch受體會被γ-secretase切割,釋放胞內段NICD(Notch intracellular domain)。NICD進入細胞核,與轉錄因子RBP-J結合,激活下游靶基因(如Hes1、Hes5)。Hes1和Hes5是堿性螺旋-環-螺旋轉錄因子,它們抑制 proneural 基因(如Ascl1、Neurogenin)的表達,從而抑制分化、維持干性。
MSC表面表達Jagged1和DLL1。當NSC和MSC共培養時,MSC通過直接接觸激活NSC的Notch信號。有實驗顯示,在沒有EGF和bFGF的培養基里,單獨培養的NSC很快就會分化——細胞變得扁平,Nestin下調,βIII-tubulin(神經元標志物)上調。但跟MSC共培養的NSC,即使沒有EGF/bFGF,仍然維持Nestin陽性,Hes1和Hes5的表達水平跟有EGF/bFGF時差不多。這說明MSC可以直接替代外源性生長因子的作用,通過Notch信號維持NSC的未分化狀態。
第二個機制:MSC通過旁分泌因子促進NSC的存活和神經元分化。
這個聽起來跟上面有點矛盾——MSC既維持NSC的干性,又促進分化?其實不矛盾,取決于微環境和時間點。
在NSC剛移植進去的時候,MSC分泌的BDNF、GDNF、HGF可以抑制凋亡通路。具體的分子通路:BDNF結合TrkB受體,激活PI3K/Akt通路,Akt磷酸化后抑制Bad和caspase-9,從而阻斷線粒體凋亡途徑。HGF結合c-Met受體,同樣激活PI3K/Akt,還激活MAPK/ERK通路,促進細胞增殖。在氧-葡萄糖剝奪(OGD)模型中(模擬缺血性中風),與MSC共培養的NSC,凋亡細胞比例比單獨培養的NSC低40-60%。
而在需要分化的時候,MSC分泌的BDNF和GDNF又可以促進NSC向神經元方向分化。具體的機制涉及:BDNF/TrkB激活下游的Ras-MAPK通路,磷酸化CREB,CREB進入細胞核促進 proneural 基因(如NeuroD1)的表達。有研究用微流控芯片做共培養,發現NSC跟MSC共培養7天后,βIII-tubulin陽性的神經元比例比對照組高出2倍以上,而且這些神經元有動作電位(電生理記錄證實)。
第三個機制:MSC通過免疫調節為NSC移植創造“免疫豁免”微環境。
這是聯合移植最直觀的好處。異體NSC移植后,宿主的免疫系統會攻擊它們——CD8+ T細胞會直接殺傷,巨噬細胞會吞噬。MSC可以通過前面說的IDO、PGE2、TGF-β等機制抑制T細胞活化,把巨噬細胞掰成M2型,減少IFN-γ和TNF-α的釋放。這樣一來,NSC的存活率可以大幅提升。
有一個經典的動物實驗:在脊髓損傷大鼠模型中,單獨移植NSC的組,8周后存活的NSC只有移植量的5-10%。而NSC+MSC聯合移植的組,存活率提升到30-40%。而且聯合移植組中,NSC分化為神經元的比例也更高——可能是因為MSC分泌的BDNF、GDNF提供了分化信號。
第四個機制:NSC反過來也能影響MSC——誘導MSC向神經譜系分化。
這個方向的證據比前三個弱一些,但確實有報道。有研究發現,NSC分泌的Shh(Sonic hedgehog)可以誘導MSC表達神經前體細胞標志物(Nestin、Pax6)。還有研究用transwell共培養(不讓細胞直接接觸,只共享培養基),發現NSC的條件培養基也能讓MSC表達一些神經元樣的標志物。但問題是,這些MSC到底有沒有變成真正的功能性神經元?目前沒有電生理證據。大多數研究者認為,即使MSC被誘導表達一些神經標志物,它們也很難形成動作電位和突觸。所以這條機制在聯合移植中的貢獻可能不大,主要貢獻還是MSC支持NSC,而不是反過來。
五、總結
干細胞與伴生/支持細胞之間的相互作用對平衡和組織再生至關重要。在許多器官中,間充質干細胞維持干細胞的存活和轉運增殖細胞(TAC)的增殖,然后分化成目標細胞類型。雖然證據尚不充分,但間質作為生態位的組成部分,似乎在靜止的間充質干細胞與增殖、分化和從細胞龕遷移的祖細胞之間的平衡中發揮作用。
神經干細胞和間充質干細胞之間也存在同樣的相互作用。
- 由于神經干細胞可能是所有神經細胞類型的無限來源,而間充質干細胞則顯示出高度的旁分泌活性,因此將它們聯合用于治療神經系統疾病似乎極具前景。
根據現有的科學文獻,間充質干細胞和神經干細胞的結合似乎代表了一個有前途的治療前景(圖4)。
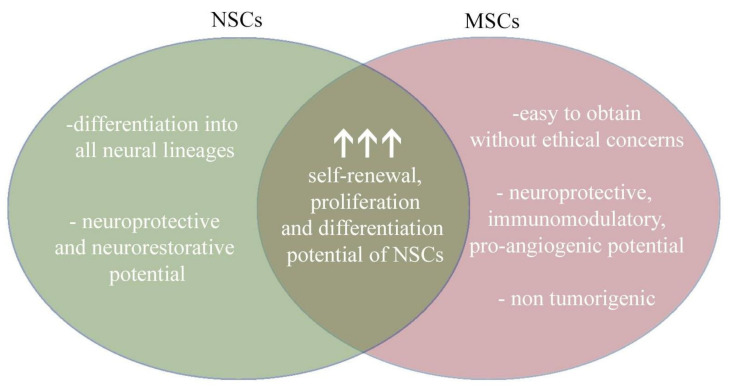
- 神經干細胞可以作為分化成成熟神經細胞和神經膠質細胞的細胞來源。
- 反過來,間充質干細胞可以通過神經保護、免疫調節和促血管生成活性支持神經干細胞的移植。使用間充質干細胞的另一個優點是易于從多個來源分離并且不產生腫瘤。
盡管這種相互作用的機制尚未被探索,但其效果已經非常有希望。盡管如此,仍然需要對這種組合的使用進行更多研究,特別是在動物模型和人體臨床試驗中。
六、常見問題解答(FAQ)
參考資料:Kaminska A, Radoszkiewicz K, Rybkowska P, Wedzinska A, Sarnowska A. Interaction of Neural Stem Cells (NSCs) and Mesenchymal Stem Cells (MSCs) as a Promising Approach in Brain Study and Nerve Regeneration. Cells. 2022 Apr 26;11(9):1464. doi: 10.3390/cells11091464. PMID: 35563770; PMCID: PMC9105617.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請及時跟本公眾號聯系,我們將在第一時間處理。



 掃碼添加官方微信
掃碼添加官方微信