炎癥、神經(jīng)遞質(zhì)和神經(jīng)元凋亡是重度抑郁癥 (MDD) 進(jìn)展的關(guān)鍵因素。先前的研究表明,間充質(zhì)干細(xì)胞 (MSC) 對(duì)神經(jīng)炎癥和神經(jīng)保護(hù)具有積極作用。
Contents
從基礎(chǔ)到臨床試驗(yàn):間充質(zhì)干細(xì)胞能通過(guò)緩解神經(jīng)炎癥改善慢性應(yīng)激引起的抑郁和焦慮
近期,“Journal of Neuroimmune Pharmacology”發(fā)表了一篇“人臍帶間充質(zhì)干細(xì)胞通過(guò)緩解神經(jīng)炎癥改善慢性不可預(yù)測(cè)的輕度應(yīng)激引起的抑郁和焦慮”的研究文章[1]。

初步的研究結(jié)果表明:MSCs可以緩解神經(jīng)炎癥,抑制中樞神經(jīng)系統(tǒng)小膠質(zhì)細(xì)胞的活化,從而防止神經(jīng)元凋亡。hUC-MSCs還可以提高5-HT、DA和BDNF的水平,從而有助于緩解抑郁和焦慮行為。
抑郁癥介紹
重度抑郁癥 (MDD) 是一種復(fù)雜且異質(zhì)性的神經(jīng)退行性疾病,其特征是情緒、精神運(yùn)動(dòng)和認(rèn)知障礙。據(jù)估計(jì),MDD影響全球超過(guò)3.5億人,每年有超過(guò)70萬(wàn)人死于自殺,是全球致殘的主要原因。單胺類(lèi)抗抑郁藥的缺陷,包括耐藥性和起效延遲,凸顯了開(kāi)發(fā)新型抗抑郁藥物的迫切需求。

神經(jīng)炎癥:解析抑郁癥病理機(jī)制的新維度與治療靶向策略
現(xiàn)有研究顯示,單胺類(lèi)神經(jīng)遞質(zhì)(如5-HT和DA)在腦區(qū)獎(jiǎng)賞預(yù)測(cè)功能中的特異性作用,但其抗抑郁療效延遲提示MDD存在其他機(jī)制。
近年發(fā)現(xiàn)神經(jīng)炎癥在MDD病理中起關(guān)鍵作用,臨床證據(jù)顯示干擾素治療可誘發(fā)抑郁,MDD患者外周炎癥因子水平顯著升高,且炎癥水平與獎(jiǎng)賞系統(tǒng)功能障礙程度相關(guān)。神經(jīng)炎癥通過(guò)激活小膠質(zhì)細(xì)胞破壞血腦屏障,形成炎癥增強(qiáng)-單胺合成受阻-神經(jīng)營(yíng)養(yǎng)信號(hào)受損的惡性循環(huán),最終導(dǎo)致神經(jīng)元功能異常。
神經(jīng)炎癥機(jī)制不僅解釋了傳統(tǒng)單胺假說(shuō)的局限性,更揭示了MDD的多維度病理特征。從外周炎癥因子水平異常到中樞神經(jīng)炎癥級(jí)聯(lián)反應(yīng),從血腦屏障損傷到神經(jīng)元功能障礙,這一系統(tǒng)性病理過(guò)程為MDD治療提供了新方向——靶向抑制神經(jīng)炎癥可能成為改善抑郁癥狀的有效策略。
人臍帶間充質(zhì)干細(xì)胞治療抑郁癥的生物分布、作用機(jī)制及臨床研究進(jìn)展
間充質(zhì)干細(xì)胞是一種多能干細(xì)胞,來(lái)源廣泛、具有自我更新和分化能力,免疫原性低,倫理問(wèn)題較少。MSCs因其歸巢能力、免疫調(diào)節(jié)特性和旁分泌作用,具有治療神經(jīng)退行性疾病的潛力。
大量臨床前研究表明,hUC-MSCs可以通過(guò)調(diào)節(jié)C3a-C3aR信號(hào)轉(zhuǎn)導(dǎo)來(lái)改變小膠質(zhì)細(xì)胞極化,從而抑制海馬 (Hip) 中IL-1β和TNF-α的水平,改善慢性不可預(yù)測(cè)性溫和應(yīng)激模型 (CUMS) 引起的抑郁癥。hUC-MSCs調(diào)節(jié)小膠質(zhì)細(xì)胞活化以減少神經(jīng)炎癥和修復(fù)神經(jīng)結(jié)構(gòu),改善抑郁樣和焦慮樣行為。
本文章總結(jié)了人臍帶間充質(zhì)干細(xì)胞 (hUC-MSC) 在CUMS小鼠模型中的療效和治療機(jī)制。目前很少有研究表明間充質(zhì)干細(xì)胞 (MSC) 定位于重度抑郁癥 (MDD) 動(dòng)物的腦部。因此,我們旨在評(píng)估hUC-MSC的生物分布,以闡明hUC-MSC參與治療MDD的機(jī)制。另外,闡述了近些年干細(xì)胞在治療抑郁癥方面的臨床研究進(jìn)展。
方法:為此,我們將人臍帶間充質(zhì)干細(xì)胞 (hUC-MSC) 注入慢性不可預(yù)測(cè)性輕度應(yīng)激模型 (CUMS) 小鼠體內(nèi),以評(píng)估其對(duì)炎癥、神經(jīng)遞質(zhì)、小膠質(zhì)細(xì)胞、神經(jīng)元活化和神經(jīng)元凋亡的影響。利用CM-Dil標(biāo)記的hUC-MSC檢測(cè)hUC-MSC在腦內(nèi)的分布。
人臍帶間充質(zhì)干細(xì)胞治療抑郁癥大鼠模型的結(jié)果
hUC-MSCs改善CUMS誘發(fā)的抑郁和焦慮樣行為
實(shí)驗(yàn)通過(guò)慢性應(yīng)激(CUMS)小鼠模型評(píng)估人臍帶間充質(zhì)干細(xì)胞(hUC-MSCs)的抗抑郁及抗焦慮效果。研究發(fā)現(xiàn),hUC-MSCs能劑量依賴(lài)性地逆轉(zhuǎn)CUMS誘導(dǎo)的體重下降,其中最高劑量組(2×10?細(xì)胞/小鼠)效果最顯著,且優(yōu)于傳統(tǒng)抗抑郁藥氟西汀(Flu)(圖1)。
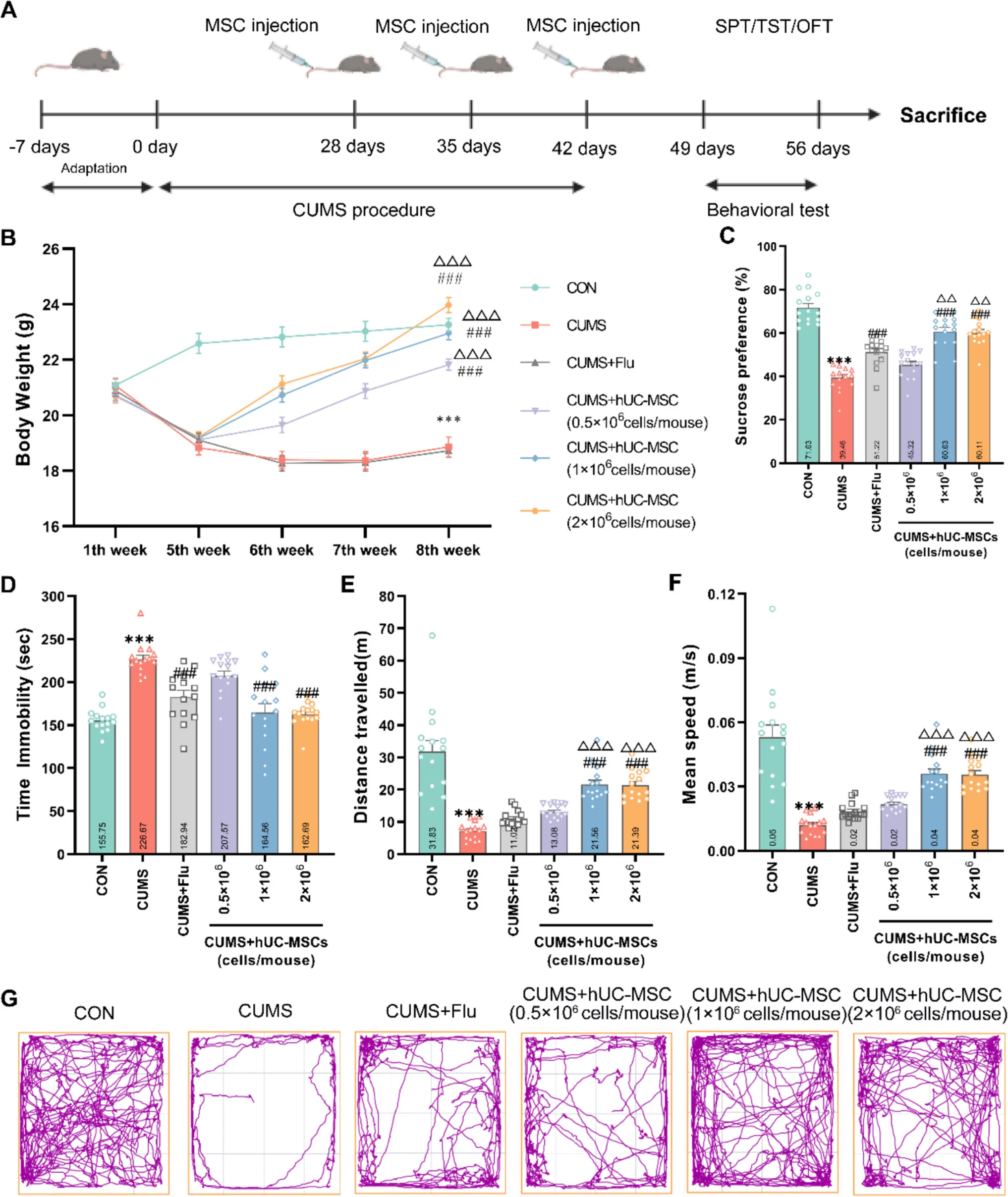
A實(shí)驗(yàn)時(shí)間線(xiàn)示意圖。B實(shí)驗(yàn)期間測(cè)量體重。C 測(cè)量了hUC-MSCs在蔗糖偏好測(cè)試 (SPT)、(?D?)懸尾測(cè)試 (TST)、(E) 距離、(F) 平均速度和 (G)開(kāi)放場(chǎng)測(cè)試(OFT) 圖形表示中的效果。
在行為學(xué)測(cè)試中,hUC-MSCs顯著改善抑郁相關(guān)癥狀:糖水消耗測(cè)試顯示高劑量組快感缺失緩解優(yōu)于Flu組;懸尾實(shí)驗(yàn)表明其縮短不動(dòng)時(shí)間的效果與Flu相當(dāng);開(kāi)野實(shí)驗(yàn)進(jìn)一步揭示,hUC-MSCs(尤其是高劑量組)在提升運(yùn)動(dòng)活力和緩解焦慮方面顯著優(yōu)于Flu,且效果與劑量正相關(guān)。
研究從多維度驗(yàn)證hUC-MSCs對(duì)CUMS模型的行為改善作用,揭示了其劑量依賴(lài)性的治療特性。相較于Flu,hUC-MSCs不僅更有效恢復(fù)應(yīng)激導(dǎo)致的生理指標(biāo)異常(如體重),還在核心抑郁癥狀(快感缺失、行為絕望)和焦慮樣行為中表現(xiàn)出優(yōu)勢(shì)。
這一發(fā)現(xiàn)提示,hUC-MSCs可能通過(guò)多重機(jī)制協(xié)同作用,為開(kāi)發(fā)基于干細(xì)胞的抑郁癥治療策略提供了實(shí)驗(yàn)依據(jù),尤其強(qiáng)調(diào)劑量?jī)?yōu)化在臨床應(yīng)用中的重要性。
hUC-MSCs減輕MDD小鼠的神經(jīng)元損傷
本研究通過(guò)檢測(cè)CUMS抑郁模型小鼠多個(gè)腦區(qū)(海馬、前額葉皮層、基底外側(cè)杏仁核及中縫背核)的神經(jīng)元凋亡標(biāo)志物(TUNEL及Cleaved Caspase-3/NeuN),發(fā)現(xiàn)hUC-MSCs能顯著減少凋亡細(xì)胞數(shù)量,緩解神經(jīng)元損傷(圖2)。
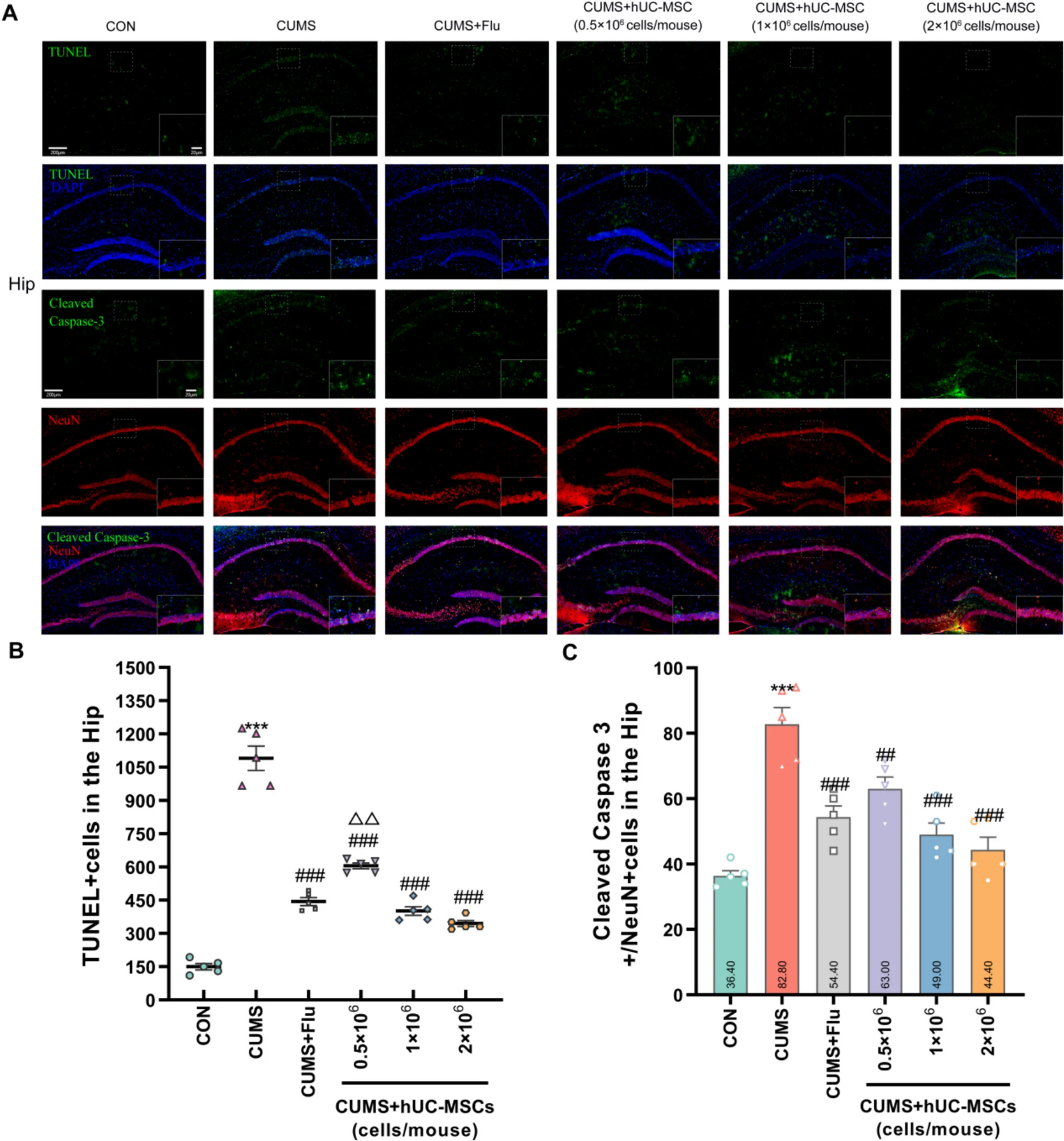
其中,高劑量hUC-MSCs(2×10?細(xì)胞/小鼠)在逆轉(zhuǎn)海馬、前額葉皮層和杏仁核損傷方面效果最優(yōu),且部分腦區(qū)(如中縫背核)的治療效果顯著優(yōu)于傳統(tǒng)藥物氟西汀。
實(shí)驗(yàn)證實(shí),hUC-MSCs的神經(jīng)保護(hù)作用具有劑量依賴(lài)性,其通過(guò)抑制神經(jīng)元凋亡通路,為抑郁癥的細(xì)胞治療提供了重要證據(jù)。
hUC-MSCs修復(fù)CUMS小鼠神經(jīng)元活動(dòng)異常
即刻早期基因c-Fos表達(dá)是神經(jīng)科學(xué)中表征腦功能活動(dòng)的標(biāo)志物。抑郁癥(MDD)小鼠腦區(qū)c-Fos表達(dá)升高提示神經(jīng)元活動(dòng)異常激活。
本研究通過(guò)檢測(cè)神經(jīng)元活動(dòng)標(biāo)志物c-Fos表達(dá),發(fā)現(xiàn)hUC-MSCs能有效逆轉(zhuǎn)CUMS小鼠海馬、前額葉皮層、中縫背核及基底外側(cè)杏仁核的神經(jīng)元活動(dòng)異常(圖3)。高劑量hUC-MSCs(2×10?細(xì)胞/小鼠)在降低c-Fos表達(dá)方面顯著優(yōu)于傳統(tǒng)抗抑郁藥氟西汀(除前額葉皮層外),提示其通過(guò)調(diào)控多腦區(qū)神經(jīng)元功能亢進(jìn)發(fā)揮治療作用。

實(shí)驗(yàn)證實(shí),hUC-MSCs通過(guò)修復(fù)神經(jīng)元活動(dòng)異常改善抑郁表型,進(jìn)一步闡明其抗抑郁機(jī)制與神經(jīng)元功能穩(wěn)態(tài)調(diào)節(jié)密切相關(guān)。
hUC-MSCs調(diào)節(jié)CUMS小鼠的神經(jīng)遞質(zhì)和腦源性神經(jīng)營(yíng)養(yǎng)因子 (BDNF) 水平
本研究揭示了hUC-MSCs對(duì)CUMS小鼠神經(jīng)遞質(zhì)系統(tǒng)的調(diào)節(jié)作用。CUMS模型導(dǎo)致海馬、前額葉皮層等腦區(qū)及血清中5-HT和DA水平顯著下降,而hUC-MSCs治療(尤其是1×10?和2×10?細(xì)胞/小鼠劑量組)能劑量依賴(lài)性地逆轉(zhuǎn)這一趨勢(shì),其效果在多數(shù)腦區(qū)優(yōu)于傳統(tǒng)抗抑郁藥氟西汀(Flu)。
例如,在PFC中劑量hUC-MSCs組的DA水平提升顯著強(qiáng)于Flu組,表明hUC-MSCs可能通過(guò)更高效的神經(jīng)遞質(zhì)穩(wěn)態(tài)重建發(fā)揮治療優(yōu)勢(shì)(圖4)。
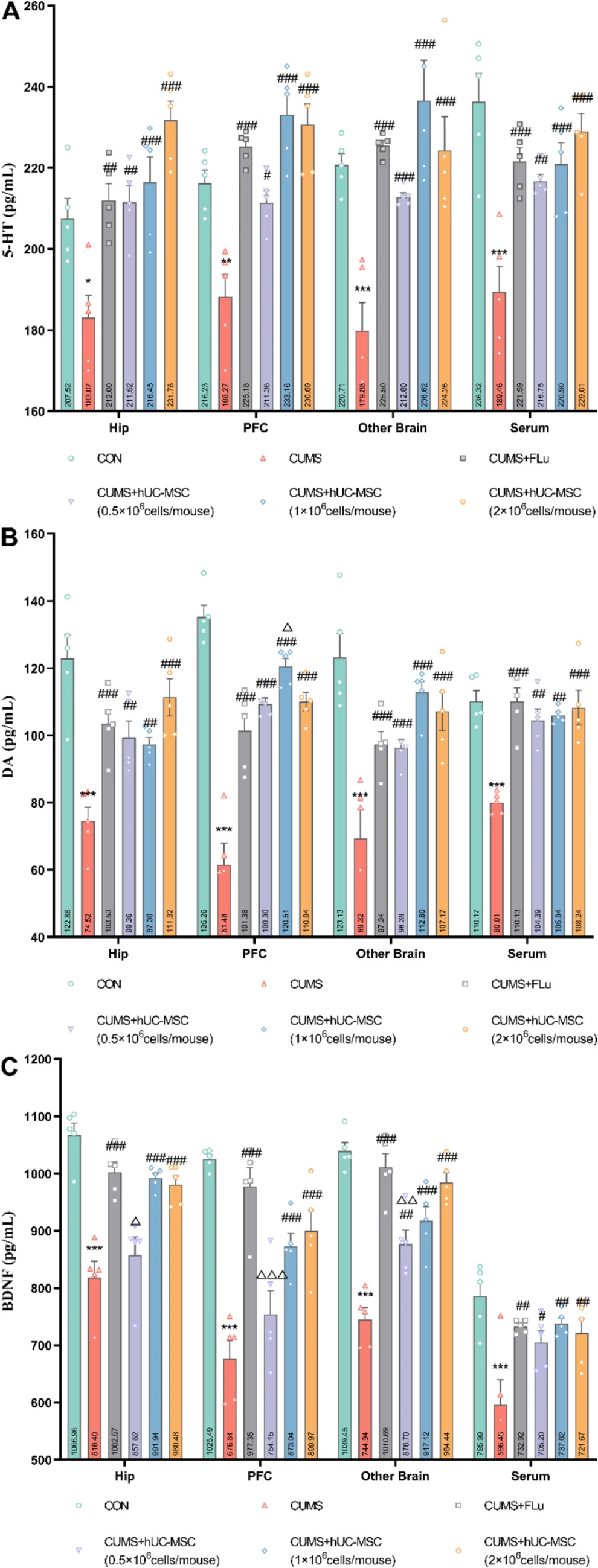
除神經(jīng)遞質(zhì)外,hUC-MSCs還顯著提升CUMS小鼠腦區(qū)及血清中的BDNF水平,但其效果與Flu組無(wú)顯著差異,提示BDNF上調(diào)可能是hUC-MSCs與Flu共有的抗抑郁機(jī)制之一。
綜合神經(jīng)遞質(zhì)與BDNF的協(xié)同調(diào)控作用,hUC-MSCs通過(guò)多靶點(diǎn)修復(fù)突觸可塑性障礙,為解釋其抗抑郁療效提供了分子層面的證據(jù)。研究進(jìn)一步支持hUC-MSCs作為抑郁癥細(xì)胞療法的潛力,并強(qiáng)調(diào)劑量?jī)?yōu)化對(duì)其臨床轉(zhuǎn)化的重要性。
hUC-MSCs調(diào)控中樞神經(jīng)系統(tǒng)炎癥水平并抑制小膠質(zhì)細(xì)胞激活
研究證實(shí),CUMS小鼠腦區(qū)及外周炎癥因子(IL-6、IL-1β、TNF-α)水平顯著升高,而hUC-MSCs治療可劑量依賴(lài)性地抑制炎癥反應(yīng),其中高劑量組(2×10?細(xì)胞/小鼠)效果與氟西汀(Flu)相當(dāng)。
值得注意的是,hUC-MSCs的抗炎作用在低、中劑量組即已顯現(xiàn),且高劑量組對(duì)炎癥因子的調(diào)控未表現(xiàn)出與Flu的顯著差異(圖5),提示其抗炎效能接近或達(dá)到傳統(tǒng)藥物水平。
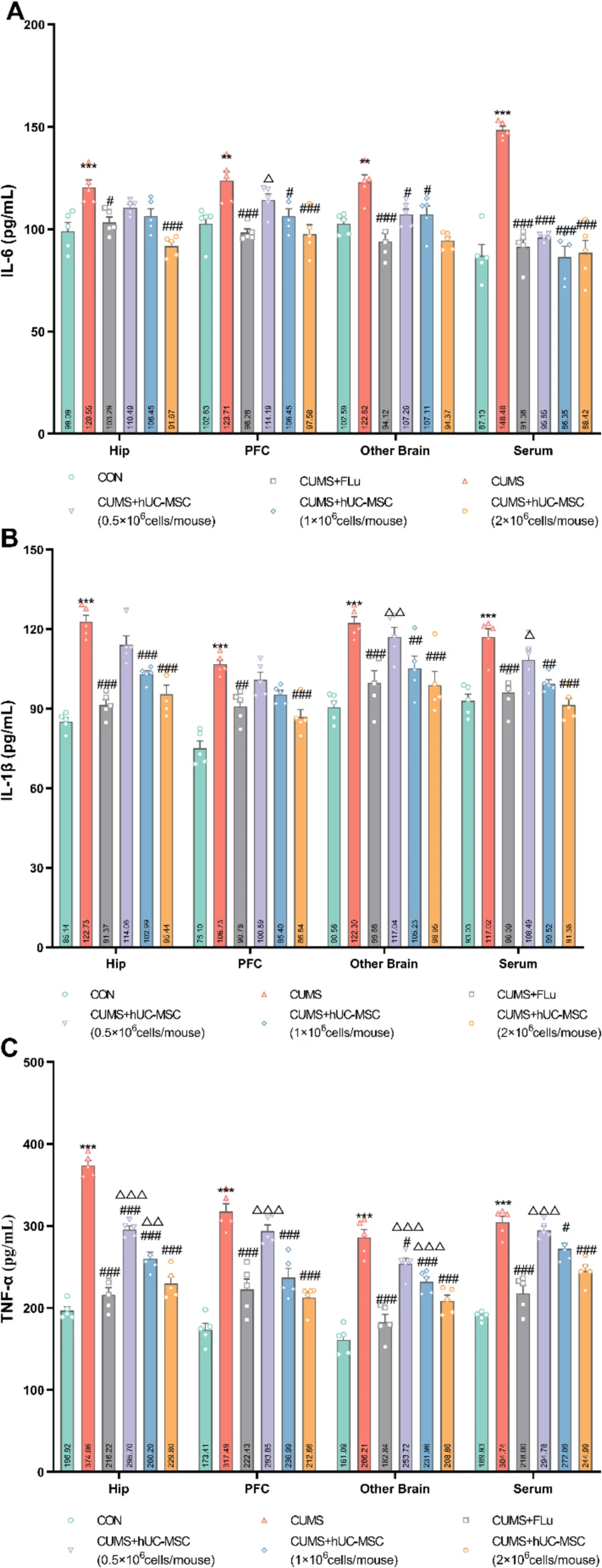
進(jìn)一步分析小膠質(zhì)細(xì)胞激活狀態(tài)發(fā)現(xiàn),hUC-MSCs顯著抑制CUMS誘導(dǎo)的Hip和PFC中IBA1+細(xì)胞數(shù)量增加,且高劑量組效果顯著優(yōu)于Flu組,凸顯其獨(dú)特的神經(jīng)免疫調(diào)節(jié)優(yōu)勢(shì)。
機(jī)制上,hUC-MSCs通過(guò)雙重路徑——降低促炎細(xì)胞因子水平與抑制小膠質(zhì)細(xì)胞過(guò)度激活——協(xié)同減輕神經(jīng)炎癥,為解釋其抗抑郁作用提供了免疫微環(huán)境層面的證據(jù)。研究強(qiáng)調(diào),hUC-MSCs的劑量依賴(lài)性效應(yīng)為其臨床應(yīng)用的精準(zhǔn)化治療策略提供了重要依據(jù)。
hUC-MSCs穿透血腦屏障并改善CUMS小鼠BBB通透性
研究證實(shí),CUMS小鼠BBB通透性顯著增加(表現(xiàn)為EB外滲增多),而hUC-MSCs治療可有效減少EB滲漏,其效果優(yōu)于傳統(tǒng)藥物氟西汀(Flu)(圖6)。通過(guò)熒光標(biāo)記技術(shù)進(jìn)一步發(fā)現(xiàn),hUC-MSCs能夠穿過(guò)受損BBB并定位于海馬、前額葉皮層等關(guān)鍵腦區(qū),提示其具有直接作用于中樞神經(jīng)系統(tǒng)的能力。
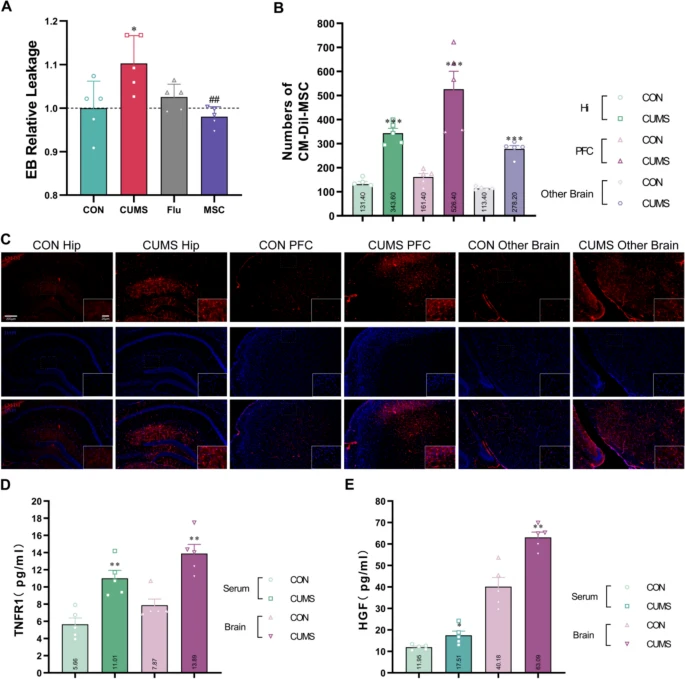
機(jī)制研究表明,hUC-MSCs通過(guò)分泌sTNFR1(抑制炎癥信號(hào))和HGF(促進(jìn)血管修復(fù))雙重途徑修復(fù)BBB結(jié)構(gòu)完整性。這一發(fā)現(xiàn)不僅解釋了hUC-MSCs降低BBB通透性的分子基礎(chǔ),還揭示了其通過(guò)調(diào)控神經(jīng)血管單元功能實(shí)現(xiàn)抗抑郁作用的潛在機(jī)制,為基于干細(xì)胞的BBB靶向治療策略提供了新依據(jù)。
討論:研究表明,炎性細(xì)胞因子在神經(jīng)細(xì)胞信號(hào)通路和神經(jīng)內(nèi)分泌系統(tǒng)功能中發(fā)揮著關(guān)鍵作用。我們的研究結(jié)果表明,hUC-MSC能夠穿透CUMS小鼠的大腦,同時(shí)保持血腦屏障 (BBB) 的完整性。此外,我們的研究還揭示,hUC-MSC能夠抑制小膠質(zhì)細(xì)胞活化,從而減少神經(jīng)炎癥并增加神經(jīng)遞質(zhì),這有助于減少神經(jīng)元凋亡并維持正常的神經(jīng)元活動(dòng)。
因此,hUC-MSC能夠有效改善CUMS引起的抑郁癥。我們的研究為hUC-MSC治療重度抑郁癥 (MDD) 的機(jī)制提供了新的見(jiàn)解,并支持其作為一種可行且有前景的 MDD 治療策略的潛力。
除此之外,近些年干細(xì)胞治療抑郁癥的臨床研究進(jìn)展有哪些?
2016年,“實(shí)驗(yàn)生物學(xué)和醫(yī)學(xué)公報(bào)”報(bào)道了一項(xiàng)“臍帶血細(xì)胞對(duì)難治性抑郁癥患者的療效”的臨床研究結(jié)果。

初步表明:科研人員(我們)研究了臍帶血細(xì)胞在女性難治性抑郁狀態(tài)治療中的療效。我們注射了2.5億個(gè)濃縮臍帶血細(xì)胞(注射4次,間隔1周)。對(duì)照組接受安慰劑。兩組患者均觀察到抑郁癥狀減少,低心境障礙嚴(yán)重程度降低。輸注細(xì)胞濃縮物有助于延遲治療耐藥性的糾正,并將抑郁癥嚴(yán)重程度降至中度。
在主要組中,我們?cè)谡J(rèn)知領(lǐng)域觀察到了顯著、持久且長(zhǎng)期的積極動(dòng)態(tài)。臍帶血細(xì)胞濃縮物的治療潛力可用于克服抑郁癥患者形成的治療耐藥性。
目前,我已經(jīng)在Clintrial.gov平臺(tái)上找到了三項(xiàng)干細(xì)胞治療抑郁癥的臨床試驗(yàn),旨在評(píng)估干細(xì)胞和外泌體用于治療抑郁癥的安全性、有效性和耐受性。
第一項(xiàng):2019年,澳大利亞國(guó)立大學(xué)進(jìn)行了一項(xiàng)異基因人類(lèi)間充質(zhì)干細(xì)胞(hMSCs)輸注治療難治性抑郁癥患者的臨床試驗(yàn)。

ClinicalTrials.gov ID:NCT02675556
研究的目的:旨在評(píng)估異基因人類(lèi)間充質(zhì)干細(xì)胞輸注與安慰劑相比對(duì)難治性抑郁癥患者的安全性和潛在療效。
目前臨床試驗(yàn)最新動(dòng)態(tài):截止2025年5月,ClinicalTrials.gov顯示臨床終止。主要原因?yàn)檎心己突I資困難。
第二項(xiàng):2024年,美國(guó)德克薩斯大學(xué)休斯頓健康科學(xué)中心開(kāi)展了一項(xiàng)輔助性異基因間充質(zhì)干細(xì)胞治療難治性雙相抑郁的臨床研究。

ClinicalTrials.gov ID:NCT03522545
研究的目的:研究人員的總體目標(biāo)是評(píng)估從血源性骨髓分離的同種異體骨髓衍生的多能間充質(zhì)基質(zhì)細(xì)胞 (MSC) 對(duì)治療難治性雙相抑郁癥患者 (TRBD) 的治療效果和耐受性。
目前臨床試驗(yàn)最新動(dòng)態(tài):招募臨床患者當(dāng)中。
第三項(xiàng):2025年,美國(guó)德克薩斯大學(xué)里奧格蘭德河谷分校進(jìn)行了一項(xiàng)同種異體人間充質(zhì)干細(xì)胞輸注與安慰劑在酒精使用障礙和重度抑郁癥中的療效對(duì)比的臨床研究。

ClinicalTrials.gov ID:NCT03265808
研究目的:本研究的目的是考察干細(xì)胞治療酒精使用障礙和重度抑郁癥 (AUD-MD) 患者的安全性。
目前臨床試驗(yàn)最新動(dòng)態(tài):正在進(jìn)行中,但是未發(fā)布相關(guān)結(jié)果,不招募患者。
寫(xiě)在最后:干細(xì)胞治療抑郁癥憑借其多靶點(diǎn)調(diào)控優(yōu)勢(shì)(抗炎、神經(jīng)再生、BBB修復(fù)),為難治性患者提供了突破傳統(tǒng)單胺假說(shuō)的新希望。
盡管臨床轉(zhuǎn)化仍面臨安全性驗(yàn)證、標(biāo)準(zhǔn)化生產(chǎn)及機(jī)制解析等挑戰(zhàn),隨著技術(shù)革新與跨學(xué)科協(xié)作,干細(xì)胞療法有望在未來(lái)十年內(nèi)成為抑郁癥治療的重要支柱。
正如項(xiàng)鵬教授所言:“從肺-腦軸到代謝微環(huán)境,干細(xì)胞研究的每一次突破都在重塑我們對(duì)抑郁癥復(fù)雜病理的認(rèn)知,并為治愈帶來(lái)更多可能。”
未來(lái)的研究需在嚴(yán)謹(jǐn)?shù)呐R床驗(yàn)證與機(jī)制探索中穩(wěn)步推進(jìn),最終將這一“生命工程師”的潛力轉(zhuǎn)化為患者切實(shí)的福音。
免責(zé)說(shuō)明:本文僅用于傳播科普知識(shí),分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專(zhuān)業(yè)建議。如有版權(quán)等疑問(wèn),請(qǐng)隨時(shí)聯(lián)系我。
文章來(lái)源:[1]:Liu, G., Miao, L., Niu, H.?et al.?Human Umbilical Cord Mesenchymal Stem Cells Ameliorated Chronic Unpredictable Mild Stress-Induced Depression and Anxiety by Alleviating Neuroinflammation.?J Neuroimmune Pharmacol?20, 45 (2025). https://doi.org/10.1007/s11481-025-10198-2



 掃碼添加官方微信
掃碼添加官方微信