Meta描述:神經(jīng)炎癥是阿爾茨海默病、帕金森病、多發(fā)性硬化癥等神經(jīng)退行性疾病的核心驅(qū)動(dòng)因素。本文基于《衰老神經(jīng)科學(xué)前沿》最新綜述,系統(tǒng)解析小膠質(zhì)細(xì)胞M1/M2極化、星形膠質(zhì)細(xì)胞A1/A2表型、外周免疫細(xì)胞浸潤(rùn)等機(jī)制,并探討干細(xì)胞療法、基因干預(yù)、納米粒子等未來(lái)治療方向。
Contents
神經(jīng)炎癥在神經(jīng)退行性疾病中的作用:當(dāng)前的理解和未來(lái)的治療方法
近日,國(guó)際期刊雜志《衰老神經(jīng)科學(xué)前沿》發(fā)表一篇《神經(jīng)炎癥在神經(jīng)退行性疾病中的作用:當(dāng)前認(rèn)識(shí)與未來(lái)治療目標(biāo)》的文獻(xiàn)綜述,這篇綜述揭示了與神經(jīng)變性相關(guān)的主要神經(jīng)炎癥信號(hào)通路。此外,它還探索了有前途的治療途徑,例如干細(xì)胞療法、基因干預(yù)和納米粒子,旨在調(diào)節(jié)神經(jīng)炎癥并可能阻礙或減緩這些疾病的進(jìn)展。全面了解神經(jīng)炎癥與這些疾病之間的復(fù)雜聯(lián)系對(duì)于制定未來(lái)的治療策略至關(guān)重要,這些策略可以減輕這些破壞性疾病帶來(lái)的負(fù)擔(dān)。

一、什么是神經(jīng)炎癥?為什么它既是朋友也是敵人?
神經(jīng)炎癥聽(tīng)起來(lái)像是一個(gè)壞東西,但事情沒(méi)那么簡(jiǎn)單。
當(dāng)你的大腦遭遇創(chuàng)傷、感染或毒素時(shí),它會(huì)啟動(dòng)一套復(fù)雜的防御反應(yīng)——這就是神經(jīng)炎癥。急性、短期的神經(jīng)炎癥是有益的:小膠質(zhì)細(xì)胞(大腦的常駐免疫細(xì)胞)被激活,它們像清道夫一樣吞噬病原體和細(xì)胞碎片,釋放炎癥介質(zhì)來(lái)控制損傷,然后修復(fù)過(guò)程開(kāi)始。沒(méi)有這個(gè)反應(yīng),大腦無(wú)法從任何損傷中恢復(fù)。
問(wèn)題出在“慢性”上。當(dāng)炎癥反應(yīng)持續(xù)數(shù)月甚至數(shù)年,小膠質(zhì)細(xì)胞和星形膠質(zhì)細(xì)胞就會(huì)從“保護(hù)模式”切換到“攻擊模式”。它們持續(xù)釋放促炎細(xì)胞因子(IL-1β、TNF-α、IL-6)、活性氧(ROS)、一氧化氮(NO)等毒性物質(zhì)。這些東西本來(lái)是用來(lái)殺病原體的,但長(zhǎng)期暴露下,它們開(kāi)始傷害健康的神經(jīng)元——導(dǎo)致突觸功能受損、線粒體功能障礙、最終神經(jīng)元死亡。
這正是阿爾茨海默病(AD)、帕金森病(PD)、多發(fā)性硬化癥(MS)、亨廷頓病(HD)、肌萎縮側(cè)索硬化癥(ALS)的共同病理特征。雖然每種病的首發(fā)部位和蛋白聚集類(lèi)型不同(AD的Aβ和tau,PD的α-突觸核蛋白,HD的亨廷頓蛋白),但慢性神經(jīng)炎癥是它們共享的“加速器”。沒(méi)有炎癥,蛋白聚集可能不會(huì)那么快殺死神經(jīng)元。
二、炎癥在神經(jīng)系統(tǒng)疾病中的“平衡法則”
炎癥本是身體抵御傷害或感染的正常防御。但在慢性神經(jīng)系統(tǒng)疾病中,持續(xù)的神經(jīng)炎癥會(huì)形成惡性循環(huán)——神經(jīng)元損傷進(jìn)一步激活膠質(zhì)細(xì)胞,釋放更多促炎因子(如IL-6、TNF-α),加劇神經(jīng)退化。
慢性神經(jīng)炎癥的特征:
- 小膠質(zhì)細(xì)胞和星形膠質(zhì)細(xì)胞過(guò)度激活
- 促炎細(xì)胞因子、趨化因子和活性氧(ROS)大量釋放
- 血腦屏障通透性增加,外周免疫細(xì)胞浸潤(rùn)
- 腸道微生物失衡與衰老因素進(jìn)一步加重炎癥
臨床視角:?國(guó)內(nèi)研究團(tuán)隊(duì)(如首都醫(yī)科大學(xué)宣武醫(yī)院)發(fā)現(xiàn),中藥單體(如姜黃素、黃芩苷)可通過(guò)抑制NF-κB通路減輕慢性神經(jīng)炎癥,相關(guān)臨床試驗(yàn)正在進(jìn)行中。
三、神經(jīng)炎癥機(jī)制
神經(jīng)炎癥是指對(duì)感染、缺血、壓力和創(chuàng)傷等有害因素的先天性和適應(yīng)性反應(yīng)。在神經(jīng)炎癥的背景下,假設(shè)有四個(gè)不同的特征作為定義標(biāo)志:細(xì)胞因子釋放增加、小膠質(zhì)細(xì)胞激活、外周免疫細(xì)胞遷移和局部組織損傷。該反應(yīng)是由小膠質(zhì)細(xì)胞、星形膠質(zhì)細(xì)胞和免疫細(xì)胞(單核細(xì)胞、中性粒細(xì)胞、淋巴細(xì)胞)釋放細(xì)胞因子、組胺和ROS等炎癥介質(zhì)觸發(fā)的。
神經(jīng)炎癥最初是一種防御反應(yīng),但現(xiàn)在研究證明,長(zhǎng)期或過(guò)度的炎癥是各種神經(jīng)系統(tǒng)疾病,特別是退行性疾病發(fā)展的主要原因。下面列出了針對(duì)神經(jīng)炎癥觸發(fā)因素的多種方法。
1. 小膠質(zhì)細(xì)胞:從“清道夫”到“縱火犯”
小膠質(zhì)細(xì)胞占中樞神經(jīng)系統(tǒng)膠質(zhì)細(xì)胞總數(shù)的20%,是大腦的第一道防線。它們?cè)诮】荡竽X中處于“靜息”狀態(tài),不斷巡邏微環(huán)境。一旦檢測(cè)到病原體相關(guān)分子模式(PAMP)或損傷相關(guān)分子模式(DAMP),它們會(huì)迅速激活。
但小膠質(zhì)細(xì)胞的激活不是單模式的。根據(jù)巨噬細(xì)胞的分類(lèi)體系,小膠質(zhì)細(xì)胞可以分為兩個(gè)極端:
- M1型(經(jīng)典激活):由脂多糖(LPS)和干擾素-γ(IFN-γ)誘導(dǎo)。這種狀態(tài)下,小膠質(zhì)細(xì)胞大量釋放促炎細(xì)胞因子——IL-1β、IL-6、TNF-α、IL-23,以及趨化因子(CCL2、CXCL10)。它們還產(chǎn)生誘導(dǎo)型一氧化氮合酶(iNOS),生成大量NO和超氧化物,形成過(guò)氧亞硝酸鹽,對(duì)神經(jīng)元產(chǎn)生氧化損傷。M1型小膠質(zhì)細(xì)胞是神經(jīng)退行性疾病中的“壞人”。
- M2型(選擇性激活):由IL-4或IL-13誘導(dǎo)。它們釋放抗炎因子(IL-10、TGF-β)、神經(jīng)營(yíng)養(yǎng)因子(BDNF、IGF-1),并表達(dá)精氨酸酶-1(Arg-1)來(lái)促進(jìn)組織修復(fù)和細(xì)胞外基質(zhì)重建。M2型是“好人”。
在健康的炎癥反應(yīng)中,小膠質(zhì)細(xì)胞會(huì)先切換到M1型清除威脅,然后迅速轉(zhuǎn)到M2型修復(fù)損傷。但在慢性神經(jīng)退行性疾病中,這個(gè)切換失靈了——小膠質(zhì)細(xì)胞被持續(xù)困在M1狀態(tài)。AD患者尸檢腦組織中,圍繞Aβ斑塊的小膠質(zhì)細(xì)胞高度表達(dá)M1標(biāo)志物(CD68、MHC-II),而M2標(biāo)志物(CD163、CD206)表達(dá)很低。
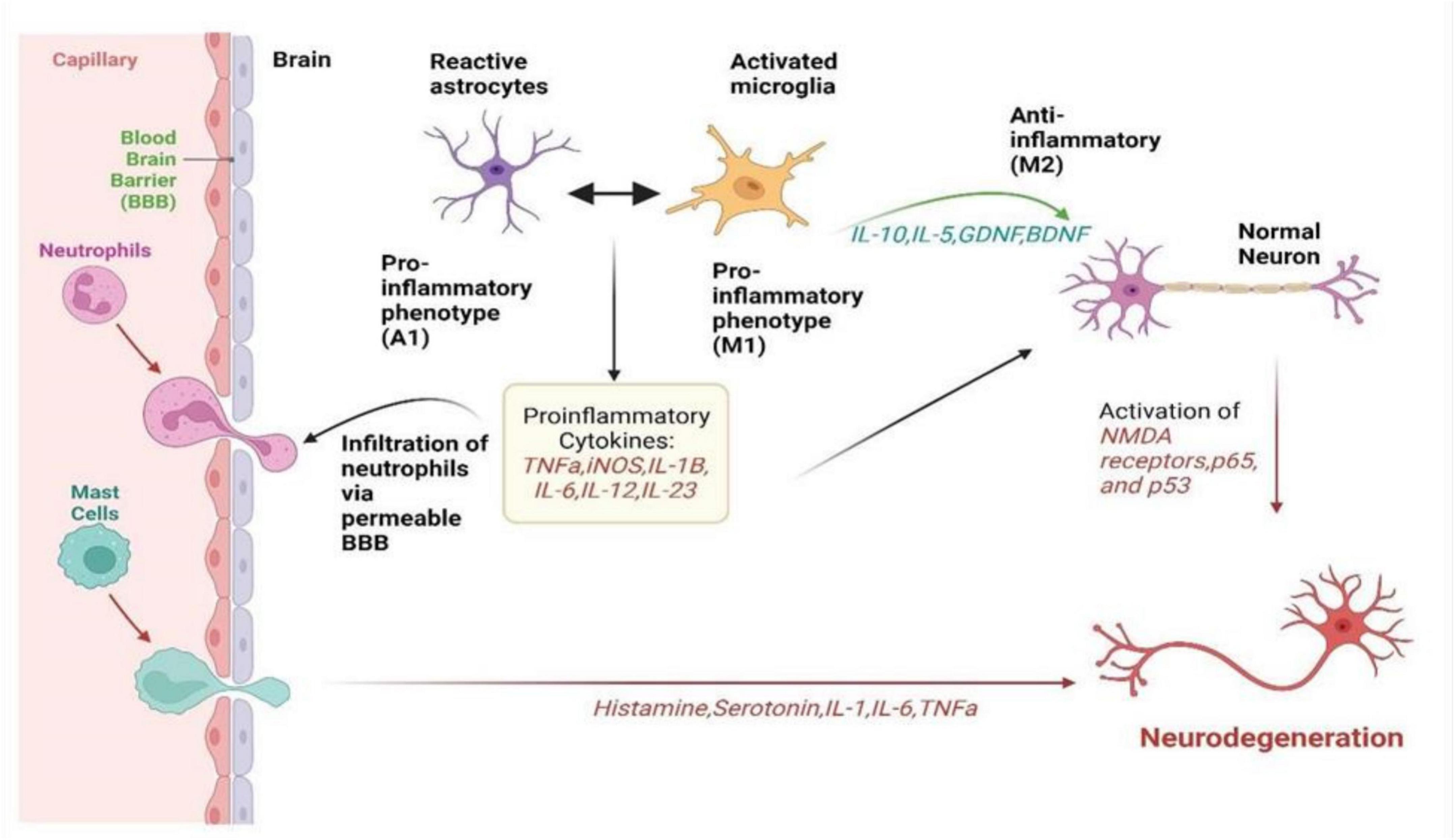
2. 星形膠質(zhì)細(xì)胞:從支持細(xì)胞到炎癥放大器
星形膠質(zhì)細(xì)胞是大腦中數(shù)量最多的膠質(zhì)細(xì)胞,它們?cè)矩?fù)責(zé)維持離子平衡、攝取谷氨酸、提供代謝支持、形成血腦屏障(BBB)。但在神經(jīng)炎癥中,它們也會(huì)“黑化”。
類(lèi)似小膠質(zhì)細(xì)胞的M1/M2分類(lèi),星形膠質(zhì)細(xì)胞被分為A1型和A2型:
- A1型(神經(jīng)毒性):被活化的小膠質(zhì)細(xì)胞分泌的IL-1α、TNF-α和C1q誘導(dǎo)。A1星形膠質(zhì)細(xì)胞失去正常的支持功能(不再促進(jìn)突觸形成、不再吞噬突觸碎片),反而分泌神經(jīng)毒性因子(尚未完全鑒定的補(bǔ)體成分和脂質(zhì)介質(zhì))。研究發(fā)現(xiàn),A1星形膠質(zhì)細(xì)胞在AD、PD、HD、ALS、MS的尸檢組織中廣泛存在,而且它們出現(xiàn)在疾病早期。
- A2型(神經(jīng)保護(hù)):被缺血誘導(dǎo),分泌神經(jīng)營(yíng)養(yǎng)因子(BDNF、GDNF),促進(jìn)神經(jīng)元存活和突觸修復(fù)。
星形膠質(zhì)細(xì)胞還通過(guò)調(diào)控BBB完整性來(lái)影響神經(jīng)炎癥。在炎癥狀態(tài)下,星形膠質(zhì)細(xì)胞的足突會(huì)從血管壁上回縮,導(dǎo)致BBB通透性增加——血漿蛋白進(jìn)入腦實(shí)質(zhì),進(jìn)一步激活小膠質(zhì)細(xì)胞,形成惡性循環(huán)。同時(shí),BBB的破壞也讓外周免疫細(xì)胞更容易浸潤(rùn)中樞神經(jīng)系統(tǒng)。
3. 外周免疫細(xì)胞:中樞神經(jīng)系統(tǒng)不再是“免疫豁免”
過(guò)去認(rèn)為大腦是“免疫豁免器官”,但現(xiàn)在知道那是錯(cuò)的。在健康狀態(tài)下,確實(shí)有少量T細(xì)胞在腦膜和脈絡(luò)叢中巡邏。但當(dāng)神經(jīng)炎癥發(fā)生時(shí),外周免疫細(xì)胞會(huì)大量涌入。
- 中性粒細(xì)胞:第一個(gè)到達(dá)損傷部位的細(xì)胞。它們釋放蛋白酶和ROS,幫助清除碎片,但也可能損傷周?chē)M織。
- 單核細(xì)胞/巨噬細(xì)胞:浸潤(rùn)后可以分化為小膠質(zhì)細(xì)胞樣細(xì)胞,但它們更容易保持促炎表型。
- T細(xì)胞:CD4+ T細(xì)胞(尤其是Th1和Th17亞型)在MS的脫髓鞘病變中大量存在。它們通過(guò)釋放IFN-γ和IL-17激活小膠質(zhì)細(xì)胞和星形膠質(zhì)細(xì)胞。CD8+ T細(xì)胞則直接攻擊表達(dá)抗原的神經(jīng)元或膠質(zhì)細(xì)胞。
- B細(xì)胞:在MS患者腦脊液中,B細(xì)胞和漿細(xì)胞數(shù)量顯著增加。它們產(chǎn)生自身抗體(如抗髓鞘少突膠質(zhì)細(xì)胞糖蛋白抗體),促進(jìn)補(bǔ)體介導(dǎo)的脫髓鞘。針對(duì)CD20的B細(xì)胞清除療法(如利妥昔單抗)在MS中有效,這直接證明了B細(xì)胞在神經(jīng)炎癥中的作用。
- NK細(xì)胞:通過(guò)釋放IFN-γ和穿孔素影響神經(jīng)膠質(zhì)細(xì)胞和神經(jīng)元。
4. 細(xì)胞因子風(fēng)暴:炎癥信號(hào)如何放大
細(xì)胞因子是免疫細(xì)胞之間的“信使”。在神經(jīng)炎癥中,幾個(gè)關(guān)鍵的細(xì)胞因子成為治療靶點(diǎn):
- TNF-α:由小膠質(zhì)細(xì)胞和星形膠質(zhì)細(xì)胞產(chǎn)生,激活NF-κB通路,誘導(dǎo)更多炎癥因子。TNF-α水平在AD、PD患者腦脊液中升高。
- IL-1β:通過(guò)激活NLRP3炎癥小體產(chǎn)生。IL-1β可以誘導(dǎo)神經(jīng)元凋亡,促進(jìn)淀粉樣前體蛋白(APP)加工成Aβ。
- IL-6:在急性期反應(yīng)中升高,慢性升高則與認(rèn)知下降相關(guān)。
- IFN-γ:主要由Th1細(xì)胞和NK細(xì)胞產(chǎn)生,是強(qiáng)效的小膠質(zhì)細(xì)胞激活劑,促使M1極化。
- GM-CSF(粒細(xì)胞-巨噬細(xì)胞集落刺激因子):促進(jìn)樹(shù)突狀細(xì)胞和巨噬細(xì)胞的分化和活化。
這些細(xì)胞因子的作用是通過(guò)與受體結(jié)合,激活JAK-STAT通路或MAPK通路,從而啟動(dòng)下游基因轉(zhuǎn)錄。這也就是為什么JAK抑制劑(如托法替布)或p38 MAPK抑制劑在神經(jīng)炎癥模型中被測(cè)試的原因。
四、神經(jīng)炎癥在不同神經(jīng)退行性疾病中的角色
與神經(jīng)炎癥相關(guān)的神經(jīng)退行性疾病包括一類(lèi)影響脊髓和大腦,導(dǎo)致神經(jīng)組織逐漸退化和死亡的疾病在這些疾病中,免疫細(xì)胞釋放到中樞神經(jīng)系統(tǒng),引起炎癥,導(dǎo)致神經(jīng)組織退化。每種疾病都有其獨(dú)特的癥狀和發(fā)展過(guò)程,但它們都有一個(gè)共同點(diǎn),即神經(jīng)炎癥在其病理生理學(xué)中起著關(guān)鍵作用。阿爾茨海默病
阿爾茨海默氏病(AD)是癡呆癥最常見(jiàn)的病因,其特點(diǎn)是進(jìn)行性神經(jīng)變性。AD的特點(diǎn)是持續(xù)的退行性過(guò)程,最初表現(xiàn)為記憶障礙,隨后導(dǎo)致認(rèn)知能力下降,從而影響行為、語(yǔ)言、視覺(jué)空間定向,并最終影響運(yùn)動(dòng)系統(tǒng)。
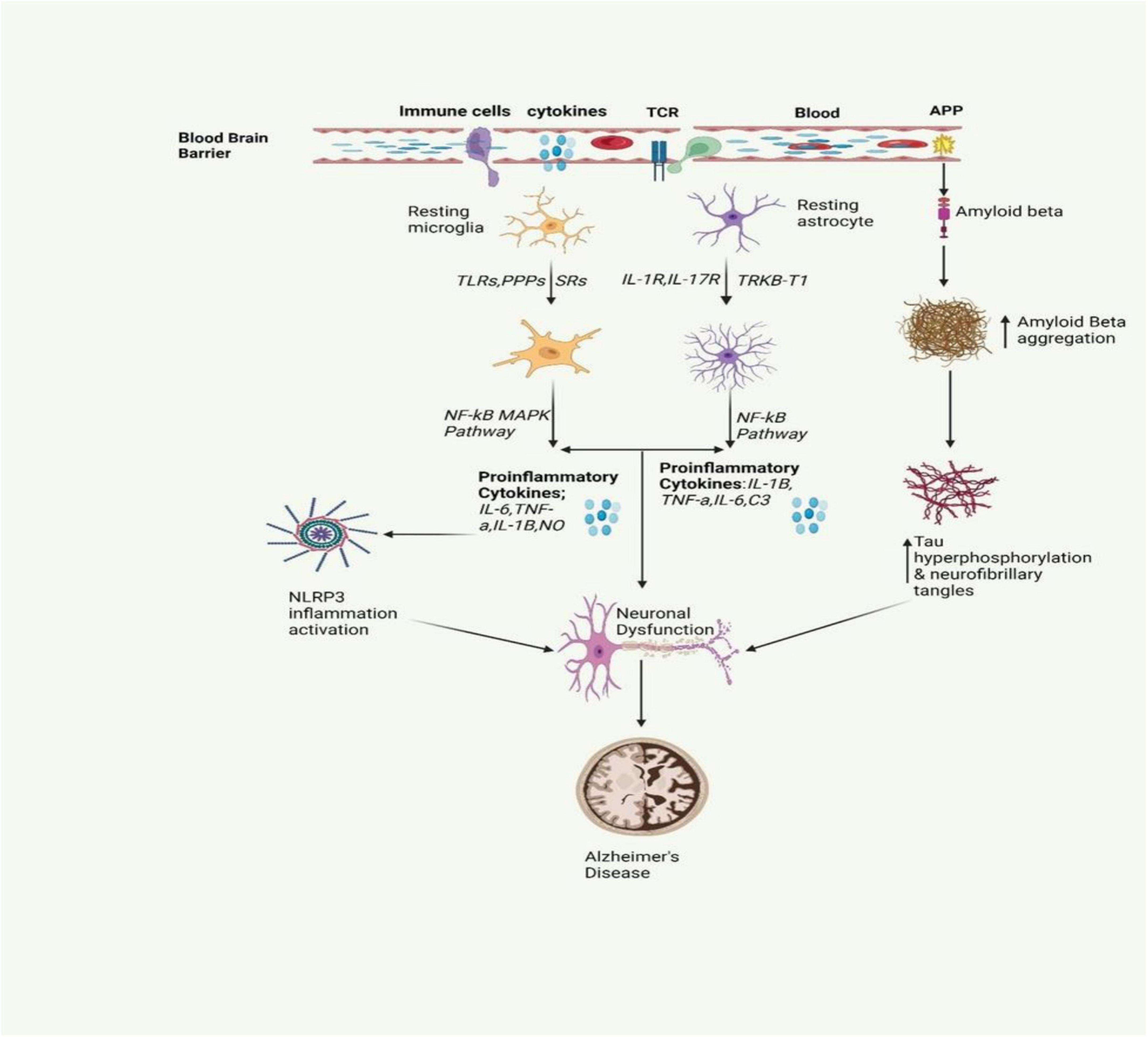
它涉及小膠質(zhì)細(xì)胞和星形膠質(zhì)細(xì)胞的激活,導(dǎo)致炎癥細(xì)胞因子的釋放。這種激活還會(huì)觸發(fā)β淀粉樣蛋白的釋放,β淀粉樣蛋白是一種對(duì)于神經(jīng)原纖維纏結(jié)的形成至關(guān)重要的蛋白質(zhì)。這些纏結(jié)和促炎細(xì)胞因子會(huì)導(dǎo)致神經(jīng)元功能障礙,這是AD的一個(gè)關(guān)鍵特征。
如圖2所示,AD的神經(jīng)病理學(xué)特征包括細(xì)胞外Aβ(淀粉樣蛋白β)斑塊和細(xì)胞內(nèi)過(guò)度磷酸化tau(p-τ)形成神經(jīng)原纖維纏結(jié),并伴有突觸和神經(jīng)元損失。當(dāng)神經(jīng)膠質(zhì)細(xì)胞(主要是小膠質(zhì)細(xì)胞和星形膠質(zhì)細(xì)胞)被激活時(shí),AD中的神經(jīng)炎癥就會(huì)發(fā)生。這種激活促使炎癥因子釋放,這些炎癥因子主要是細(xì)胞因子和趨化因子,進(jìn)而圍繞老年斑和大腦中受損的神經(jīng)元。
帕金森病
PD的特征是黑質(zhì)致密部多巴胺能神經(jīng)元的進(jìn)行性丟失,以及路易小體(主要成分為α-突觸核蛋白)的形成。
α-突觸核蛋白從神經(jīng)元釋放后,可以被小膠質(zhì)細(xì)胞攝取。異常的α-突觸核蛋白寡聚體結(jié)合TLR2,激活NF-κB通路,導(dǎo)致TNF-α、IL-1β、IL-6的釋放。這些細(xì)胞因子反過(guò)來(lái)作用于多巴胺能神經(jīng)元,加重線粒體功能障礙和氧化應(yīng)激。
有趣的是,PD的炎癥可能起源于腸道。α-突觸核蛋白在腸道神經(jīng)系統(tǒng)中沉積,通過(guò)迷走神經(jīng)上行到腦干。同時(shí),腸道菌群失調(diào)(dysbiosis)導(dǎo)致腸道通透性增加,細(xì)菌產(chǎn)物(如LPS)進(jìn)入門(mén)脈循環(huán),激活全身免疫系統(tǒng),進(jìn)而影響大腦。這就是為什么PD患者的結(jié)腸活檢中可以看到α-突觸核蛋白聚集,而糞便移植或益生菌治療在動(dòng)物模型中顯示出抗炎和神經(jīng)保護(hù)作用(圖3)。
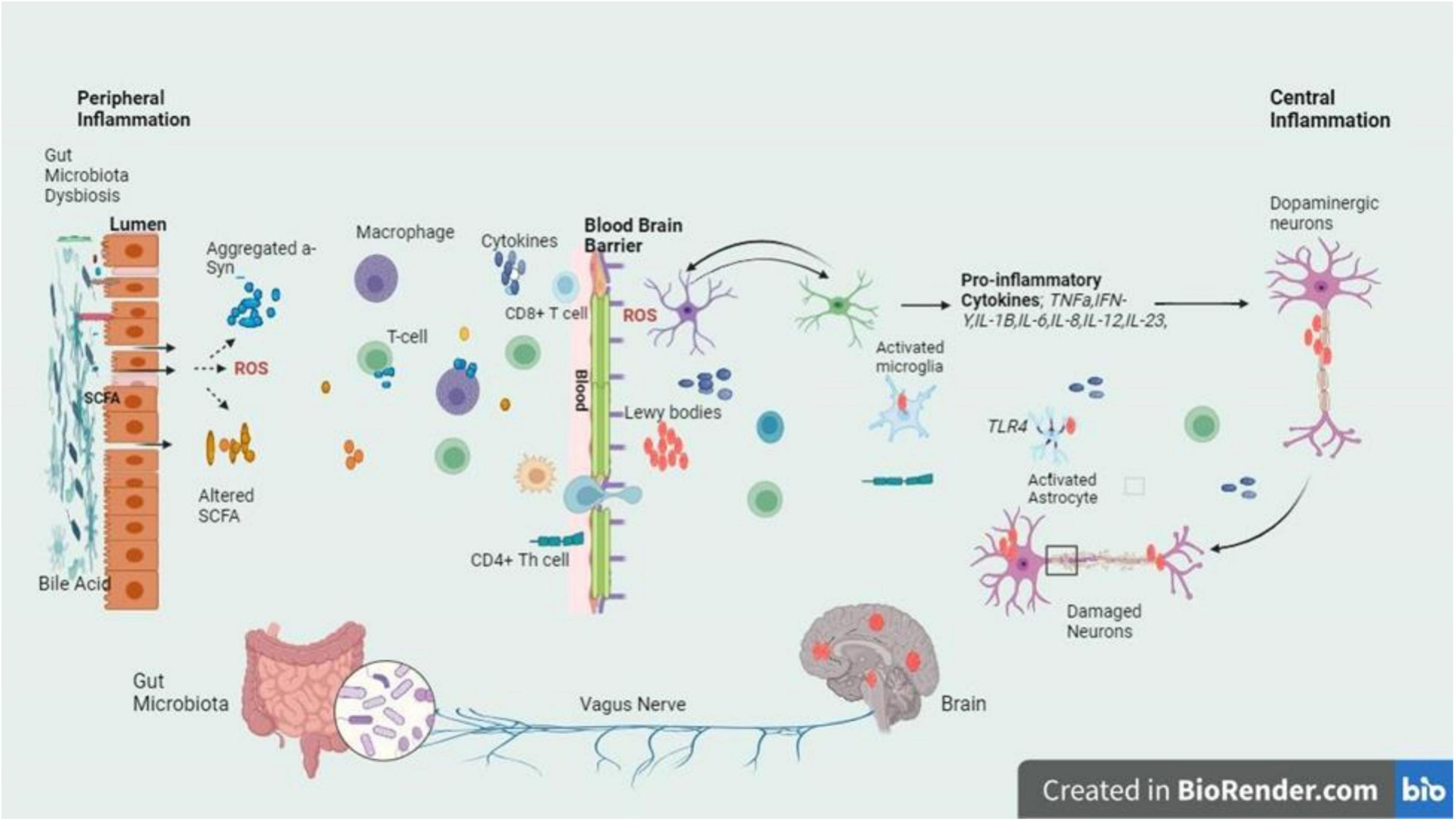
菌群失調(diào)導(dǎo)致腸道微生物群組成失衡,進(jìn)而促進(jìn)炎性細(xì)胞因子的釋放。這些細(xì)胞因子突破BBB并滲入大腦,對(duì)多巴胺能神經(jīng)元產(chǎn)生有害影響。該圖強(qiáng)調(diào)了菌群失調(diào)誘導(dǎo)的炎癥在導(dǎo)致帕金森病神經(jīng)退行性特征中的關(guān)鍵作用,并強(qiáng)調(diào)了腸道-大腦軸中緩解疾病進(jìn)展的潛在治療靶點(diǎn)。
多發(fā)性硬化癥、亨廷頓病和肌萎縮側(cè)索硬化癥
MS是自身免疫性脫髓鞘疾病的典型代表。與AD和PD不同,MS的初始驅(qū)動(dòng)因素是外周免疫系統(tǒng)的異常激活——自身反應(yīng)性T細(xì)胞(尤其是Th17)穿越BBB進(jìn)入中樞神經(jīng)系統(tǒng),識(shí)別髓鞘抗原(如髓鞘堿性蛋白、蛋白脂蛋白、髓鞘少突膠質(zhì)細(xì)胞糖蛋白),引發(fā)一系列炎癥級(jí)聯(lián)。
在活動(dòng)性MS病變中,小膠質(zhì)細(xì)胞和浸潤(rùn)的巨噬細(xì)胞圍繞在脫髓鞘軸突周?chē)淌伤枨仕槠K鼈冡尫诺腡NF-α、IL-1β、一氧化氮等直接損傷少突膠質(zhì)細(xì)胞和軸突。星形膠質(zhì)細(xì)胞反應(yīng)性增生,形成膠質(zhì)疤痕,雖然這有助于限制病變范圍,但也阻礙了髓鞘再生。
值得注意的是,MS的進(jìn)展性階段(primary progressive MS和secondary progressive MS)更多地由中樞神經(jīng)系統(tǒng)內(nèi)的“隔室化”炎癥驅(qū)動(dòng)——腦膜中形成B細(xì)胞濾泡樣結(jié)構(gòu),產(chǎn)生寡克隆抗體,促進(jìn)皮層脫髓鞘和神經(jīng)元丟失。這也是為什么針對(duì)B細(xì)胞的療法(如ocrelizumab)在進(jìn)展性MS中有效的原因。
亨廷頓病(HD)是一種導(dǎo)致神經(jīng)元進(jìn)行性退化的遺傳性疾病。它是由亨廷頓基因的重復(fù)突變引起的。HD是一種神經(jīng)退行性疾病,其特征是紋狀體神經(jīng)元選擇性喪失,導(dǎo)致運(yùn)動(dòng)和認(rèn)知障礙,并常常在癥狀出現(xiàn)后10-15年內(nèi)導(dǎo)致死亡(圖4)。
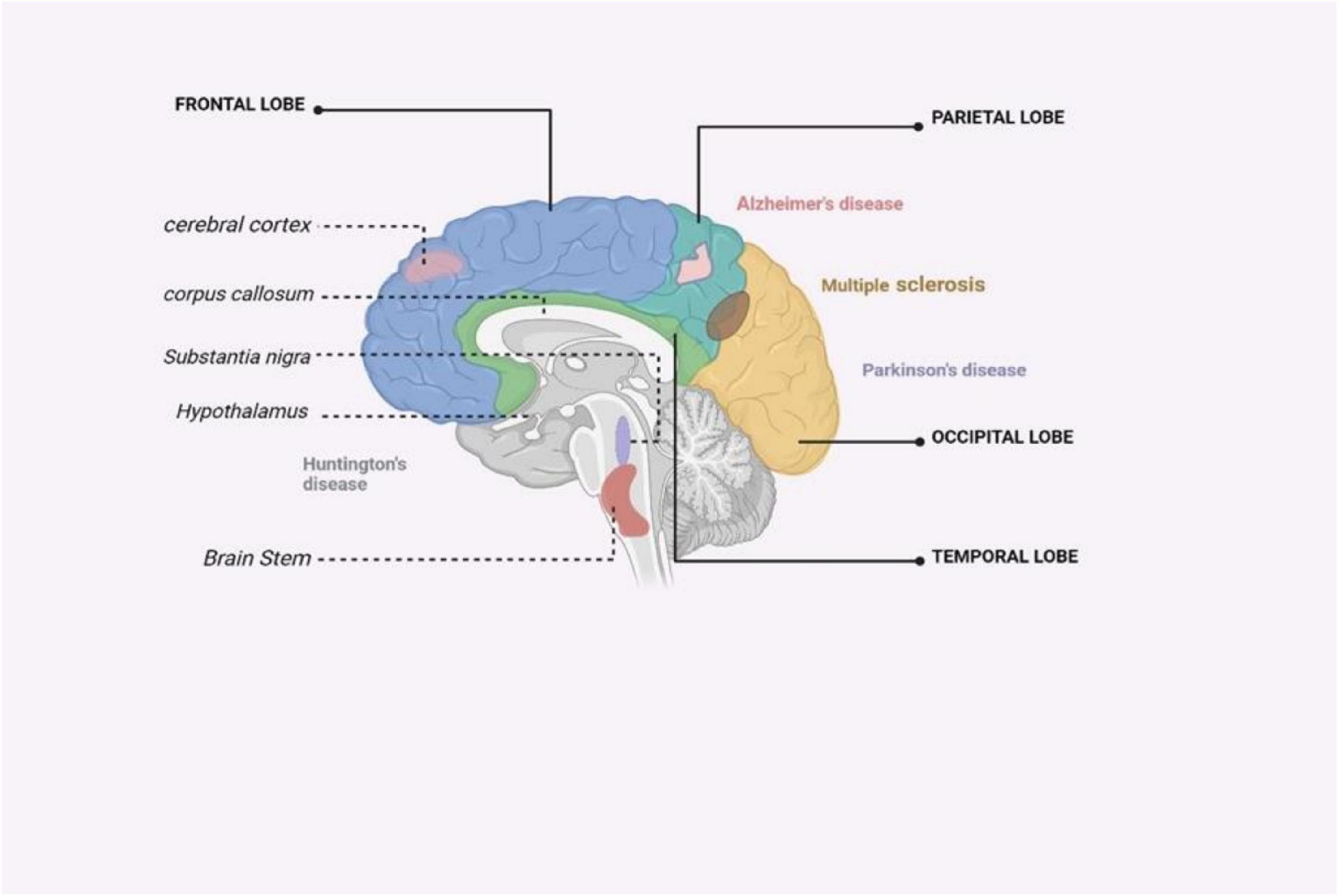
漸凍癥(ALS)是一種快速進(jìn)展的神經(jīng)退行性疾病,其特征是上運(yùn)動(dòng)神經(jīng)元和下運(yùn)動(dòng)神經(jīng)元的喪失。這會(huì)導(dǎo)致肌肉萎縮、虛弱,最終導(dǎo)致癱瘓。在ALS的神經(jīng)退行性過(guò)程中,某些蛋白質(zhì)(例如TDP-43)在細(xì)胞中錯(cuò)誤定位和聚集,導(dǎo)致神經(jīng)元細(xì)胞死亡。
該疾病可由遺傳因素和散發(fā)因素引起,遺傳形式與特定基因的突變有關(guān),例如TARDBP、FUS、SOD1和C9orf72。ALS中的炎癥涉及反應(yīng)性小膠質(zhì)細(xì)胞和星形膠質(zhì)細(xì)胞。運(yùn)動(dòng)神經(jīng)元釋放的突變型超氧化物歧化酶1會(huì)觸發(fā)小膠質(zhì)細(xì)胞和星形膠質(zhì)細(xì)胞激活,從而促進(jìn)炎癥過(guò)程。樹(shù)突狀細(xì)胞、T細(xì)胞、小膠質(zhì)細(xì)胞和巨噬細(xì)胞產(chǎn)生促進(jìn)炎癥的細(xì)胞因子和趨化因子。
四、未來(lái)治療策略:從抗炎到干細(xì)胞修復(fù)
靶向小膠質(zhì)細(xì)胞和星形膠質(zhì)細(xì)胞的藥物
NLRP3炎癥小體抑制劑:MCC950(一種選擇性NLRP3抑制劑)在AD小鼠模型中減少了Aβ沉積和IL-1β釋放,改善了認(rèn)知。目前正在進(jìn)行臨床試驗(yàn)。
TLR拮抗劑:TLR4拮抗劑(如TAK-242)在PD模型中減輕了多巴胺神經(jīng)元丟失。但由于TLR在全身免疫中的廣泛作用,系統(tǒng)給藥的副作用風(fēng)險(xiǎn)高,局部或靶向遞送可能是方向。
激酶抑制劑:p38 MAPK和JNK在炎癥信號(hào)中起核心作用。p38抑制劑(如MW150)在AD小鼠模型中減輕了突觸功能障礙和認(rèn)知下降。
腸道微生物調(diào)節(jié)
益生菌(如乳酸桿菌和雙歧桿菌)補(bǔ)充在PD患者中改善了便秘和部分運(yùn)動(dòng)癥狀。糞便微生物移植(FMT)在MS患者的小型研究中顯示出降低復(fù)發(fā)率的趨勢(shì)。但這些都是早期探索,大規(guī)模的RCT還在進(jìn)行。
抗氧化劑
白藜蘆醇(存在于葡萄皮中)通過(guò)激活SIRT1通路,減少Aβ的毒性和聚集,增加神經(jīng)發(fā)生,保護(hù)BBB。在AD患者的臨床試驗(yàn)中,高劑量白藜蘆醇(每天1-2克)可以降低腦脊液中的Aβ40和Aβ42水平,但胃腸道副作用限制了使用。
維生素E、omega-3脂肪酸、褪黑素等補(bǔ)充劑在觀察性研究中與較低的認(rèn)知下降風(fēng)險(xiǎn)相關(guān),但隨機(jī)對(duì)照試驗(yàn)的結(jié)果并不一致。這可能是因?yàn)檫@些抗氧化劑的口服生物利用度低,很難在腦內(nèi)達(dá)到有效濃度。
納米粒子靶向遞送
納米粒子(NP)可以包裹藥物,穿越BBB,將藥物精準(zhǔn)遞送到炎癥病灶。脂質(zhì)體納米粒子包裹的siRNA靶向TNF-α mRNA,在ALS小鼠模型中降低了脊髓中的TNF-α水平,延緩了疾病進(jìn)展。
外泌體是天然的納米粒子。間充質(zhì)干細(xì)胞來(lái)源的外泌體(MSC-Exos)攜帶抗炎miRNA(如miR-146a、miR-124),可以抑制小膠質(zhì)細(xì)胞的M1極化。在AD小鼠模型中,鼻腔給藥的MSC外泌體可以分布到全腦,減少Aβ斑塊和磷酸化tau,改善認(rèn)知。而且外泌體沒(méi)有活細(xì)胞的致瘤和栓塞風(fēng)險(xiǎn),是很有前景的無(wú)細(xì)胞治療策略。
基因治療
siRNA/ASO:靶向C9orf72(ALS和額顳葉癡呆最常見(jiàn)的遺傳突變)的反義寡核苷酸(ASO)在I期臨床試驗(yàn)中顯示出安全性,并降低了腦脊液中的聚(GP)蛋白水平(突變產(chǎn)生的毒性二肽重復(fù)蛋白)。但長(zhǎng)期療效還需要更大樣本的驗(yàn)證。
CRISPR基因編輯:在HD動(dòng)物模型中,利用AAV遞送CRISPR-Cas9在紋狀體中敲除突變亨廷頓基因,可以顯著減少聚集物形成并改善運(yùn)動(dòng)功能。但脫靶編輯和免疫原性仍然是臨床轉(zhuǎn)化的主要障礙。
神經(jīng)退行性疾病的干細(xì)胞療法
這是這篇綜述的重點(diǎn),也是目前最受關(guān)注的方向。為了徹底了解干細(xì)胞技術(shù)如何用于治療神經(jīng)退行性疾病,我們必須了解不同的干細(xì)胞特征如何與疾病機(jī)制相互作用(圖5)。
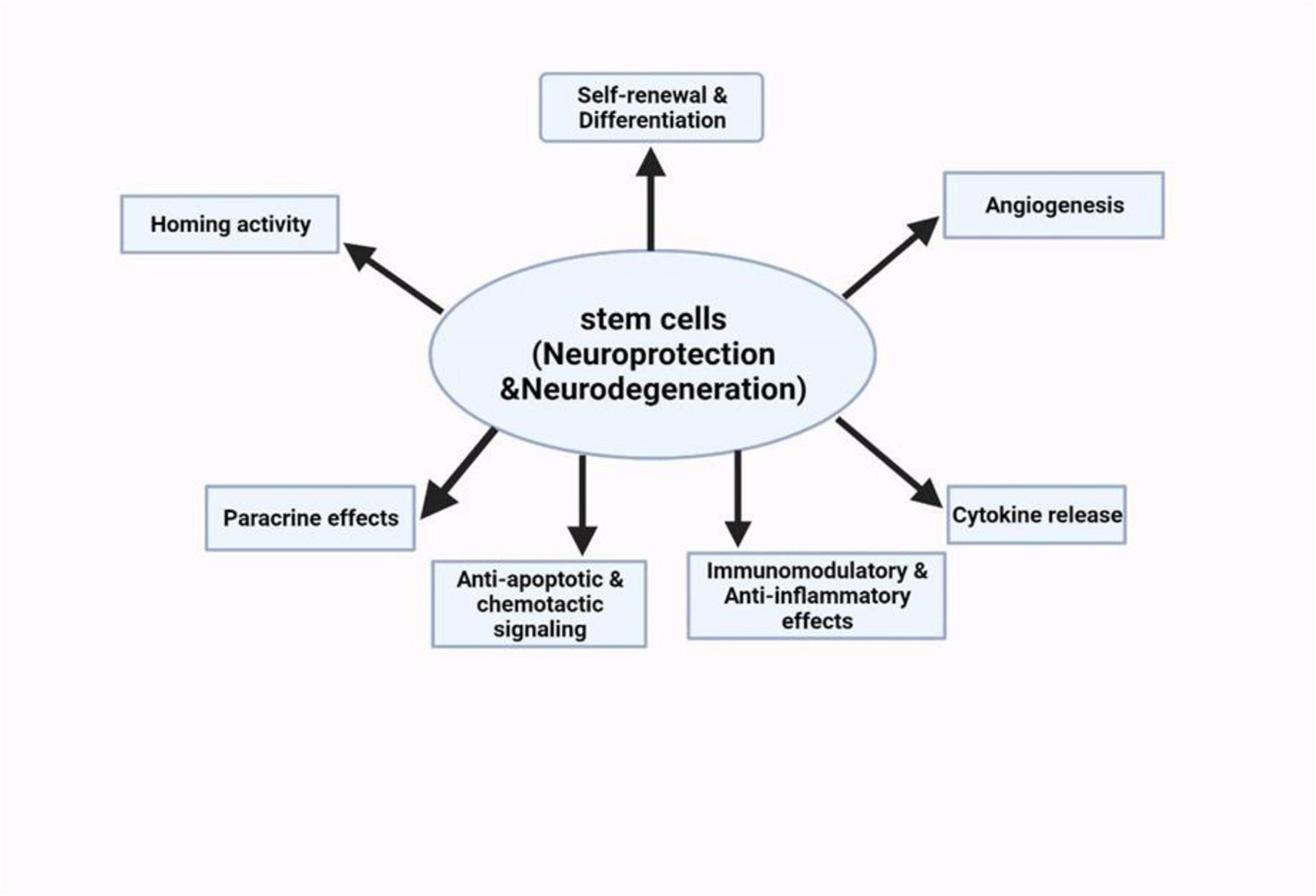
間充質(zhì)干細(xì)胞(MSC):MSC不主要通過(guò)分化成神經(jīng)元來(lái)發(fā)揮作用,而是靠旁分泌和免疫調(diào)節(jié)。
在AD模型中,鞘內(nèi)注射人臍帶MSC(UC-MSC)的小鼠,大腦中的小膠質(zhì)細(xì)胞活化標(biāo)志物(Iba-1)和星形膠質(zhì)細(xì)胞標(biāo)志物(GFAP)顯著降低,氧化應(yīng)激指標(biāo)(MDA)下降,抗凋亡蛋白(Bcl-2)升高。行為學(xué)上,這些小鼠在水迷宮實(shí)驗(yàn)中找到平臺(tái)的潛伏期縮短,表明學(xué)習(xí)記憶能力改善。
在PD模型中,靜脈注射MSC可以增加紋狀體中的多巴胺水平,保護(hù)黑質(zhì)多巴胺神經(jīng)元免于凋亡。機(jī)制上,MSC分泌的GDNF是關(guān)鍵——GDNF是多巴胺神經(jīng)元最有效的生存因子。在6-OHDA損毀的大鼠模型中,MSC移植組的旋轉(zhuǎn)行為(阿樸嗎啡誘導(dǎo))從術(shù)前的8-10轉(zhuǎn)/分鐘降低到2-3轉(zhuǎn)/分鐘。
在MS中,MSC通過(guò)抑制T細(xì)胞增殖、誘導(dǎo)Treg生成、促進(jìn)M2小膠質(zhì)細(xì)胞極化,減輕了EAE(實(shí)驗(yàn)性自身免疫性腦脊髓炎)模型的脫髓鞘和癱瘓。
神經(jīng)干細(xì)胞(NSC)和iPSC來(lái)源細(xì)胞:與MSC不同,NSC可以直接分化成丟失的神經(jīng)元類(lèi)型,實(shí)現(xiàn)結(jié)構(gòu)修復(fù)。
在帕金森病中,移植人類(lèi)多能干細(xì)胞(ESC或iPSC)來(lái)源的多巴胺能祖細(xì)胞進(jìn)入患者殼核,已經(jīng)在多個(gè)臨床試驗(yàn)中開(kāi)展。2024年發(fā)表的日本京都大學(xué)I/II期試驗(yàn)(Nature)顯示,7例患者中有4例在24個(gè)月隨訪時(shí)運(yùn)動(dòng)癥狀改善,PET證實(shí)移植細(xì)胞存活并產(chǎn)生多巴胺,無(wú)腫瘤形成。中國(guó)的同類(lèi)試驗(yàn)也在進(jìn)行中。
在ALS中,移植脊髓來(lái)源的NSC可以分化成星形膠質(zhì)細(xì)胞,為運(yùn)動(dòng)神經(jīng)元提供支持。Neuralstem公司的NSI-566細(xì)胞系(人脊髓來(lái)源NSC)在I期試驗(yàn)中被植入ALS患者脊髓灰質(zhì),結(jié)果顯示安全,部分患者的功能下降速率減慢。
干細(xì)胞治療的挑戰(zhàn):細(xì)胞存活率低(移植后第一周可能死亡90%以上)、致瘤風(fēng)險(xiǎn)(尤其是iPSC來(lái)源細(xì)胞)、免疫排斥(異體細(xì)胞)、最佳劑量和給藥途徑不明確、長(zhǎng)期安全性數(shù)據(jù)缺乏。盡管如此,MSC因其良好的安全性和易于獲取,已經(jīng)進(jìn)入了許多臨床試驗(yàn),而多能干細(xì)胞來(lái)源的產(chǎn)品則面臨更嚴(yán)格的監(jiān)管。
五、結(jié)論
神經(jīng)炎癥是連接蛋白聚集、線粒體功能障礙、氧化應(yīng)激、突觸丟失和神經(jīng)元死亡的核心樞紐。靶向神經(jīng)炎癥并不需要完全“消除”炎癥——那會(huì)破壞正常的防御功能——而是需要把失衡的M1/M2、A1/A2比例重新調(diào)回來(lái)。
目前最有希望的抗神經(jīng)炎癥策略包括:針對(duì)NLRP3或TLR的小分子抑制劑、基于外泌體的miRNA遞送、以及干細(xì)胞(特別是MSC)的免疫調(diào)節(jié)作用。干細(xì)胞治療的優(yōu)勢(shì)在于它不是一個(gè)單一的靶點(diǎn),而是通過(guò)分泌多種因子整體性地調(diào)節(jié)微環(huán)境,這符合神經(jīng)炎癥網(wǎng)絡(luò)的復(fù)雜性。
但要真正進(jìn)入臨床,還需要解決:如何在正確的時(shí)間窗口干預(yù)(早期比晚期有效)、如何實(shí)現(xiàn)BBB穿透(靜脈注射MSC大部分被肺截留,鞘內(nèi)或鼻腔給藥可能更優(yōu))、以及如何建立預(yù)測(cè)療效的生物標(biāo)志物(如腦脊液中的TREM2、NfL)。
未來(lái)的治療很可能是組合拳——基因編輯糾正遺傳缺陷,干細(xì)胞調(diào)節(jié)微環(huán)境,納米粒子靶向遞送抗炎藥物。而這一切的基礎(chǔ),是我們對(duì)神經(jīng)炎癥機(jī)制的深入理解。
六、常見(jiàn)問(wèn)題
參考資料:Adamu A, Li S, Gao F and Xue G (2024) The role of neuroinflammation in neurodegenerative diseases: current understanding and future therapeutic targets. Front. Aging Neurosci. 16:1347987. doi: 10.3389/fnagi.2024.1347987
免責(zé)說(shuō)明:本文僅用于傳播科普知識(shí),分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專(zhuān)業(yè)建議。如有版權(quán)等疑問(wèn),請(qǐng)及時(shí)跟本公眾號(hào)聯(lián)系,我們將在第一時(shí)間處理。



 掃碼添加官方微信
掃碼添加官方微信